1805年春天,瑞士日内瓦的街道上弥漫着一种令人不安的气息。医生加斯帕尔·维约索正注视着一具刚刚去世的年轻尸体,困惑与恐惧交织在他的眼中。这是他见过的第数十例相似的死亡——患者先是高烧不退,随后剧烈头痛、颈部僵硬,最终陷入昏迷,在痛苦中离世。这种疾病来得如此迅猛,以至于家属往往来不及道别,患者便已永远闭上了眼睛。维约索不知道,他正在见证人类历史上首次被明确记录的流行性脑膜炎大流行,而这种疾病将在接下来的两个多世纪里,夺走数百万人的生命,成为人类最恐惧的"闪电杀手"之一。
流行性脑膜炎的病原体是一种名为脑膜炎奈瑟菌(Neisseria meningitidis)的细菌,它的形态优雅而致命——在显微镜下,它们呈咖啡豆状,成对排列,被称为"双球菌"。这种细菌表面覆盖着一层多糖荚膜,如同穿戴着隐身斗篷,能够逃避人体免疫系统的追捕。更令人惊叹的是,这种细菌拥有至少12种不同的血清群,其中A、B、C、W、X、Y六种是导致人类疾病的主要类型。每一种血清群都有其独特的地理分布和流行病学特征,仿佛一支训练有素的军队,在全球不同的战场执行着各自的使命。

这种细菌最令人恐惧的特性,在于它与人类之间的微妙共生关系。在全球范围内,约有5%至10%的人口在鼻咽部无症状携带脑膜炎奈瑟菌,在某些特定人群中,这一比例甚至可以高达25%以上。这些携带者毫不知情地成为了细菌的传播媒介,通过咳嗽、打喷嚏、亲密接触,将致命的种子播撒开来。然而,细菌从鼻咽部侵入血液并最终穿透血脑屏障的过程,至今仍是医学界最令人着迷的谜题之一。科学家们发现,只有当宿主的免疫系统处于某种特定的脆弱状态时——比如合并上呼吸道病毒感染、暴露于干燥多尘的环境、或是经历极度疲劳——这些潜伏的细菌才会突然暴起,发起致命的进攻。
脑膜炎奈瑟菌穿透血脑屏障的过程堪称微生物界的特种作战。当细菌突破鼻咽部黏膜进入血液后,它们首先需要突破的是人体最严密的防御工事——血脑屏障。这道由内皮细胞紧密连接构成的城墙,原本能够阻挡几乎所有有害物质进入中枢神经系统。然而,脑膜炎奈瑟菌进化出了一整套精密的入侵工具。它们表面的IV型菌毛如同微型抓钩,能够牢牢抓住血管内皮细胞;特殊的表面蛋白CD147则充当着入侵的钥匙,与内皮细胞上的受体精确对接。一旦锚定成功,细菌便会触发一系列细胞信号通路,使内皮细胞的紧密连接松开,为它们打开通往大脑的门户。
当细菌成功侵入蛛网膜下腔,它们释放的内毒素便开始了疯狂的屠杀。脑膜炎奈瑟菌的脂寡糖(LOS)是一种强效的炎症触发器,它能够激活免疫细胞释放大量促炎细胞因子,包括肿瘤坏死因子-α、白细胞介素-1β和白细胞介素-6。这场被医学界称为"细胞因子风暴"的免疫反应,原本旨在消灭入侵者,却反而成为了加速患者死亡的帮凶。炎症导致血管通透性增加,血浆渗入脑组织,颅内压急剧升高,最终压迫脑干,导致呼吸和心跳停止。从细菌入侵到患者死亡,整个过程可能仅需24至48小时,这就是流行性脑膜炎被称为"闪电杀手"的原因。
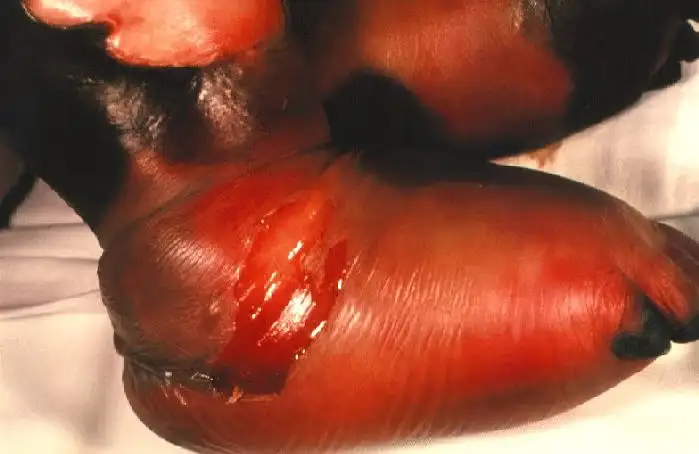
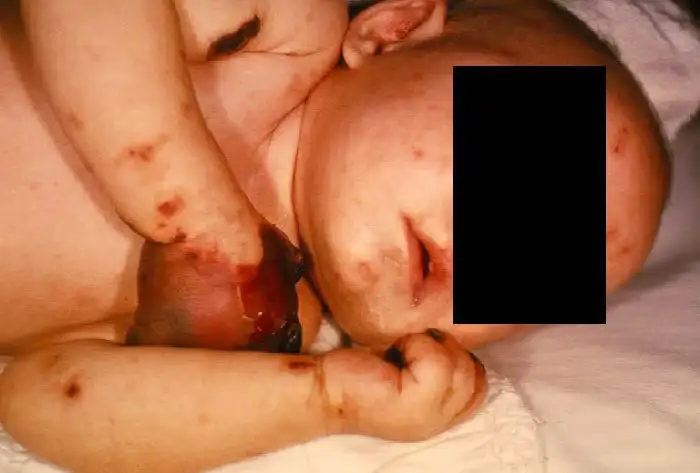
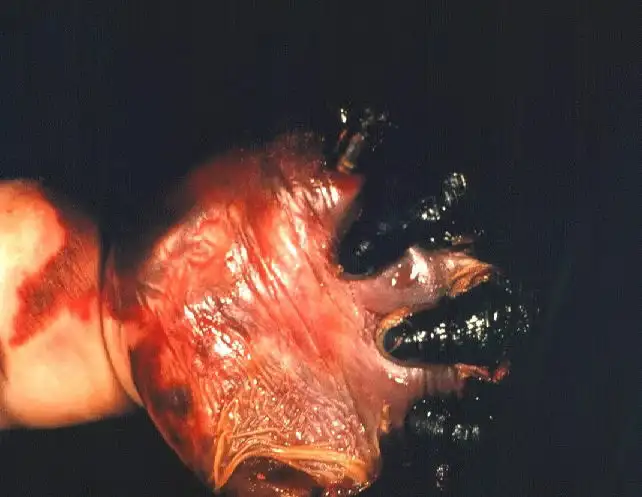
在部分患者身上,疾病以一种更加残酷的形式展现——脑膜炎球菌血症。这种系统性感染会导致最令人毛骨悚然的临床表现:暴发性紫癜。患者的皮肤上首先出现针尖大小的瘀点,随后迅速扩大、融合,形成大片紫黑色斑块。这是因为内毒素触发了弥散性血管内凝血(DIC),导致全身微血管内形成大量血栓,同时消耗掉所有的凝血因子,造成广泛出血。患者的四肢可能因为血管阻塞而发生坏疽,即使幸存下来,也不得不接受截肢的命运。这种临床表现如此典型而骇人,以至于在抗生素问世之前的年代,医生仅凭皮肤上的紫斑就能做出诊断,而这样的诊断往往意味着死亡判决。
1887年,奥地利病理学家安东·魏克斯尔鲍姆在一位脑膜炎患者的脑脊液中首次分离出了脑膜炎奈瑟菌,为这种疾病的确切病因提供了科学证据。然而,发现病原体并不意味着找到治疗方法。在接下来的半个世纪里,流行性脑膜炎的死亡率始终维持在70%至90%之间,医院里充斥着绝望的哭喊和临终的呻吟。医生们尝试了各种疗法——放血、冷水浴、高剂量水银——但都无法阻止疾病的进程。每一次流行都像是一场无法预料的灾难,突然降临,夺走无数生命,然后悄然消失,留下一地悲伤。
1904年冬天,一场大规模的脑膜炎流行席卷了纽约市。在短短几个月内,超过3000人死去,医院走廊里躺满了呻吟的患者。刚成立不久的洛克菲勒医学研究所所长西蒙·弗莱克斯纳被任命为市政府特别委员会成员,负责调查这场疫情。弗莱克斯纳是一位经验丰富的病理学家,十年前曾参与调查马里兰州煤矿工人中爆发的脑膜炎疫情。他深知,当时唯一可用的治疗方法是使用马血清制备的抗血清,但常规的皮下注射几乎无效——血清无法到达细菌肆虐的大脑。
弗莱克斯纳做出了一个大胆的决定:将抗血清直接注射到患者的椎管内,也就是后来被称为"鞘内注射"的技术。这项操作需要在腰椎部位穿刺,将针头插入蛛网膜下腔,直接将药物送达感染部位。1907年,在俄亥俄州爆发的另一场疫情中,弗莱克斯纳的新疗法首次应用于人体。结果令人震惊:患者的死亡率从原来的75%下降到约35%,几乎减半。这一突破性进展让弗莱克斯纳声名大噪,也帮助说服了约翰·D·洛克菲勒在1908年承诺出资建造洛克菲勒医院。这种治疗方法在此后的三十年间一直是唯一有效的救命手段。

第一次世界大战期间,脑膜炎再次成为军队的噩梦。拥挤的营房、恶劣的卫生条件、年轻的男性群体——所有这些都是脑膜炎传播的理想环境。在英国、法国、德国和美国的军营中,疫情此起彼伏。尽管总病例数相对较少——美国军队中报告了约5839例——但疾病的高死亡率让军方不敢掉以轻心。弗莱克斯纳实验室改进了抗血清的制备方法,并通过洛克菲勒基金会的支持,在前线广泛分发。这是历史上首次大规模的血清治疗行动,为后来的抗生素时代积累了宝贵的经验。
1937年,一个革命性的发现改变了一切。弗朗索瓦·施文特克在巴尔的摩的西德纳姆医院首次使用磺胺类药物成功治疗了脑膜炎患儿。磺胺类药物是人类历史上第一种系统性抗菌药物,它的出现让脑膜炎的治疗进入了一个全新的时代。在磺胺类药物出现之前,即使是最有经验的医生,面对脑膜炎患者也只能祈祷奇迹;而在此之后,医生们终于拥有了真正有效的武器。死亡率进一步下降到10%至20%左右,这在当时简直是医学奇迹。然而,好景不长,耐药菌株很快开始出现,磺胺类药物逐渐失去了它的光芒。
1940年代,青霉素的发现为脑膜炎治疗带来了新的希望。这种由霉菌产生的抗生素对脑膜炎奈瑟菌具有强大的杀灭作用,而且耐药性问题在当时尚未出现。然而,青霉素并非完美无缺——它难以穿透血脑屏障,需要大剂量使用才能在脑脊液中达到有效浓度。此外,部分患者对青霉素过敏,这限制了它的应用范围。在接下来的几十年里,随着头孢菌素类抗生素的出现,脑膜炎的治疗选择变得更加丰富,治疗成功率也进一步提高。如今,在及时诊断和正确治疗的情况下,流行性脑膜炎的死亡率已降至10%至15%左右。
然而,抗生素只能治疗已经发生的感染,真正的突破在于预防。脑膜炎疫苗的发展历程堪称一部医学史诗。最早期的尝试可以追溯到20世纪初,当时科学家们发现,将灭活的细菌注射到人体内可以激发免疫反应。但这些早期疫苗效果有限,且副作用明显。1960年代,美国军方开始系统研究脑膜炎疫苗,因为军队新兵营一直是脑膜炎疫情的高发场所。研究发现,提纯的细菌荚膜多糖能够激发保护性抗体反应,这成为第一代脑膜炎疫苗的基础。
1980年代,A群脑膜炎多糖疫苗在非洲脑膜炎带国家开始使用,在一定程度上控制了疫情。然而,多糖疫苗有一个致命的弱点:它们无法激发T细胞依赖的免疫记忆,这意味着保护效果持续时间短,且对婴幼儿几乎无效——而恰恰是婴幼儿最容易受到感染。1999年,英国成为世界上第一个引入C群脑膜炎结合疫苗的国家,这种将多糖与载体蛋白结合的新型疫苗能够激发更强的免疫反应,并提供持久的保护。疫苗接种计划的实施效果令人瞩目:在短短几年内,英国C群脑膜炎的发病率下降了90%以上。
非洲脑膜炎带是流行性脑膜炎最猖獗的地区。这片从塞内加尔延伸至埃塞俄比亚的撒哈拉以南非洲地区,横跨26个国家,覆盖约3亿人口。世界卫生组织的莱昂·拉佩索尼在1963年首次定义了这个区域,他注意到脑膜炎的高发区域与年降雨量300至1100毫米的地带惊人地吻合。在这里,大规模流行每隔5至12年就会发生一次,发病率可达每10万人100至1000例,是世界上最严重的地方性流行病之一。
1996年至1997年,非洲脑膜炎带经历了有记录以来最严重的一次大流行。仅尼日利亚一国就报告了超过10.9万例病例,其中近1.2万人死亡。整个地区的总病例数超过25万,死亡人数接近2.5万。医院里人满为患,走廊和帐篷里都挤满了患者。许多村庄失去了整整一代年轻人,留下的是无尽的悲痛和破碎的家庭。这场灾难震撼了国际社会,也催生了历史上最具雄心的公共卫生项目之一——脑膜炎疫苗项目。
2010年,专为非洲设计的新型A群脑膜炎结合疫苗MenAfriVac开始投入使用。这是有史以来第一种专门为发展中国家开发的疫苗,也是第一种获得世界卫生组织预认证、可以在无冷链条件下存储数天的疫苗。接种运动取得了惊人的成功:在疫苗接种覆盖率达到80%以上的地区,A群脑膜炎的发病率几乎降为零。超过3.5亿人接种了疫苗,估计避免了超过100万例病例和15万例死亡。这是人类公共卫生史上最伟大的胜利之一,证明了即使是世界上最贫困的地区,也能够通过科学和合作战胜最可怕的疾病。
然而,细菌从未停止进化。随着A群脑膜炎得到控制,C群、W群和X群开始填补生态位,引发新的疫情。2017年,尼日利亚北部爆发的C群脑膜炎疫情导致超过1.4万人感染,近1200人死亡。2019年,“脑膜炎带"国家仍然报告了超过2.2万例疑似病例。这场与细菌的战争远未结束,科学家们正在加紧研发覆盖更多血清群的广谱疫苗,希望能够彻底消除这一威胁。
流行性脑膜炎对社会的影响远不止于死亡数字。根据世界卫生组织的数据,即使在接受治疗的患者中,仍有约10%至20%的幸存者会留下永久性后遗症。听力损失是最常见的并发症,发生在约5%至10%的幸存者身上;其他并发症还包括认知障碍、癫痫、肢体瘫痪和严重的皮肤瘢痕。对于暴发性紫癜的幸存者,截肢往往是不可避免的命运。这些后遗症不仅给患者和家庭带来沉重的负担,也对社会医疗体系构成了持续的压力。
在儿童和青少年中,脑膜炎的影响尤为深远。大脑在发育过程中受到感染,可能导致学习障碍、行为问题和发育迟缓。一个原本健康聪明的孩子,可能在一场短暂的疾病后变得面目全非——无法继续学业,无法独立生活,需要终身照护。对于那些失去孩子的家庭,创伤更是难以愈合。许多父母在数十年后仍然无法从悲痛中恢复,他们的人生从此被分割成了"之前"和"之后"两部分。
流行性脑膜炎的流行病学特征也揭示了人类社会的深层不平等。在发达国家,随着疫苗的广泛使用,脑膜炎已成为相对罕见的疾病;但在发展中国家,它仍然是主要的公共卫生威胁。非洲脑膜炎带的国家大多是世界上最贫困的地区,医疗资源匮乏,诊断能力有限,疫苗覆盖率不足。当一个富裕国家的孩子在数小时内就能得到诊断和治疗时,一个非洲偏远村庄的孩子可能要步行数天才能到达最近的诊所,而此时,致命的细菌早已完成了它的破坏。
诊断流行性脑膜炎的金标准是腰椎穿刺——将一根针插入椎管,抽取脑脊液进行分析。这项技术由德国医生海因里希·昆克在1891年首次应用于临床,最初是为了缓解脑积水患者的颅内压,后来才成为诊断脑膜炎的关键手段。在显微镜下,感染脑膜炎的脑脊液呈现出浑浊的外观,白细胞数量急剧升高,蛋白质含量增加,葡萄糖含量下降——这些都是细菌性感染的典型特征。革兰染色可以显示特征性的革兰阴性双球菌,而培养则能够明确诊断并指导抗生素选择。
然而,腰椎穿刺并非总是可行的。在资源有限的地区,设备和训练有素的人员可能严重不足。在一些病例中,患者就诊时已经处于严重休克状态,进行腰椎穿刺可能带来风险。因此,世界卫生组织制定了一套临床病例定义,用于在流行期间快速识别病例:发热、头痛、颈部僵硬或意识改变,加上皮肤瘀点或瘀斑。虽然不如实验室诊断精确,但这种方法在疫情爆发期间帮助公共卫生部门快速评估形势并部署干预措施。
脑膜炎奈瑟菌的传播动力学同样复杂而迷人。这种细菌似乎与人类共同进化了数千年,发展出了一种微妙的平衡。在大多数情况下,细菌安静地居住在宿主的鼻咽部,不引起任何症状;只有在特定条件下,才会突破防线,引发侵袭性疾病。这种从无症状携带到致命感染的转变,是流行性脑膜炎最令人困惑的特征之一。科学家们提出多种假说,包括病毒共感染、环境因素、遗传易感性等,但至今仍未有定论。
遗传学研究揭示了另一个有趣的层面:某些人群比其他人更容易感染脑膜炎。例如,先天性补体缺陷的患者感染脑膜炎的风险是普通人的数千倍;脾切除患者也面临更高的风险。这些发现不仅帮助识别高危人群,也为开发新的治疗方法提供了线索。补体替代疗法和单克隆抗体正在成为重症脑膜炎治疗的潜在选择,为那些传统抗生素治疗失败的患者带来新的希望。
流行性脑膜炎还与人类的历史进程交织在一起。在中世纪,朝圣者们在前往圣地亚哥德孔波斯特拉的路上,常常会在拥挤的旅馆和客栈中感染这种疾病,因此脑膜炎曾被称为"朝圣者热”。在拿破仑战争的战场上,士兵们在恶劣的条件下聚集,脑膜炎在军营中蔓延,夺走的生命有时甚至超过战斗本身。在两次世界大战期间,军队调动和难民营为疾病的传播创造了完美的条件,每一次大规模的人口流动都伴随着疫情爆发的风险。
朝圣活动至今仍是脑膜炎传播的重要场景。1987年,沙特阿拉伯的麦加朝圣期间爆发了一次大规模的A群脑膜炎疫情,随后疾病随着返回的朝圣者传播到世界各地,引发了尼泊尔、沙特阿拉伯和乍得等国的流行。这一事件促使沙特政府要求所有朝圣者接种脑膜炎疫苗,成为朝圣签证的必要条件。这再次证明,在全球化的时代,传染病的传播不再受国界限制,任何一个地方的疫情都可能成为全球性问题。
从分子生物学的角度来看,脑膜炎奈瑟菌是一种高度可变的病原体。它的基因组频繁发生重组和水平基因转移,这使得细菌能够不断逃避宿主的免疫反应和医疗干预。科学家们发现,即使在同一次疫情中分离的菌株,也可能存在显著的遗传差异。这种变异性为疫苗开发带来了巨大挑战——一种疫苗可能对某一菌株有效,但对稍有不同的另一菌株却毫无作用。这也是为什么脑膜炎疫苗需要不断更新,以应对不断变化的病原体。
现代基因组学技术为脑膜炎防控提供了新的工具。通过全基因组测序,科学家们能够追踪疫情的传播路径,识别感染源,预测潜在的大流行菌株。2019年,一个国际研究团队利用这些技术,成功预测了一次在非洲爆发的C群脑膜炎疫情,并及时提醒当地卫生部门采取预防措施。这种"基因组流行病学"代表了传染病控制的前沿,有可能在未来的疫情应对中发挥关键作用。
对于普通人来说,了解流行性脑膜炎的警示信号可能意味着生与死的差别。这种疾病的典型三联征是高热、剧烈头痛和颈部僵硬——当患者无法将下巴贴近胸部时,医生会高度怀疑脑膜炎。然而,在疾病早期,症状可能并不典型,可能仅表现为发热、疲劳或肌肉酸痛,很容易被误认为是普通感冒或流感。皮肤瘀点或瘀斑的出现是疾病进展的危险信号,表明细菌已经开始在血液中大量繁殖,患者可能正在发展为败血症。
玻璃杯测试是一个简单但有效的家庭筛查方法:将透明玻璃杯压在皮疹上,如果斑点透过玻璃仍然可见,即所谓的"不褪色皮疹",则高度提示脑膜炎球菌感染,需要立即就医。这个测试虽然简单,却可能在关键时刻挽救生命。世界各地的脑膜炎慈善组织都在努力提高公众对这一测试的认识,希望每一位家长都能掌握这一基本的医学知识。
在治疗方面,时间就是生命。研究表明,从症状出现到开始抗生素治疗,每延迟一小时,死亡风险就会显著增加。因此,在疑似脑膜炎的病例中,医生往往会在实验室结果出来之前就开始经验性抗生素治疗,通常是第三代头孢菌素,如头孢曲松或头孢噻肟。对于严重病例,还需要支持性治疗,包括液体复苏、血管活性药物和机械通气。在暴发性紫癜患者中,重组活化蛋白C曾一度被认为是突破性治疗,但由于其出血风险,目前的使用受到限制。
预防方面,疫苗是最有效的手段。目前市面上有多种脑膜炎疫苗,包括针对A、C、W、Y群的四价结合疫苗,以及针对B群的疫苗。在许多发达国家,这些疫苗已被纳入儿童常规免疫计划。对于前往脑膜炎流行地区旅行的人,世界卫生组织建议在出发前至少10天接种适当的疫苗。对于补体缺陷患者、脾切除患者和其他免疫功能受损的人群,疫苗接种尤为重要,因为他们感染脑膜炎的风险远高于常人。
流行性脑膜炎的故事,是人类与传染病斗争史的缩影。从1805年日内瓦医生困惑的眼神,到今天覆盖数亿人的疫苗接种计划;从曾夺走90%患者生命的绝症,到如今可以被有效预防和治疗的疾病——这一历程凝聚了无数科学家、医生和公共卫生工作者的智慧与努力。然而,这场战争远未结束。在非洲的偏远村庄,在南亚的拥挤城市,在任何一个医疗资源匮乏的地方,脑膜炎奈瑟菌仍在伺机而动,等待着下一个脆弱的宿主。
疾病的阴影提醒我们,人类与微生物的共处从未真正和平过。脑膜炎奈瑟菌作为一种无症状携带率高达10%的细菌,与人类的关系更像是复杂的共生,而非简单的敌对。它在绝大多数时候安静无害,却在特定条件下暴起伤人,这种特性让流行性脑膜炎成为一种永远无法完全消除的威胁。我们能做的,是保持警惕,继续研究,不断改进预防和治疗手段,将这场博弈的天平进一步向人类倾斜。
当下一个疫情来临的时候——它终将来临——人类已经准备好了比两个世纪前更强大的武器:精准的诊断工具、有效的抗生素、保护性疫苗,以及全球协作的公共卫生网络。这些进步凝聚了无数先辈的智慧和牺牲,是我们在与微生物的无声战争中赢得的宝贵成果。然而,这些成果是脆弱的,需要我们持续投入资源、保持关注、推动创新。因为在我们看不见的地方,那些微小的生命从未停止进化,而我们的责任,就是确保人类能够永远领先一步。
参考资料
- Vieusseux G. Mémoire sur la maladie qui a régné à Genève au printemps de 1805. Journal de Médecine, Chirurgie et Pharmacie. 1805;11:163-182.
- Weichselbaum A. Ueber die Aetiologie der akuten Meningitis cerebro-spinalis. Fortschrift der Medizin. 1887;5:573-583.
- Flexner S. The results of the serum treatment in thirteen hundred cases of epidemic meningitis. Journal of Experimental Medicine. 1913;17:553-576.
- Schwentker FF, Gelman S, Long PH. The treatment of meningococcic meningitis with sulfanilamide. Journal of the American Medical Association. 1937;108:1407-1409.
- Lapeyssonnie L. La méningite cérébro-spinale en Afrique. Bulletin of the World Health Organization. 1963;28(suppl):1-114.
- Rosenstein NE, Perkins BA, Stephens DS, Popovic T, Hughes JM. Meningococcal disease. New England Journal of Medicine. 2001;344:1378-1388.
- Stephens DS. Biology and pathogenesis of the evolutionarily successful, obligate human bacterium Neisseria meningitidis. Vaccine. 2009;27S:B71-B77.
- Paireau J, Chen A, Broutin H, Grenfell B, Basta NE. Seasonal dynamics of bacterial meningitis: a time-series analysis. The Lancet Global Health. 2016;4:e370-e377.
- Trotter CL, Maiden MC. Meningococcal vaccines and herd immunity: lessons learned from serogroup C conjugate vaccination programs. Expert Review of Vaccines. 2009;8:851-861.
- World Health Organization. Meningitis. WHO Fact Sheet. 2021.
- Centers for Disease Control and Prevention. Meningococcal Disease. CDC Yellow Book 2020.
- Coureuil M, Join-Lambert O, Lécuyer H, Bourdoulous S. Mechanism of meningeal invasion by Neisseria meningitidis. Virulence. 2012;3:1-11.
- Davila S, Wright VJ, Khor CC, et al. Genome-wide association study identifies variants in the CFH region associated with host susceptibility to meningococcal disease. Nature Genetics. 2010;42:772-776.
- Caugant DA, Maiden MC. Meningococcal carriage and disease—population biology and evolution. Vaccine. 2009;27S:B64-B70.
- Tiffay K, Jodar L, Kieny MP, Socquet M, LaForce FM. The evolution of the Meningitis Vaccine Project. Clinical Infectious Diseases. 2015;61(suppl 5):S396-S403.