1947年4月18日,乌干达恩德培市附近一片名为寨卡的雨林中,一只编号766的恒河猴发起了高烧。这只猴子是洛克菲勒基金会黄热病研究项目的"哨兵动物"——它被关在树冠层的笼子里,日夜守望着丛林中蚊虫传播的疾病。科学家们提取了它的血液样本,接种到瑞士小白鼠和另一只恒河猴体内。几天后,小白鼠们相继病倒,一种前所未知的病毒从它们的大脑中被分离出来。研究人员以发现地的名字命名了这种新病毒:寨卡病毒。

乌干达的寨卡森林,一片看似宁静的热带雨林。1947年,正是在这里,科学家们从一只发高烧的恒河猴体内首次分离出寨卡病毒。这片森林成为了人类与一种隐形杀手首次相遇的见证地。
那时候没有人知道,这个被发现的微小敌人会在七十年后让全世界为之战栗。更没有人能预料到,它会以最残酷的方式——袭击尚未出生的孩子——展现自己最黑暗的一面。
从非洲雨林到太平洋岛屿的漫长蛰伏
寨卡病毒在被发现后的半个多世纪里,几乎如同隐身一般存在于热带地区的阴影之中。1952年,科学家们从同一片雨林中捕获的非洲伊蚊体内再次分离出这种病毒,确认了它的传播媒介。1954年,尼日利亚一名十岁女孩成为第一个有记录的人类感染者,她出现了黄疸症状,但同时也感染了疟疾,使得诊断变得复杂。在此后的六十年间,全世界记录在案的人类寨卡病毒感染病例不足二十例。
病毒在沉默中传播,却从未引起关注。血清学调查表明,寨卡病毒在非洲和亚洲的热带地区广泛流行,但大多数感染者要么毫无症状,要么只出现轻微的发烧、皮疹和关节疼痛——这些症状如此普通,以至于常被误诊为登革热或其他更常见的疾病。在很长一段时间里,寨卡病毒被医学界视为"最无聊的黄病毒"——它不会导致严重疾病,不会引起死亡,甚至不需要特别关注。
然而,病毒从未停止进化。它在非洲和亚洲的丛林中悄然传播,随着蚊子的叮咬在猴群和人群之间跳跃,不断积累基因突变。科学家们后来发现,寨卡病毒分化出了三个主要的谱系:非洲谱系、亚洲谱系和美洲谱系。正是这些看似微不足道的基因变化,为后来席卷全球的灾难埋下了伏笔。
2007年,西太平洋雅浦岛爆发了人类历史上第一次有记录的寨卡病毒疫情。这个仅有七千人口的偏远小岛上,约五千人被感染,占全岛人口的四分之三。大多数人出现了皮疹、结膜炎和关节痛等症状,但所有病例都呈自限性,没有出现严重并发症或死亡。这场疫情像是一个警告,却被世界卫生组织和其他公共卫生机构完全忽视了。
2013年10月,法属波利尼西亚迎来了更大规模的爆发。超过三万人感染,约占当地人口的十分之一。这一次,事情开始变得不对劲。疫情高峰期间,当地报告了42例吉兰-巴雷综合征——一种自身免疫性疾病,会导致肌肉无力、瘫痪,严重时甚至需要呼吸机维持生命。这个数字是正常发病率的二十倍。更令人不安的是,医生们开始注意到一些孕妇生下的婴儿头部异常小。当时,没有人把这些症状与寨卡病毒联系起来。
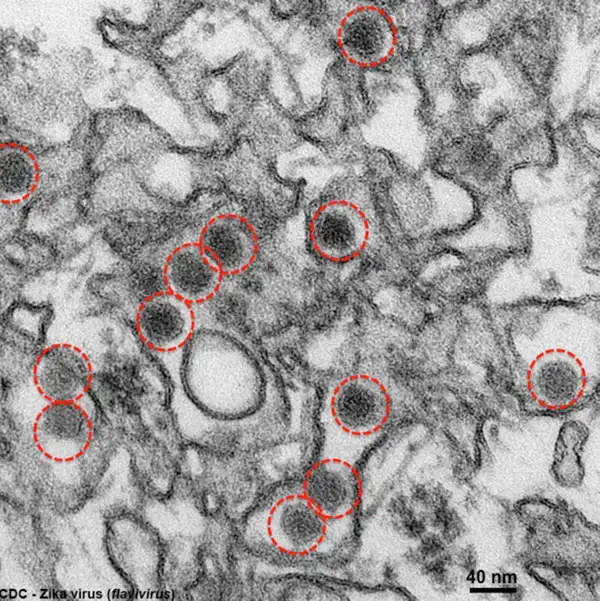
寨卡病毒颗粒在电子显微镜下的真容。这些直径约40纳米的球形颗粒,拥有外层包膜和内部致密核心。正是这些看似无害的微小颗粒,却能让未出生婴儿的大脑永远停止发育。图片来源:CDC公共卫生图像库
巴西的噩梦:当真相浮出水面
2015年3月,巴西东北部开始出现一种奇怪的疾病。患者们出现皮疹、低烧、结膜炎和关节痛——症状与登革热相似,却又有所不同。当地医生最初以为这是一种新的登革热变种,直到5月,巴西卫生部门确认了寨卡病毒在美洲的首次传播。
起初,这似乎只是一场普通的蚊媒疾病疫情。巴西正在为一年后的奥运会做准备,人们对寨卡病毒的关注仅限于它可能影响游客的健康。直到2015年8月,伯南布哥州的儿科医生们开始注意到一个令人不安的趋势:新生儿中出现的严重小头症病例数量急剧增加。
阿德里安娜·范德林登是伯南布哥州公立医院的一名儿科神经科医生。8月的一天,她接诊了一个刚出生的女婴,孩子的头围只有29厘米,远低于正常新生儿的下限33厘米。更奇怪的是,孩子的头部形状异常,前额几乎完全缺失。在随后的几周内,范德林登医生接诊了越来越多类似的病例。她开始意识到,这不是一个偶然现象。
“以前我们可能一年见到一两例小头症,“范德林登后来回忆道,“但突然之间,我们每天都能看到两三个这样的婴儿。这太不正常了。”
范德林登医生和她的同事们开始调查这些病例的共同点。他们发现,大多数小头症婴儿的母亲在怀孕期间都曾出现皮疹和发烧等症状——这与寨卡病毒感染的典型症状高度吻合。一个可怕的可能性开始浮出水面:寨卡病毒可能正在攻击胎儿的大脑。
2015年11月11日,巴西卫生部宣布进入公共卫生紧急状态。一个月后,一个来自斯洛文尼亚的病例提供了决定性的证据。一名曾在巴西东北部生活的孕妇在怀孕28周时因胎儿异常而终止妊娠。尸检发现,胎儿的大脑严重萎缩,几乎只剩下正常大小的三分之一。更重要的是,科学家们从胎儿的大脑中完整地提取出了寨卡病毒的基因组——这是寨卡病毒能够通过胎盘感染胎儿并导致大脑损伤的确凿证据。
2016年2月1日,世界卫生组织宣布寨卡病毒疫情为"国际关注的公共卫生紧急事件”。从非洲雨林中的一只猴子,到全球公共卫生危机,寨卡病毒用了近七十年时间完成了它的蜕变。
分子级的战争:病毒如何摧毁一个正在发育的大脑
寨卡病毒为何能够如此精准地攻击胎儿的大脑?这个问题的答案,隐藏在病毒与神经细胞之间一场惊心动魄的分子战争中。
寨卡病毒属于黄病毒家族,与登革病毒、西尼罗病毒和黄热病病毒是近亲。它的基因组是一条单链RNA,约含有10,800个核苷酸,编码三种结构蛋白和七种非结构蛋白。病毒颗粒呈球形,直径约40至50纳米,表面覆盖着由包膜蛋白形成的棘突。正是这些棘突,像钥匙一样打开了人类细胞的大门。
研究发现,寨卡病毒进入细胞的主要受体之一是AXL受体酪氨酸激酶。这种蛋白质在胚胎神经祖细胞中高度表达,它本应参与正常的细胞生长和分化过程。然而,寨卡病毒"劫持"了这个受体,通过它进入细胞内部。一旦进入,病毒就开始疯狂复制,将细胞变成自己的生产工厂。
但寨卡病毒对神经祖细胞的破坏远不止于简单的感染。科学家们发现,病毒感染会激活细胞内的TLR3受体——一种先天免疫系统的关键组分。TLR3的激活引发了一系列连锁反应,最终导致细胞周期停滞和程序性细胞死亡。更可怕的是,寨卡病毒还会诱导线粒体功能障碍,使细胞失去能量来源。在感染的神经祖细胞中,科学家们观察到染色质异常、中心体错误定位和有丝分裂失败——这些损伤会永远改变大脑的发育轨迹。

实验室里的研究人员正在分析寨卡病毒样本。2016年,当寨卡病毒与小头症的关联被确认后,全球科学界迅速动员起来,争分夺秒地研究这种病毒的致病机制和开发疫苗。
寨卡病毒的另一个独特之处在于它能跨越胎盘屏障。大多数病毒无法通过母体血液进入胎儿体内,因为胎盘是一个高度选择性的过滤系统。但寨卡病毒进化出了突破这一防线的能力。研究发现,寨卡病毒能够感染胎盘中的滋养层细胞和霍夫鲍尔细胞(胎盘巨噬细胞),引发炎症反应和细胞凋亡,从而破坏胎盘屏障的完整性。
一旦寨卡病毒进入胎儿体内,它便展现出对发育中大脑的惊人"偏好”。在胎儿大脑中,神经祖细胞是负责产生所有神经元和胶质细胞的"种子细胞"。寨卡病毒感染这些细胞后,会造成两种毁灭性的后果:一是直接杀死正在分裂的神经祖细胞,二是干扰它们的正常分化过程。结果就是大脑无法产生足够的神经元,颅骨也随之停止生长。
2016年,一组科学家利用人类干细胞培养的大脑类器官模型揭示了寨卡病毒的破坏力。这些类器官在感染寨卡病毒后,体积缩小了近40%,神经祖细胞层明显变薄,细胞凋亡率大幅增加。更令人震惊的是,科学家们发现寨卡病毒感染会导致与微头症相关的多个基因表达下调——这解释了为什么感染寨卡病毒的胎儿会出现与遗传性微头症相似的症状。
科学家们还发现了一个令人不安的事实:寨卡病毒可能通过劫持一种名为ANKLE2的宿主蛋白来支持自身复制。ANKLE2在大脑发育中扮演着重要角色,它的突变与遗传性微头症有关。寨卡病毒似乎"借用"了这个对大脑发育至关重要的蛋白来服务自己的繁殖目的,在这个过程中彻底摧毁了它本应帮助构建的大脑。
吉兰-巴雷综合征:成年人也未能幸免
寨卡病毒对胎儿的伤害最为触目惊心,但它对成年人的威胁同样不容忽视。2013年法属波利尼西亚疫情期间,医生们首次注意到寨卡病毒感染与吉兰-巴雷综合征之间的关联。吉兰-巴雷综合征是一种罕见的自身免疫性疾病,患者的免疫系统会错误地攻击自己的周围神经系统,导致肌肉无力、感觉异常,严重者可能出现呼吸肌麻痹,危及生命。
在法属波利尼西亚疫情中,42名患者被诊断为吉兰-巴雷综合征,其中93%的患者寨卡病毒抗体检测呈阳性。研究人员估计,寨卡病毒感染后发生吉兰-巴雷综合征的风险约为正常人群的二十倍。更令人担忧的是,寨卡病毒相关的吉兰-巴雷综合征往往进展更快,症状更严重,需要重症监护的比例更高。
科学家们认为,寨卡病毒感染后,病毒蛋白与人体的神经组织蛋白之间存在"分子模拟"现象——它们的某些结构相似到足以欺骗免疫系统。当免疫系统产生针对病毒蛋白的抗体时,这些抗体也会攻击神经组织,导致脱髓鞘和神经传导障碍。这是一种典型的"无辜旁观者"效应:免疫系统在追杀病毒的同时,误伤了无辜的神经细胞。
2015年巴西疫情爆发后,吉兰-巴雷综合征的病例数量同样出现了激增。巴西卫生部门报告的病例数是往年的数倍。在其他寨卡病毒流行的国家,如哥伦比亚、委内瑞拉和萨尔瓦多,也观察到了类似的趋势。这进一步证实了寨卡病毒与神经系统并发症之间的因果关系。
除了吉兰-巴雷综合征,寨卡病毒感染还与脑炎、脊髓炎和脑膜炎等神经系统疾病有关。虽然这些并发症在感染者中的比例不高,但考虑到寨卡病毒在流行地区的高感染率,受影响的总人数仍然相当可观。
传播之谜:一只蚊子的全球旅行
寨卡病毒能够在短短几年内从南太平洋蔓延到美洲大陆,主要归功于它的主要传播媒介——埃及伊蚊。这种黑白条纹相间的蚊子是人类历史上最成功的疾病传播者之一,它同时也是登革热、黄热病和基孔肯雅热的传播者。
埃及伊蚊原产于非洲,但随着大西洋奴隶贸易和全球航运的发展,它在过去几百年间成功殖民了全世界的热带和亚热带地区。这种蚊子偏爱人类居住的环境,喜欢在人工容器(如花盆、轮胎、水桶)中繁殖,以人类血液为主要食物来源。一只雌性埃及伊蚊在一次吸血后可以产下数百枚卵,这些卵在干燥条件下可以存活数月,一旦遇到水就会孵化。
埃及伊蚊的叮咬行为使它成为极其高效的疾病传播者。它通常在白天活动,喜欢在清晨和黄昏时分吸血。与普通蚊子不同,埃及伊蚊的叮咬往往不被人察觉——它的唾液中含有麻醉成分,叮咬时几乎不引起疼痛。一只受感染的蚊子可以在整个生命周期内传播病毒,而病毒还可以通过卵传给下一代,形成持续的传播循环。

蚊子,人类历史上最致命的动物。埃及伊蚊是寨卡病毒的主要传播媒介,同时也是登革热、黄热病和基孔肯雅热的传播者。这种蚊子偏爱人类居住的环境,在人工容器中繁殖,以人类血液为主要食物来源。
寨卡病毒从南太平洋传入美洲的确切路径至今仍是一个谜。科学家们通过基因测序分析发现,2015年巴西流行的寨卡病毒与法属波利尼西亚的病毒株高度相似,表明病毒可能是从南太平洋传入的。一种理论认为,病毒可能是通过2013年国际足联联合会杯、2014年世界杯足球赛或2014年瓦卡世界划船锦标赛等大型体育赛事带入巴西的。另一种可能性是,病毒通过单独的旅行者传入,然后在巴西东北部的条件下获得了爆发性传播的机会。
巴西东北部成为寨卡病毒疫情的震中并非偶然。这个地区拥有埃及伊蚊繁殖的理想条件:热带气候、大量积水、城市化程度高但卫生设施落后。更重要的是,当地居民对寨卡病毒缺乏免疫力,形成了病毒快速传播的"干柴烈火"局面。科学家们估计,2015年至2016年间,巴西可能有超过150万人感染了寨卡病毒。
值得注意的是,寨卡病毒还可以通过性接触传播。2011年,一名美国科学家在从塞内加尔返回后,将寨卡病毒传染给了他的妻子,这成为第一例记录在案的寨卡病毒性传播病例。此后,多国报告了类似的传播事件。研究发现,寨卡病毒可以在精液中存活数周甚至数月,这使得性传播成为寨卡病毒扩散的一个次要但重要的途径。
受害者的声音:那些被遗忘的孩子和母亲
数字可以告诉我们疫情的规模,却无法传达个体的痛苦。截至2016年底,巴西确认了超过2600例与寨卡病毒相关的先天性综合征病例,另有超过3200例疑似病例仍在调查中。这些数字背后,是数千个家庭永远被改变的人生。
鲁特·弗雷雷斯是巴西东北部阿拉戈斯州的一位母亲。2015年,她在怀孕期间感染了寨卡病毒。当时,她对这种疾病几乎一无所知——它看起来只是一场轻微的发烧和皮疹,几天后就自行消退了。直到女儿塔玛拉出生,她才意识到发生了什么。
塔玛拉出生时头围严重偏小,被诊断为先天性寨卡综合征。医生告诉鲁特,她的女儿可能永远无法行走、说话甚至微笑。九年过去了,医生们的预言大部分成真了。塔玛拉通过胃管进食,双手越来越僵硬和挛缩,头部难以保持稳定。她需要全天候的照顾,无法独立完成任何日常活动。
“很早以前我就被告知,她不会走路,不会说话,也不会笑,“鲁特说,“但我仍然会问每一个我见到的医生:‘我的孩子会走路的,对吗?’”
像鲁特这样的母亲并不是孤例。在寨卡病毒疫情最严重的时期,巴西东北部出现了数以千计的小头症婴儿。许多父亲在得知孩子的诊断后选择了离开,留下母亲独自承担起照顾特殊需要儿童的重担。这些母亲中,大多数人不得不辞去工作,依靠微薄的政府救济金生活。
为了相互支持,一些母亲组织起来,成立了互助团体。她们分享信息、交换照顾技巧,更重要的是,在彼此最黑暗的时刻提供情感支持。在阿拉戈斯州,十多位母亲申请到了同一栋公共住房,她们已经一起生活了五年。她们的孩子们有的可以通过胃管进食,有的完全无法活动,只有极少数能够行走和说话。
安妮·卡罗琳·达·席尔瓦·罗莎是这些母亲中的一员。她的儿子莫伊塞斯同样患有先天性寨卡综合征。“我们开始互相交谈,交换信息……事情终于开始变得有意义了,“她说。当鲁特决定重返夜校完成高中学业时,安妮·卡罗琳和其他邻居帮忙照顾塔玛拉,让她得以实现自己的梦想。
这些孩子们的未来充满了不确定性。先天性寨卡综合征不仅仅意味着小头症,它还包括心脏问题、关节异常、协调障碍、视力和听力损伤等一系列并发症。大多数孩子无法达到传统的发展里程碑——他们不会爬行、走路、说话或进行如厕训练。随着年龄增长,他们的健康状况可能会进一步恶化。
更令人担忧的是,对这些孩子的长期研究仍然严重不足。十年过去了,科学家们仍然不知道这些孩子的预期寿命、成年后的生活质量,以及寨卡病毒感染对他们的长期影响。在这个意义上,这些孩子和他们的母亲成为了一场持续进行的医学实验的对象——而没有人能告诉他们实验的结果会是什么。

寨卡病毒疫情留给人类的,不仅仅是那些被永久改变生命的儿童和家庭,还有一系列关于全球公共卫生体系的深刻教训。这些特殊需要儿童需要终身护理,而他们的家庭往往缺乏足够的支持。
科学界的紧急动员
2016年初,当寨卡病毒与小头症之间的联系被确认后,全球科学界迅速动员起来。美国疾病控制与预防中心发布了旅行警告,建议孕妇避免前往寨卡病毒流行地区。一些国家甚至建议女性推迟怀孕计划——萨尔瓦多的建议是等到2018年。
实验室里,科学家们争分夺秒地工作。2016年3月,普渡大学的研究团队发表了寨卡病毒的3D结构,分辨率达到3.8埃。这是当时人类获得的任何包膜病毒的最高分辨率图像。这一突破为开发疫苗和抗病毒药物铺平了道路,因为它揭示了病毒表面可能的药物结合位点。
研究人员还开发了多种动物模型来研究寨卡病毒的致病机制。小鼠模型显示,寨卡病毒感染怀孕母鼠后会导致胎儿大脑损伤,复制了人类先天性寨卡综合征的关键特征。非人灵长类动物模型则提供了更接近人类的感染过程数据。
疫苗研发也在紧急推进。截至2025年,已有多种寨卡病毒疫苗进入临床试验阶段,包括灭活疫苗、减毒活疫苗、DNA疫苗、mRNA疫苗和病毒载体疫苗。其中,Moderna公司的mRNA-1893疫苗已成功完成一期临床试验,显示出良好的安全性和免疫原性。然而,由于寨卡病毒疫情在2017年后迅速消退,大规模三期临床试验变得困难,迄今仍无寨卡病毒疫苗获得最终批准。
科学家们还在探索寨卡病毒的另一个潜在用途:治疗一种致命的脑癌——胶质母细胞瘤。由于寨卡病毒对神经祖细胞的特异性杀伤能力,研究人员正在改造它,使其能够靶向杀死胶质母细胞瘤细胞,同时保留正常脑细胞。这种"以毒攻毒"的策略已在小鼠模型中显示出初步疗效,为这种致命疾病的治疗带来了新的希望。
疫情为何突然消失?
2017年初,寨卡病毒疫情像它出现时一样突然地消退了。2016年巴西报告了超过20万例寨卡病毒疑似病例,而2017年这个数字下降到不足1.8万例。到2018年,巴西全年报告的病例数仅为几千例。这种戏剧性的下降让科学家们困惑不已。
一种理论认为,寨卡病毒感染后产生的免疫力在人群中形成了群体免疫屏障。在疫情高峰期,可能有超过三分之二的巴西人口感染了寨卡病毒,获得了至少暂时的免疫力。当易感人群的数量下降到一定程度时,病毒的传播链就被打断了。
另一种可能性是,寨卡病毒与登革病毒之间的交叉反应发挥了作用。巴西是登革热的高流行区,许多居民曾感染过登革病毒。研究发现,某些登革病毒抗体可以与寨卡病毒交叉反应,虽然这种反应有时会增强寨卡病毒感染(一种称为抗体依赖性增强的现象),但在某些情况下也可能提供保护。
还有一种理论认为,寨卡病毒可能因为某种未知的环境因素而失去了传播优势。科学家们发现,巴西东北部疫情最严重的地区恰好是干旱地区,居民们依赖储水容器生活,为埃及伊蚊提供了理想的繁殖场所。当这些地区的供水条件改善后,蚊虫密度可能下降,病毒的传播也因此减少。
然而,最令人担忧的是,寨卡病毒可能从未真正消失。由于大多数感染者无症状或症状轻微,病例报告系统可能严重低估了实际的传播水平。寨卡病毒可能正在以低水平持续传播,等待着下一次爆发的机会。科学家们警告说,只要埃及伊蚊仍然存在,只要人类对寨卡病毒的免疫力开始消退,新的疫情就可能卷土重来。
被忽视的教训
寨卡病毒疫情留给人类的,不仅仅是那些被永久改变生命的儿童和家庭,还有一系列关于全球公共卫生体系的深刻教训。
首先,寨卡病毒疫情揭示了疾病监测系统的巨大漏洞。寨卡病毒在非洲和亚洲流行了七十多年,却从未引起足够的关注。当它最终在美洲爆发时,公共卫生机构几乎是被动地应对而非主动预防。如果早在雅浦岛或法属波利尼西亚疫情期间就能识别出寨卡病毒的神经毒性,巴西的悲剧或许可以避免。
其次,寨卡病毒疫情暴露了科研资源分配的不平等。寨卡病毒长期以来被忽视,部分原因是它主要影响发展中国家。当寨卡病毒威胁到发达国家时,科研经费和研究兴趣才迅速涌入。这种"富国优先"的研究模式意味着许多可能威胁全球健康的疾病被长期忽视。
第三,寨卡病毒疫情凸显了公共卫生沟通的挑战。在疫情初期,关于寨卡病毒与小头症关联的信息混乱不堪,一些政府甚至建议女性完全避免怀孕——这对一个以天主教为主的国家来说是一个敏感而困难的决定。如何在不引起恐慌的情况下传达风险信息,仍然是公共卫生领域的一大挑战。
最后,寨卡病毒疫情提醒我们,新发传染病的威胁从未消失。在过去的几十年里,人类经历了艾滋病、SARS、H1N1流感、埃博拉、寨卡、MERS和COVID-19等一系列新发传染病的冲击。每一次疫情都是一个警告,提醒我们与微生物世界的战争从未结束。
今天,那些因寨卡病毒而出生的孩子们正在成长。他们中的大多数永远无法独立生活,永远无法理解这个世界为何对他们如此残酷。而寨卡病毒,这个从非洲雨林中走出来的隐形杀手,仍然在某个地方潜伏着,等待着下一次机会。
对于人类来说,寨卡病毒的故事是一个残酷的提醒:我们对微生物世界的了解仍然太过肤浅。一个被忽视近七十年的"温和"病毒,可以在一夜之间变成吞噬未出生孩子未来的恶魔。在病毒与人类的永恒战争中,谦卑和警惕,或许是我们最需要的品质。

实验室培养皿中的细胞。寨卡病毒疫情提醒我们,新发传染病的威胁从未消失。每一次疫情都是一个警告,提醒我们与微生物世界的战争从未结束。谦卑和警惕,或许是人类面对病毒时最需要的品质。
参考资料
-
Dick GW, Kitchen SF, Haddow AJ. Zika virus. I. Isolations and serological specificity. Trans R Soc Trop Med Hyg. 1952;46(5):509-520.
-
Musso D, Gubler DJ. Zika Virus. Clin Microbiol Rev. 2016;29(3):487-524.
-
Duffy MR, Chen TH, Hancock WT, et al. Zika virus outbreak on Yap Island, Federated States of Micronesia. N Engl J Med. 2009;360(24):2536-2543.
-
Cao-Lormeau VM, Blake A, Mons S, et al. Guillain-Barré Syndrome outbreak associated with Zika virus infection in French Polynesia: a case-control study. Lancet. 2016;387(10027):1531-1539.
-
Mlakar J, Korva M, Tul N, et al. Zika Virus Associated with Microcephaly. N Engl J Med. 2016;374(10):951-958.
-
Tang H, Hammack C, Ogden SC, et al. Zika Virus Infects Human Cortical Neural Progenitors and Attenuates Their Growth. Cell Stem Cell. 2016;18(5):587-590.
-
Wen Z, Song H, Ming GL. How does Zika virus cause microcephaly? Genes Dev. 2017;31(9):849-861.
-
Brasil P, Pereira JP Jr, Moreira ME, et al. Zika Virus Infection in Pregnant Women in Rio de Janeiro. N Engl J Med. 2016;375(24):2321-2334.
-
Sirohi D, Chen Z, Sun L, et al. The 3.8 Å resolution cryo-EM structure of Zika virus. Science. 2016;352(6284):467-470.
-
Faria NR, Quick J, Claro IM, et al. Establishment and cryptic transmission of Zika virus in Brazil and the Americas. Nature. 2017;546(7658):406-410.
-
Qian X, Nguyen HN, Song MM, et al. Brain-region-specific organoids using mini-bioreactors for modeling ZIKV exposure. Cell. 2016;165(5):1238-1254.
-
Cugola FR, Fernandes IR, Russo FB, et al. The Brazilian Zika virus strain causes birth defects in experimental models. Nature. 2016;534(7606):267-271.
-
Hamel R, Dejarnac O, Wichit S, et al. Biology of Zika Virus Infection in Human Skin Cells. J Virol. 2015;89(17):8880-8896.
-
Miner JJ, Cao B, Govero J, et al. Zika Virus Infection during Pregnancy in Mice Causes Placental Damage and Fetal Demise. Cell. 2016;165(5):1081-1091.
-
Heymann DL, Hodgson A, Sall AA, et al. Zika virus and microcephaly: why is this situation a PHEIC? Lancet. 2016;387(10020):719-721.