1975年的一个深秋午后,美国国立卫生研究院的血液病学家哈维·奥尔特盯着眼前的一组数据陷入了沉思。他刚刚完成了对输血后肝炎患者的血清学分析,结果却让他感到一阵寒意——那些患者感染的既不是甲型肝炎病毒,也不是刚刚被发现的乙型肝炎病毒。某种未知的病原体正在血液供应的阴影中悄然蔓延,而医学界对它一无所知。
奥尔特无法想象,他手中的这份报告将开启一场长达十四年的追寻。更无法预见,这场追寻最终会让三名科学家站在斯德哥尔摩的音乐厅里接受诺贝尔奖,而他们发现的病毒已经感染了全球超过七千一百万人,在几十年的时间里无声地吞噬着数以千万计的肝脏。这是一种被称为"沉默杀手"的病毒,它的故事是一部关于血腥、谎言、科学坚持与最终胜利的史诗。
血液中的幽灵
丙型肝炎病毒的故事要从更早的年代说起。1960年代,输血已经成为现代医学不可或缺的一部分,但每一次输血都像是一场赌博——当时还没有有效的筛查手段,接受输血的患者有高达百分之三十的风险患上输血后肝炎。那是一种令人恐惧的疾病:患者可能在输血后几周出现黄疸、乏力、恶心,严重者会发展为慢性肝病甚至死亡。
1972年,当巴鲁克·布隆伯格因发现乙型肝炎病毒而获得诺贝尔奖时,医学界以为输血后肝炎的谜团即将解开。通过筛查血液中的澳大利亚抗原——后来被证实是乙型肝炎病毒的表面蛋白——理论上可以将乙肝病毒从血库中清除。然而,现实给了医生们一记沉重的耳光。即使在实施了严格的乙肝病毒筛查之后,输血后肝炎的发病率仍然居高不下——居然还有百分之八十的病例无法用乙肝病毒解释。
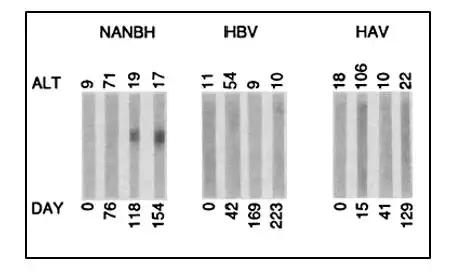
奥尔特当时正在美国国立卫生研究院的临床中心输血部门工作。他与同事们对一组输血后肝炎患者的血清进行了细致的分析,结果令人震惊:这些患者体内没有任何甲型肝炎病毒或乙型肝炎病毒感染的证据。奥尔特意识到,他们面对的是一种全新的病原体。1975年,他在《柳叶刀》杂志上发表论文,将这种神秘疾病命名为"非甲非乙型肝炎"。这个名字听起来像是一个临时标签,没有人想到它会持续使用整整十四年。
接下来的十年是医学史上最令人沮丧的时期之一。全球各地的实验室都在尝试分离这种神秘的病毒,但所有的努力都石沉大海。传统的病毒分离方法——细胞培养、动物接种、免疫电镜——统统失效。病毒似乎在故意嘲弄着人类的科技:它就存在于患者的血液中,却拒绝向人类展示真面目。
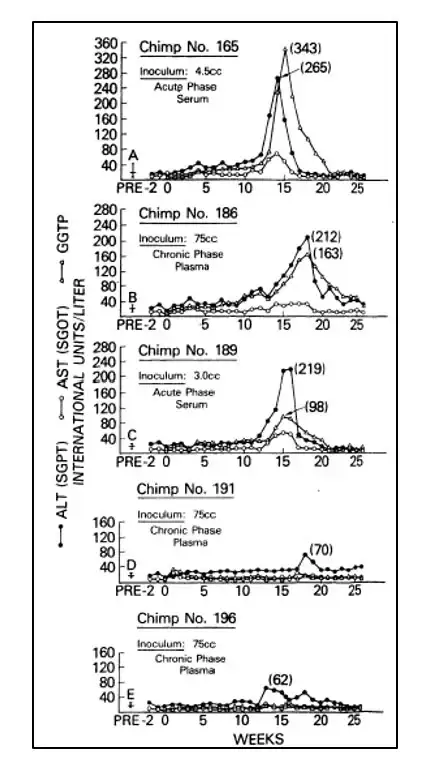
奥尔特和他的同事们至少取得了一个关键突破。他们发现,将非甲非乙型肝炎患者的血清注射给黑猩猩,可以成功地让这些与人类基因最接近的灵长类动物患上肝炎。这是人类第一次建立了一个可靠的动物模型,为后续的研究奠定了基础。通过这个模型,奥尔特还发现这种病原体对氯仿敏感——这意味着它是一种包膜病毒。他们还通过过滤实验估计了病毒的大小:直径在三十到六十纳米之间。
但这些信息仍然不足以鉴定病毒的身份。在基因测序技术尚不成熟的年代,科学家们只能在黑暗中摸索。而与此同时,非甲非乙型肝炎正在全球范围内悄然蔓延。在埃及,一场本意拯救生命的公共卫生运动正在为这个国家埋下一颗定时炸弹;在英国,数千名血友病患者正在接受一种被称为"革命性治疗"的凝血因子制剂,却不知道自己正在被注射进死亡的种子。
尼罗河畔的悲剧
埃及的悲剧是医学史上最令人心碎的公共卫生灾难之一。这个故事要从血吸虫病说起。血吸虫病是一种由寄生虫引起的慢性疾病,在二十世纪中叶的埃及,它是最严重的公共卫生问题之一。尼罗河流域的农民在灌溉渠道中劳作,寄生虫的幼虫穿透他们的皮肤,在肝脏和肠道中产卵,导致严重的器官损伤。
1918年,一位名叫约翰·克里斯托弗森的英国医生发现,注射酒石酸锑钾可以治愈血吸虫病。从那时起,注射治疗成为了埃及对抗血吸虫病的主要武器。1950年代,埃及卫生部在世界卫生组织的建议下,发起了一场声势浩大的全国性血吸虫病治疗运动。
这场运动的初衷是崇高的,但执行方式却埋下了灾难的种子。为了治疗数以百万计的患者,医疗队深入尼罗河三角洲和上埃及的每一个村庄,为当地居民进行静脉注射。问题是,注射器的消毒极其简陋——往往只是用热水简单冲洗后就给下一位患者使用。在长达三十年的时间里,超过三千六百万次注射被实施,每次注射都可能将前一位患者血液中的病原体传递给下一位。
当时没有人知道,这些注射器中潜伏着一种未知的病毒。它的传播是无声的,它的潜伏期长达数十年。急性感染往往没有明显症状,百分之八十的患者甚至不知道自己已经被感染。病毒就这样在不知不觉中传播开来,从一个人到另一个人,从一个村庄到另一个村庄。
直到1990年代,当埃及的流行病学家开始调查为什么这个国家的肝炎发病率异常之高时,真相才逐渐浮出水面。2000年发表在《柳叶刀》上的一项里程碑式研究揭示了惊人的数字:埃及人口中丙型肝炎病毒的感染率高达百分之十四点七——这是全球最高的。在尼罗河三角洲和上埃及的某些地区,感染率甚至高达百分之二十六到百分之二十八。据估计,有一千一百五十万埃及人携带这种病毒。
这个数字背后是一个令人窒息的真相:埃及政府在世界卫生组织的建议下发起的这场公共卫生运动,无意中创造了人类历史上最大规模的医源性感染。那些被注射治疗"拯救"的人们,在几十年后发现自己的肝脏正在被一种无法治愈的疾病慢慢吞噬。他们中的许多人将在生命的最后阶段发展成肝硬化或肝癌,而这个过程可能持续二十到四十年——从感染到症状出现,恰好是一代人的时间。
更讽刺的是,血吸虫病本身就会造成肝脏损伤。当血吸虫病患者同时感染丙型肝炎病毒时,两种疾病的协同效应会大大加速肝硬化的进程。一项长期研究显示,在同时感染两种病原体的患者中,百分之四十八发展成了肝硬化,而仅感染丙型肝炎病毒的患者中这一比例为百分之十五。这意味着,那场旨在拯救生命的运动,实际上将数百万人推向了更深的深渊。
血液丑闻的阴影
埃及并非唯一一个因医疗实践而遭受丙型肝炎病毒重创的国家。在大洋彼岸的英国,另一场悲剧正在上演,而它的受害者是另一群无辜的人——血友病患者。
血友病是一种遗传性凝血障碍,患者缺乏一种关键的凝血因子,即使是轻微的创伤也可能导致致命的出血。在1970年代之前,血友病患者的治疗方法十分有限,严重出血往往需要大量输血。然而,1970年代出现了一种革命性的新疗法——浓缩凝血因子制剂。这种从数千名献血者的血浆中提取的冻干粉末,让血友病患者第一次可以在家中自行注射,不必再为每一次小伤口担惊受怕。
这是一种被称为"革命"的进步,但它的代价是惨重的。
浓缩凝血因子的生产过程本身就是一个公共卫生噩梦。为了生产一批制剂,制造商需要将数千甚至数万名献血者的血浆混合在一起。这虽然大大提高了生产效率,但也意味着只要其中有一个献血者携带病原体,整批产品都会被污染。而当时,美国许多血浆采集站会向献血者支付报酬——这吸引了大量高风险人群,包括监狱囚犯和吸毒者。一份报告显示,某些批次的凝血因子制剂可能汇集了多达六万名献血者的血浆。
当英国在1970年代开始大量进口美国生产的凝血因子制剂时,没有人意识到其中潜藏的危险。1975年,世界卫生组织就已经通过决议,敦促所有国家实现血液制品的自给自足。英国的官员们心知肚明,国内生产的血液制品远远无法满足需求,而建设更多生产设施需要大量投资。于是,进口继续进行。
1983年的一项研究敲响了警钟:首次接受未处理的凝血因子制剂治疗的血友病患者,感染肝炎的风险是百分之百。但这份报告并没有阻止产品的使用。同样是在1983年,当英国传染病监测中心的主任斯彭斯·加尔布雷思写信警告政府应该暂停使用美国血液制品时,卫生部的回应是这种建议"为时过早"。
接下来的岁月里,悲剧不可避免地发生了。根据2024年公布的英国感染血液调查报告,大约有三万人因接受被污染的血液或血液制品而感染了丙型肝炎病毒和艾滋病毒。截至调查报告发布时,已有超过三千人死亡,而且死亡人数仍在持续增加——许多感染者在感染几十年后才发展成晚期肝病。
这是一个关于贪婪、疏忽和系统性失败的复杂故事。血液制品公司在明知风险的情况下继续销售产品;政府在明知危险的情况下继续进口产品;医生在明知可能感染患者的情况下继续使用产品。整个系统像是被某种不可见的惯性驱动着,即使警告信号一个接一个地亮起,也没有人愿意按下停止键。
而对于那些血友病患者来说,他们不仅要承受血友病本身带来的痛苦,还要面对另一种更加可怕的疾病——以及来自社会的歧视和羞辱。许多人将感染归咎于他们"生活方式不检点",而事实是,他们只是信任了医生和政府。
黑暗中的曙光
在患者们承受着病痛的同时,科学家们仍在孜孜不倦地寻找那个神秘的病毒。1982年,一位名叫迈克尔·霍顿的英国病毒学家加入了加州一家名为凯龙的生物技术公司,开始了他的追寻之旅。
霍顿深知传统方法的局限性。既然病毒无法在细胞培养中生长,无法通过免疫电镜观察到,也无法用常规的免疫学方法检测,那就需要一种全新的思路。他决定采用分子克隆的方法,试图从感染黑猩猩的血浆中直接钓出病毒的基因序列。
这是一个大胆的计划,但进展极其缓慢。霍顿和他的团队构建了一个来自感染黑猩猩血浆的互补DNA文库,然后用各种方法试图筛选出病毒序列。然而,他们找到的几乎全是宿主本身的基因——人类和黑猩猩的DNA充斥着样本,而病毒序列就像大海捞针一样难以寻觅。
转机出现在他们决定采用一种新的免疫筛选策略时。霍顿与同事邱立林、乔治·郭合作,将感染血浆的cDNA文库导入细菌中,然后用一位非甲非乙型肝炎患者的血清来探测——这位患者的血清中应该含有针对未知病毒的抗体。他们筛选了一百万个细菌菌落,终于发现了那根珍贵的针——一个不包含黑猩猩或人类DNA序列的克隆。
这个被命名为5-1-1的克隆序列,最终被证实来自一种全新的RNA病毒。它的基因组约有一万个核苷酸,编码一个巨大的开放阅读框,与已知的黄病毒科成员有远缘关系。霍顿将这种新病毒命名为丙型肝炎病毒(HCV)。1989年,这一发现发表在《科学》杂志上,标志着人类第一次看到了这个隐藏了数十年的敌人。
但故事的最后一块拼图还缺失着。霍顿的工作建立了HCV感染与非甲非乙型肝炎之间的关联,但严格来说,这并不构成因果关系的证明。要证明一种病原体确实是某种疾病的原因,需要满足著名的科赫法则——其中最关键的一条是:纯化的病原体必须能够导致同样的疾病。
这个任务落到了查尔斯·赖斯肩上。赖斯当时在华盛顿大学圣路易斯分校工作,他注意到HCV基因组3’末端有一个高度保守的非编码区,可能与病毒的复制密切相关。他构建了包含这个保守区域的病毒RNA基因组,注射到黑猩猩的肝脏中。第一次实验失败了——没有产生新的病毒。
赖斯意识到问题所在。RNA病毒的复制是高度易错的,许多病毒基因组携带着致命的突变。他重新设计了实验:根据已有的病毒序列信息,构建了一个"共识序列"——理论上最接近原始野生型病毒的基因组。他消除了可能存在的失活突变,然后再次将RNA注射到黑猩猩体内。
这一次,奇迹发生了。黑猩猩血液中出现了可检测到的病毒复制,它们发展出了肝炎的临床特征,并且病毒可以在体内持续存在数月。赖斯的工作提供了最终的证据:HCV单独就足以导致肝炎,而且可以长期潜伏。1997年,这一突破性发现发表在《科学》杂志上,为非甲非乙型肝炎的谜团画上了句号。
病毒的真面目
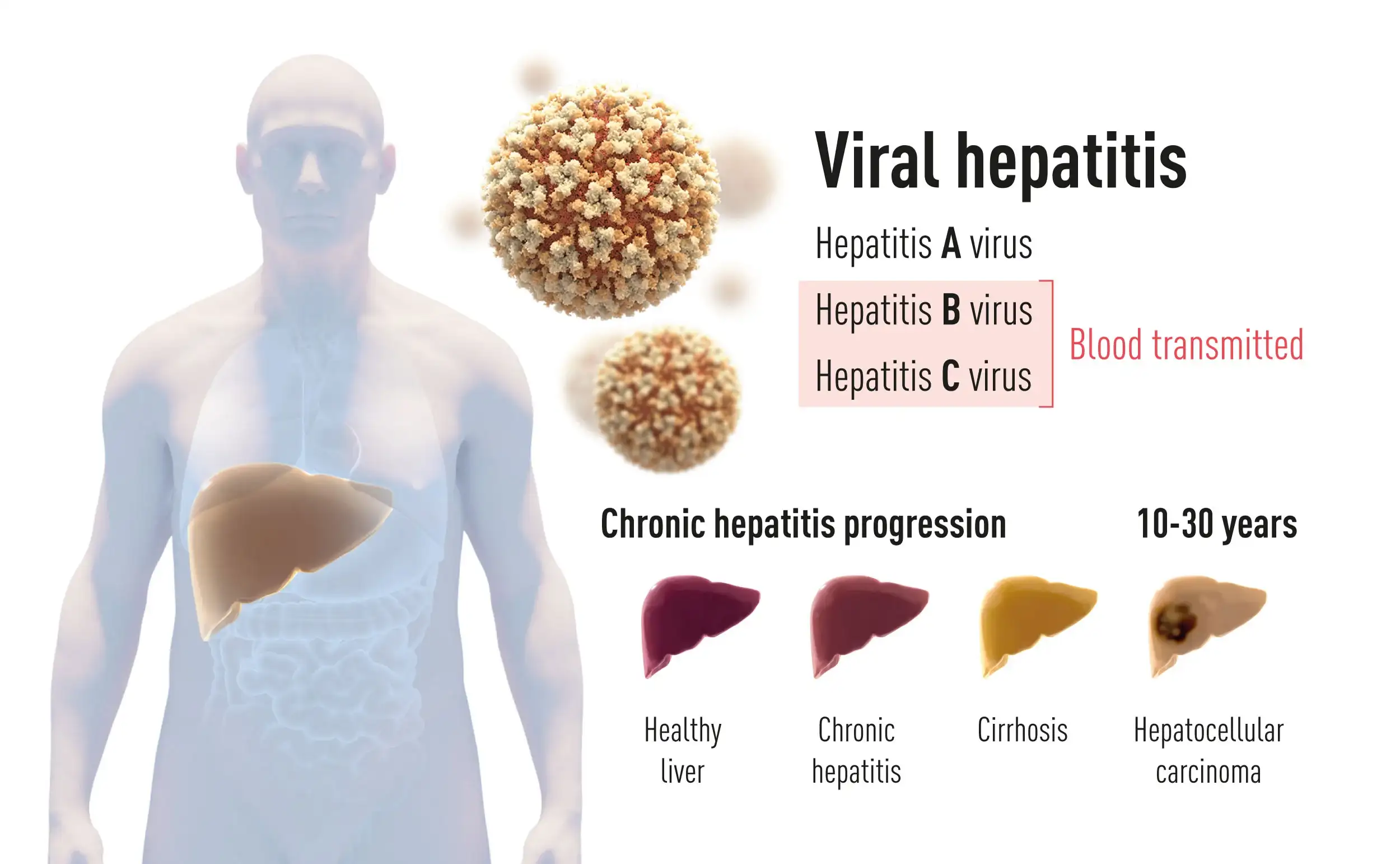
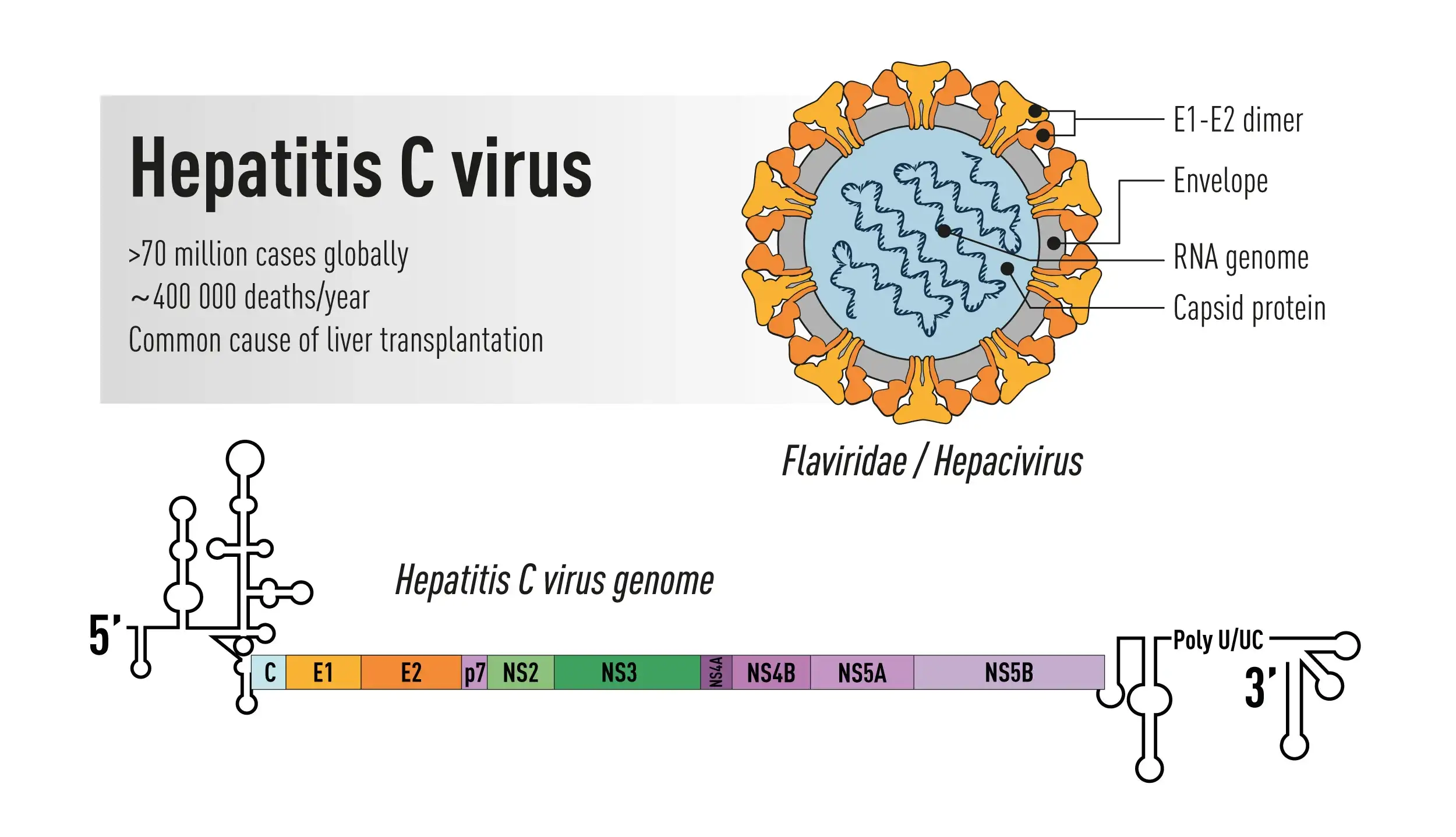
丙型肝炎病毒是一种极其狡猾的病原体。它是一种包膜的正链RNA病毒,属于黄病毒科,与登革病毒、西尼罗病毒和寨卡病毒是远亲。病毒颗粒直径约五十纳米,表面镶嵌着两种糖蛋白E1和E2,它们负责与宿主细胞表面受体结合,启动感染过程。
病毒的基因组编码一个多聚蛋白,被切割成十种不同的蛋白质。其中三种是结构蛋白:核心蛋白形成病毒的核衣壳,包裹着RNA基因组;E1和E2糖蛋白构成病毒的包膜。其余七种是非结构蛋白,包括NS3解旋酶/蛋白酶、NS5B RNA依赖性RNA聚合酶等,它们负责病毒基因组的复制。
HCV的复制策略堪称精妙。当病毒进入肝细胞后,它的RNA基因组被直接翻译成一个多聚蛋白前体。这个前体被病毒和宿主的蛋白酶切割成各个功能蛋白。然后,病毒在宿主细胞的内质网上构建一个特殊的"膜网"结构——这是一个由双膜囊泡组成的复制工厂,病毒RNA就在这里被大量复制。
每天,一个感染者体内可以产生多达一万亿个新的病毒颗粒。这种疯狂的复制速度是HCV逃避免疫系统的关键策略之一。RNA病毒的复制酶本身就没有校对功能,每复制一个基因组就会引入约一个错误。这意味着,在任何一个感染者体内,HCV都以"准种"的形式存在——一大群基因序列略有不同的病毒变异体。
当宿主的免疫系统产生针对某种病毒变异体的抗体时,另一种变异体可能已经悄然占据优势。这就像是一场永恒的军备竞赛:免疫系统刚追上一步,病毒就已经变换了伪装。这也解释了为什么约百分之七十的急性HCV感染会转为慢性——免疫系统最终在这场竞赛中败下阵来。
HCV还有一个独特的本领:它可以直接抑制宿主的先天免疫反应。病毒的NS3/4A蛋白酶可以切割宿主细胞中两种关键的信号分子MAVS和TRIF,从而阻断干扰素的产生。干扰素是机体对抗病毒感染的第一道防线,当这道防线被突破后,病毒就可以在肝细胞中肆无忌惮地复制。
在分子水平上,HCV造成的肝脏损伤是多因素的。病毒蛋白可以直接诱导肝细胞凋亡;持续的炎症反应会导致肝星状细胞活化,产生大量胶原蛋白,引起纤维化;慢性炎症还创造了促癌微环境,增加了肝细胞癌变的风险。从感染到肝硬化,平均需要二十年;从感染到肝癌,可能需要三十年或更长。这就是为什么HCV感染被称为"沉默的杀手"——在最初的几十年里,患者往往没有任何症状,而肝脏正在被一点点掏空。
干扰素的黑暗时代
在HCV被发现后的二十多年里,治疗这种疾病是一种折磨。医生们手中唯一的武器是干扰素——一种人体自然产生的抗病毒蛋白,最初发现于1957年,因其能够"干扰"病毒复制而得名。
干扰素治疗的原理很简单:注射外源性的干扰素,刺激细胞产生一系列抗病毒蛋白,增强免疫系统对HCV的攻击。早期的研究显示,干扰素确实可以降低部分患者体内的病毒载量,甚至实现病毒的清除。但代价是巨大的。
每周三次的皮下注射,持续六个月到一年。每一次注射都可能带来流感样症状:发热、寒战、肌肉酸痛、极度疲劳。许多患者形容治疗过程比疾病本身更加痛苦。更可怕的是精神副作用:干扰素可以导致严重的抑郁症,有患者在接受治疗期间出现了自杀念头。脱发、体重下降、甲状腺功能障碍、视网膜病变——副作用清单长得令人窒息。
即便患者咬牙坚持完成了治疗,成功率也令人失望。对于最常见的基因一型HCV,标准干扰素联合利巴韦林治疗的成功率仅有百分之四十五到七十。这意味着超过一半的患者在经历了数月的折磨后,病毒仍然顽固地存在于他们的血液中。
利巴韦林是一种核苷类似物,可以抑制多种RNA病毒的复制,但它本身对HCV的作用有限。联合使用的主要目的是提高干扰素的疗效,但它也带来了自己的问题——溶血性贫血是利巴韦林最常见且最严重的副作用,可能迫使治疗中断。
2000年代初期,聚乙二醇化干扰素的出现带来了些许改善。通过将干扰素分子与聚乙二醇链连接,药物在体内的半衰期大大延长,患者只需要每周注射一次,而不是三次。副作用略有减轻,疗效也有所提高。但对于基因一型感染,治愈率仍然只有百分之五十左右。
更令人绝望的是,即便治疗成功,也不意味着一切都结束了。那些发展成晚期肝病的患者,即使清除了病毒,仍然面临着肝功能衰竭和肝癌的风险。对于已经肝硬化的患者,治疗成功率更低,副作用更严重。
干扰素时代是HCV治疗史上的至暗时刻。患者和医生都在黑暗中摸索,明知前路艰难却别无选择。一些人选择放弃治疗,宁愿在沉默中等待疾病的进展;另一些人则用自己的身体承受着治疗的痛苦,只为换取一线生机。
药物革命的黎明
转折点出现在2013年。那一年,美国食品药品监督管理局批准了一种名为索非布韦的药物。这是一种核苷酸类似物,直接靶向HCV的NS5B RNA聚合酶——病毒复制机器的核心部件。与干扰素那种粗糙的"加强免疫系统"策略不同,索非布韦以精确的外科手术般的精准度,阻断了病毒复制的关键步骤。
临床试验的结果令人难以置信。对于基因二型和三型HCV感染,索非布韦联合利巴韦林治疗十二周,治愈率高达百分之九十以上——这在干扰素时代是不可想象的数字。更重要的是,许多患者完全不需要使用干扰素。对于那些在干扰素时代受尽折磨的患者来说,这简直是奇迹。
但这仅仅是开始。科学家们很快发现,同时靶向HCV复制过程中的多个关键蛋白,可以进一步提高治愈率并缩短疗程。2014年,一种名为哈沃尼的组合药物获得批准,它将索非布韦与另一种直接抗病毒药物雷迪帕韦结合在一起。雷迪帕韦靶向NS5A蛋白——一种对病毒复制和组装都至关重要的调节蛋白。
哈沃尼的临床试验数据震惊了医学界。对于基因一型HCV感染——曾经最难治疗的类型——单纯口服哈沃尼八到十二周,治愈率超过百分之九十五。患者每天只需要服用一片药,不需要注射,不需要忍受干扰素那种令人崩溃的副作用。许多患者在治疗过程中甚至感觉不到任何不适。
这一突破开启了直接抗病毒药物(DAA)的黄金时代。在随后的几年里,一系列DAA药物相继问世,它们靶向HCV生命周期中的不同环节:NS3/4A蛋白酶抑制剂阻断病毒多聚蛋白的切割;NS5A抑制剂干扰病毒复制复合物的组装;NS5B聚合酶抑制剂阻断RNA链的延伸。
当这些药物联合使用时,病毒几乎没有逃脱的机会。即使病毒在复制过程中产生变异,它也很难同时逃逸针对多个靶点的药物的攻击。这就像是一场不对称战争:HCV曾经依靠快速变异逃避免疫系统的追捕,但现在它面对的是精确制导的导弹群。
到2010年代末期,几乎所有的HCV基因型都可以通过口服药物治愈。治疗周期从最初的四十八周缩短到八周甚至更短。治愈率普遍超过百分之九十五,对于某些患者群体甚至接近百分之百。更神奇的是,DAA药物对晚期肝病患者仍然有效——那些曾经被认为"无药可救"的患者,现在也有了重获新生的希望。
诺贝尔奖的荣耀
2020年10月5日,诺贝尔委员会宣布将该年度的生理学或医学奖授予哈维·奥尔特、迈克尔·霍顿和查尔斯·赖斯,以表彰他们发现丙型肝炎病毒的开创性贡献。
这是一个迟到了三十年的荣誉。奥尔特从1970年代就开始研究输血后肝炎,他的工作奠定了"非甲非乙型肝炎"的概念基础;霍顿在1989年首次克隆出HCV的基因组,让病毒暴露在科学的聚光灯下;赖斯在1997年完成了最后的拼图,证明HCV确实是肝炎的病原体。三个人的工作接力传递,最终实现了医学史上最重要的发现之一。
诺贝尔奖委员会在公告中写道:“由于他们的发现,现在可以对病毒进行高度敏感的血液检测,这几乎消除了世界许多地区输血传播肝炎的风险。他们的发现还使得可以开发出抗病毒药物,治愈这种疾病。这是历史上第一次,一种慢性病毒感染现在可以被治愈。”
“可以被治愈”——这四个字背后是无数人的努力和牺牲。从那些在输血中意外感染的普通人,到那些在埃及的村庄里排队接受注射的农民,到那些信任医生却被注射了死亡的血友病患者,再到那些在黑暗的干扰素时代苦苦挣扎的患者——他们的痛苦没有白费,他们的故事推动了科学的进步,最终让后来者不必再承受同样的命运。
未完成的使命
然而,HCV的故事并没有以完美的方式结束。尽管我们拥有了可以治愈这种疾病的药物,但全球仍有约五千八百万人携带着病毒——其中许多人甚至不知道自己已被感染。世界卫生组织估计,只有约百分之三十六的感染者知道自己携带病毒,而已确诊的患者中只有约百分之三十接受了治疗。
诊断的障碍是多方面的。急性感染往往没有症状,而慢性感染可能在几十年内都悄无声息。许多人是在出现肝硬化或肝癌症状时才被诊断,那时治疗窗口已经大大缩窄。筛查程序的覆盖面仍然不足,尤其是在资源有限的国家。
治疗的可及性是另一个严峻挑战。当索非布韦首次上市时,一个十二周疗程的价格高达八万四千美元——平均每片药一千美元。这种定价策略引发了全球范围内的争议和愤怒。虽然仿制药的引入大大降低了价格,但在许多低收入国家,DAA药物仍然遥不可及。
疫苗的研发是另一个未竟的事业。与甲型肝炎和乙型肝炎不同,至今没有针对HCV的有效疫苗。病毒的快速变异能力使疫苗设计变得极其困难:研究者很难找到一个稳定的靶点,可以诱导出能够中和各种HCV变异体的抗体。尽管有几种候选疫苗进入了临床试验阶段,但距离成功还有很长的路要走。
但希望仍然存在。2023年,埃及成为世界上第一个被世界卫生组织认可走上消除丙型肝炎道路的国家。通过大规模筛查和治疗运动,这个曾经承受着全球最沉重HCV负担的国家,正在向着消除这种疾病的目标迈进。埃及的成功证明了,即使在资源有限的环境下,只要有足够的政治意愿和合理的资源配置,战胜HCV是可以实现的。
丙型肝炎病毒的故事是一部关于科学、人性、悲剧与救赎的史诗。它告诉我们,医学的进步往往建立在患者的痛苦之上;公共卫生的良好初衷如果没有严谨的科学指导,可能酿成难以想象的灾难;而人类面对疾病时的坚韧和智慧,最终可以化不可能为可能。
从埃及尼罗河畔的注射针管,到英国血友病患者家中的凝血因子冻干粉;从1975年奥尔特手中的神秘血清,到2020年斯德哥尔摩音乐厅里的诺贝尔奖奖章;从干扰素时代的漫长黑夜,到直接抗病毒药物的治愈曙光——HCV的故事跨越了半个世纪,改变了无数人的命运。而这场战斗还在继续。在全球范围内,每一天都有人被感染,有人被诊断,有人被治愈。也许有一天,我们可以像消灭天花一样,将HCV从地球上抹去。那将是这部史诗的最后一章。
参考资料
-
Nobel Prize Committee. The Nobel Prize in Physiology or Medicine 2020: Advanced Information. NobelPrize.org, 2020.
-
Alter HJ, Holland PV, Purcell RH, et al. Clinical and serological analysis of transfusion-associated hepatitis. Lancet, 1975, 2(7940): 838-841.
-
Choo QL, Kuo G, Weiner AJ, et al. Isolation of a cDNA clone derived from a blood-borne non-A, non-B viral hepatitis genome. Science, 1989, 244(4902): 359-362.
-
Kolykhalov AA, Agapov EV, Blight KJ, et al. Transmission of hepatitis C by intrahepatic inoculation with transcribed RNA. Science, 1997, 277(5325): 570-574.
-
Frank C, Mohamed MK, Strickland GT, et al. The role of parenteral antischistosomal therapy in the spread of hepatitis C virus in Egypt. Lancet, 2000, 355(9207): 887-891.
-
Miller FD, Abu-Raddad LJ. Evidence of intense ongoing endemic transmission of hepatitis C virus in Egypt. Proceedings of the National Academy of Sciences, 2010, 107(33): 14757-14762.
-
Infected Blood Inquiry. Final Report. United Kingdom, 2024.
-
World Health Organization. Global Hepatitis Report 2017. Geneva: WHO, 2017.
-
Lawitz E, Mangia A, Wyles D, et al. Sofosbuvir for previously untreated chronic hepatitis C infection. New England Journal of Medicine, 2013, 368(20): 1878-1887.
-
Holmes JA, Rutledge SM, Chung RT. Direct-acting antiviral treatment for hepatitis C. Lancet, 2019, 393(10179): 1392-1394.
-
Bartenschlager R, Lohmann V, Penin F. The molecular and structural basis of advanced antiviral therapy for hepatitis C virus infection. Nature Reviews Microbiology, 2013, 11(7): 482-496.
-
Thong VD, Akbar SMF, Huy NT. Hepatitis C in Egypt – past, present, and future. International Journal of General Medicine, 2016, 10: 25-29.