1953年的一个春日,波士顿儿童医院的实验室里,诺贝尔奖得主托马斯·威勒正盯着显微镜下的细胞培养皿。他的研究对象来自一个三岁男孩身上的水泡液——那是典型的儿童水痘。然而,威勒并不知道,他即将揭开医学史上一个持续近两千年的谜团。当他成功分离出那种病毒后,一个令人震惊的真相浮出水面:困扰儿童的水痘与折磨老人的带状疱疹,竟然是同一个敌人的两种面目。
这个发现颠覆了人类对这种疾病的认知。在威勒之前,没有人能够解释为什么一个人在童年得了水痘后,数十年后会突然在身体某侧长出痛苦的水泡。更没有人想到,那个在记忆中早已远去的儿时疾病,竟然一直在神经系统的深处静静蛰伏,等待着时机重新崛起。
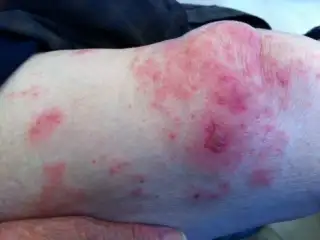
在人类医学史上,很少有疾病像水痘-带状疱疹病毒这样充满了戏剧性的身份转换。它的拉丁学名"varicella"意为"小天花",这个名字本身就揭示了人类对它的长期误解。直到1767年,英国医生威廉·赫伯登才首次系统地描述了水痘与天花的区别。在此之前,这两种疾病在欧洲医学文献中一直被混为一谈。天花的恐怖让任何带有水泡的皮疹都蒙上了死亡的阴影,而水痘的相对温和则让它被视为一种"伪天花"。
古代医学对这种疾病的记载模糊不清。希波克拉底曾描述过一种"疱疹",但他所指的是什么至今仍有争议。罗马医生斯克里博尼乌斯·拉古斯在公元48年首次将"zona"(腰带)一词与这种疾病联系起来——因为带状疱疹典型的皮疹常常环绕腰间,如同一条燃烧的腰带。这个词后来演变成英语中的"shingles",源自拉丁语"cingulus",意为"腰带"。
然而,古代医生们完全不知道水痘和带状疱疹之间存在任何联系。在他们看来,这是两种截然不同的疾病:一种是无害的儿童皮疹,另一种是折磨老年人的痛苦病症。这种误解持续了近两千年。
神经深处的隐秘旅程
水痘-带状疱疹病毒的基因组是一条约125000个碱基对的双链DNA,编码至少71个开放阅读框。与其他疱疹病毒一样,它拥有一层蛋白质衣壳,外面包裹着来自宿主细胞的脂质包膜。在电子显微镜下,这种病毒呈现出典型的疱疹病毒形态——一个直径约125纳米的二十面体,表面布满了糖蛋白刺突。
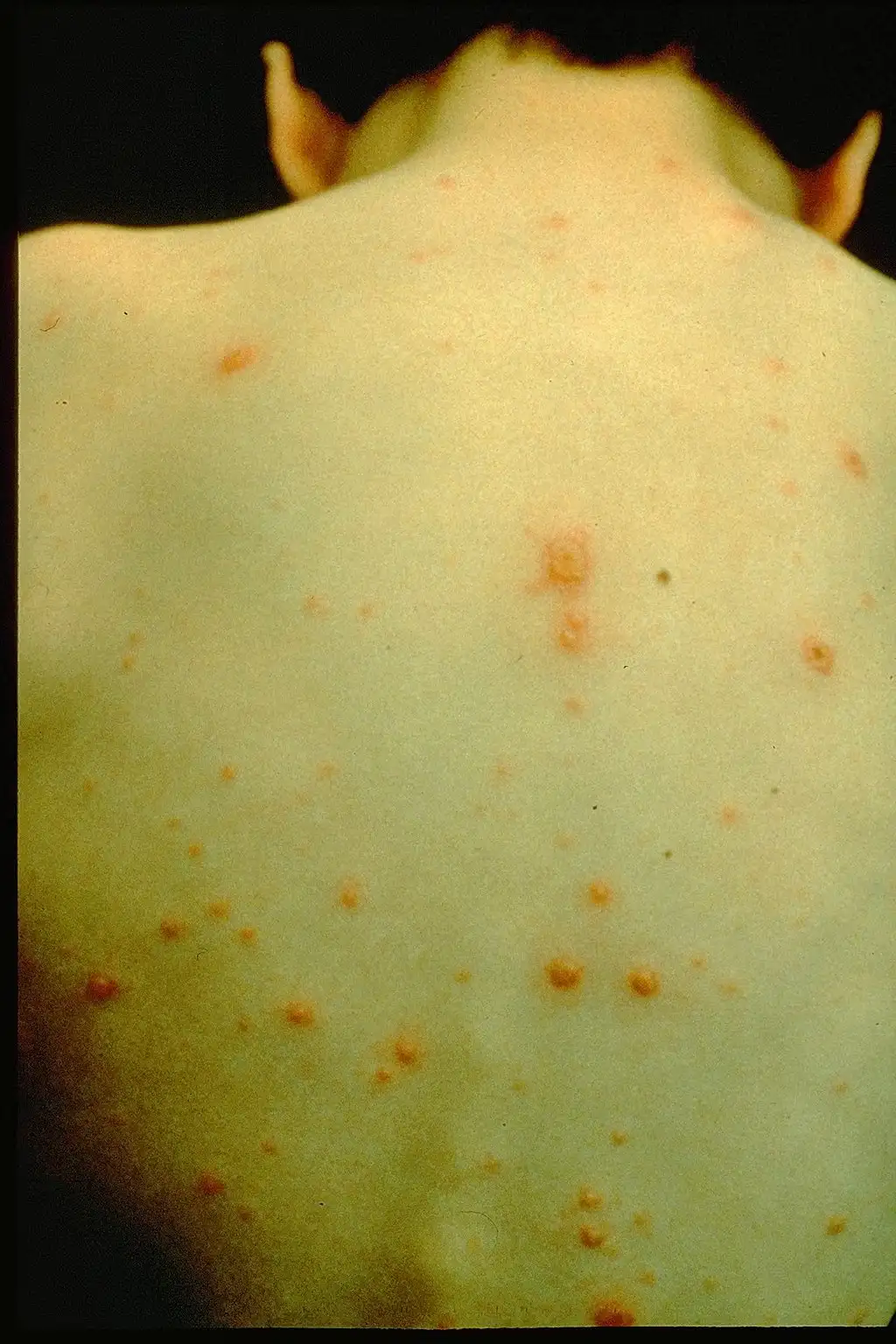
当这种病毒首次进入人体时,它选择的是一条空中航线。感染者的呼吸道飞沫携带着数以百万计的病毒颗粒,通过空气传播进入新的宿主体内。病毒首先在口咽部和上呼吸道的黏膜上皮细胞中建立立足点,进行初步复制。这个过程悄无声息,感染者在接下来的10到21天里完全没有察觉。
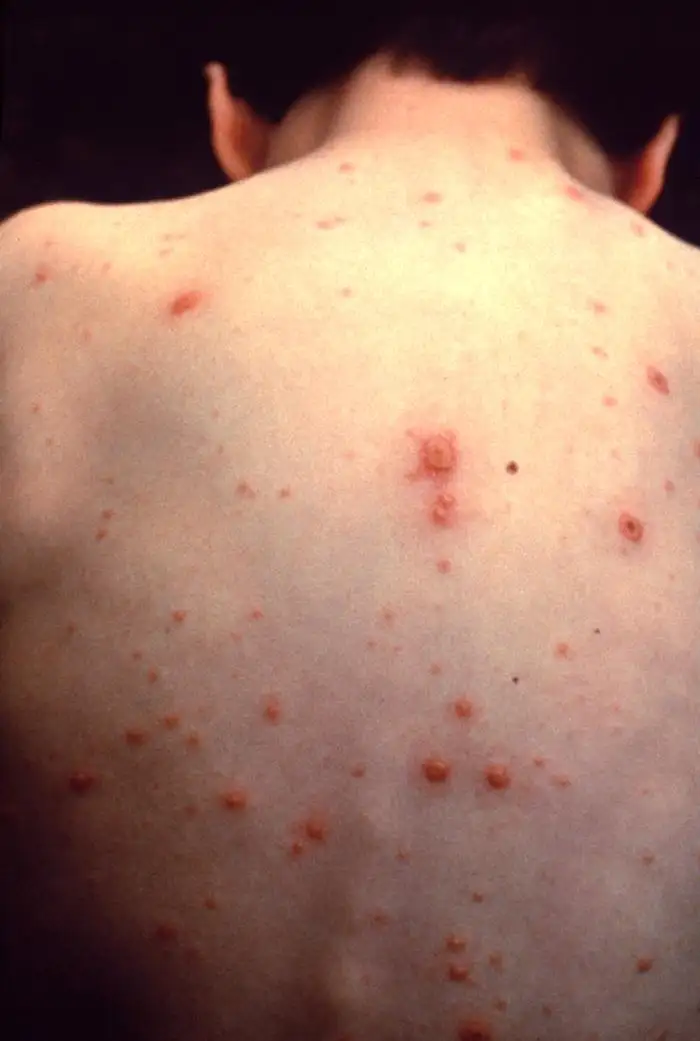
随后,病毒开始了一场精心策划的全身扩散。它侵入局部淋巴结,进入血液循环,建立起第一次病毒血症。血液将病毒带到肝脏、脾脏等内脏器官,在这里进行更大规模的复制。几天后,第二次病毒血症将病毒送往全身皮肤。这时候,典型的水痘皮疹开始出现——从头皮和躯干开始,逐渐蔓延到四肢。每一颗水泡中都充满了数以亿计的病毒颗粒,等待着下一次传播的机会。
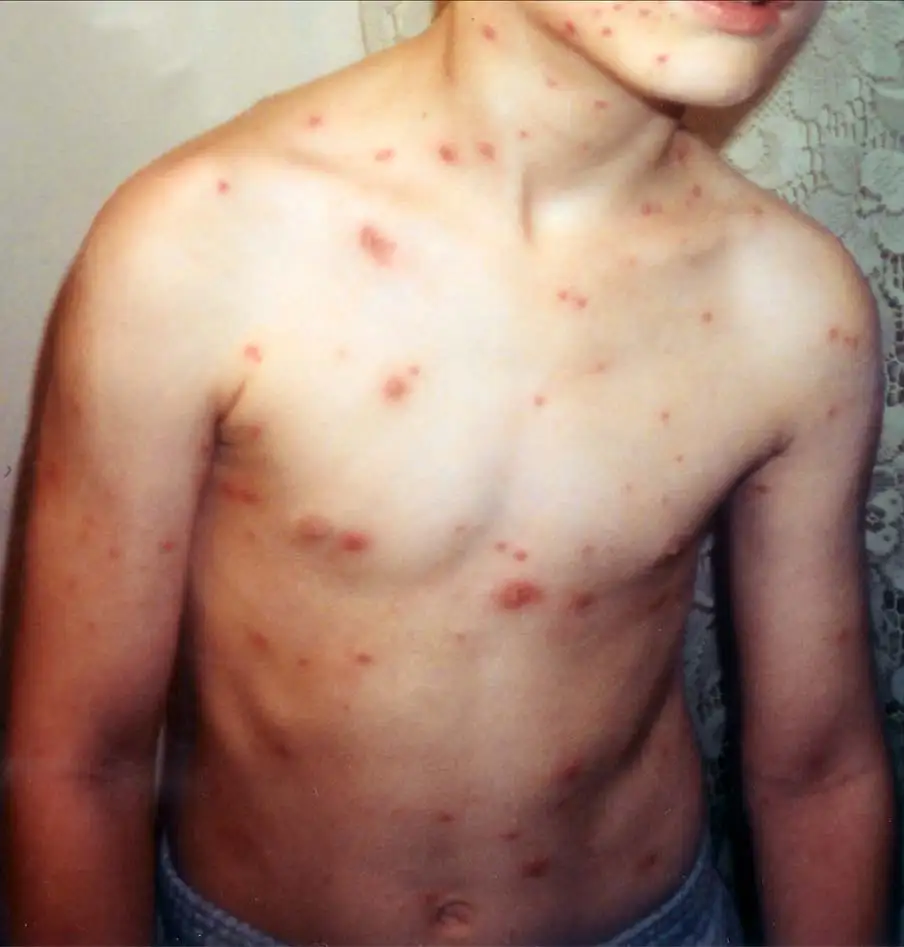
但病毒的真正目标并不是皮肤。在皮疹出现的同时,病毒已经派遣了另一支"特遣队",沿着感觉神经的轴突逆向行进,深入到脊髓背根神经节和三叉神经节。这些神经节是感觉神经元聚集的地方,也是病毒选择的终身庇护所。在这里,病毒将它的基因组以环状附加体的形式保存下来,进入一种近乎完美的休眠状态。
沉默的守望者
在背根神经节的神经元中,病毒展现出了令人惊叹的潜伏策略。与活跃感染时不同,潜伏期的病毒几乎完全不表达蛋白质。它的基因组静静地坐在那里,仅转录少数几个非编码RNA,这些RNA可能帮助维持潜伏状态,防止宿主细胞检测到入侵者的存在。
更令人称奇的是,病毒在潜伏期间并非完全沉默。研究发现,即使在没有明显症状的情况下,病毒的基因也会进行低水平的转录。一种叫做ORF63的基因产物似乎在潜伏期的维持中扮演着关键角色。这种蛋白质可能与宿主的细胞周期调控蛋白相互作用,创造一个有利于病毒潜伏的细胞环境。
神经节中的卫星细胞——那些包裹在神经元周围的小型胶质细胞——也可能成为病毒的藏身之处。这意味着,当一个神经节被感染时,病毒可能同时存在于神经元和卫星细胞中,形成一种"双保险"的潜伏机制。
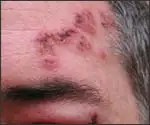
免疫系统当然不会对这种入侵视而不见。在原发感染后,身体会产生针对病毒的特异性T细胞和抗体。这些免疫细胞会定期"巡视"神经节,检查是否有病毒重新激活的迹象。在健康人体内,这种免疫监视极其有效,能够压制病毒长达数十年。
然而,免疫系统的力量会随着年龄增长而衰退。或者当身体遭遇重大压力、疾病或免疫抑制治疗时,这种微妙的平衡可能被打破。病毒感知到免疫监控的松懈,开始激活那些长期沉默的基因。病毒DNA开始复制,新的病毒颗粒在神经元内组装,然后沿着感觉神经轴突向皮肤方向移动。
这就是带状疱疹爆发的开始。
燃烧的腰带
带状疱疹的疼痛常常在皮疹出现前几天就开始了。这种前驱期的疼痛往往让患者和医生都困惑不已——剧烈的烧灼感、刺痛或电击般的痛感,局限在身体的某一个区域。有些患者会误以为是心脏问题、肾结石或腰椎间盘突出。只有当特征性的水泡沿着神经支配的区域成片出现时,诊断才变得明朗。
疼痛的机制是复杂的。病毒在神经节内复制时,会直接损伤神经元和周围的神经组织。更重要的是,活跃复制的病毒会引发强烈的炎症反应,释放大量促炎细胞因子,进一步加剧神经损伤。受损的神经纤维变得异常敏感,即使轻微的触碰——衣服的摩擦、床单的重量——都可能引发剧烈的疼痛。
这种疼痛被一些患者描述为"世界上最可怕的折磨"。在疼痛量表上,带状疱疹的疼痛常常被评定为8到10分——接近甚至超过分娩的痛楚。有些患者因为疼痛而无法睡眠,无法工作,甚至无法进行最基本的日常活动。

当带状疱疹累及面部时,情况可能更加严重。病毒如果侵及膝状神经节,会导致拉姆齐·亨特综合征——一种以外耳道疱疹、周围性面瘫和听力障碍为特征的疾病。2022年,流行歌手贾斯汀·比伯就曾公开透露自己患上了这种疾病,他的一侧面部完全瘫痪,无法微笑、眨眼或移动嘴巴。对于一个依靠表情和舞台表演的艺人来说,这无疑是毁灭性的打击。
更年长的患者面临的威胁是死亡。2019年去世的美国参议员黛安·范斯坦在与带状疱疹的斗争中经历了远比公众所知更严重的并发症。病毒不仅引发了皮疹和剧烈疼痛,还导致了脑炎——一种可能致命的脑部炎症。她的经历揭示了一个残酷的事实:在老年人身上,这种"童年的小病"可能演变成一场生死攸关的危机。
不散的幽灵:带状疱疹后神经痛
当皮疹消退、水泡结痂脱落后,大多数人会以为自己已经痊愈。然而,对于约10%到20%的患者来说,真正的噩梦才刚刚开始。
带状疱疹后神经痛——这个拗口的医学术语背后,是无数患者难以言说的痛苦。在病毒活跃复制期间造成的神经损伤,可能在皮疹完全消失后持续数月、数年,甚至终生不退。有些研究记录了疼痛持续超过三十年的极端病例。
这种慢性疼痛的本质是神经病理性疼痛——一种源于受损神经本身的异常信号。被病毒破坏的神经纤维可能会产生自发性放电,向大脑发送错误的疼痛信号。同时,脊髓和大脑中的疼痛处理中枢可能发生功能重组,变得对疼痛信号过度敏感。
患者描述这种感觉如同"被火烧"、“被电击"或"刀割”。有患者告诉医生,即使是被单轻轻触碰皮肤,都像是有砂纸在摩擦伤口。一位叫玛丽的退休护士在接受采访时说:“我宁愿再经历一次分娩,也不愿忍受这种痛。至少分娩有终点,而这种疼痛可能永远不会结束。”
这种疼痛对患者生活质量的影响是毁灭性的。研究发现,带状疱疹后神经痛患者的抑郁发生率显著高于普通人群。一些患者因为无法忍受持续的痛苦而产生了自杀的念头。在医学文献中,这种疾病有时被含蓄地称为"自杀性疾病"——不是因为病毒本身会致死,而是因为疼痛可能将患者推向绝境。
从绝望到希望:抗病毒药物的诞生
在很长一段时间里,医生们对带状疱疹束手无策。他们能做的只是开些止痛药,等待疾病自行消退。对于带状疱疹后神经痛,更是几乎没有有效的治疗方法。这种状况一直持续到20世纪70年代。
1977年,一种名为阿昔洛韦的药物横空出世,彻底改变了疱疹病毒感染的治疗格局。这种药物的研发者是杰特鲁德·埃利恩——一位没有博士学位却最终获得诺贝尔奖的女性科学家。她在宝来威康公司工作的四十年间,开发了一系列改变医学史的药物,阿昔洛韦只是其中之一。
阿昔洛韦的精妙之处在于它的选择性毒性。这种药物是一种核苷类似物,只有在被疱疹病毒的胸苷激酶磷酸化后才能发挥抗病毒作用。人体的正常细胞缺乏这种酶,因此药物对正常细胞几乎没有毒性。这意味着它可以精确地靶向被感染的细胞,而放过健康的细胞——一个近乎完美的抗病毒策略。
对于带状疱疹患者来说,阿昔洛韦及其衍生物伐昔洛韦和泛昔洛韦的出现意味着什么?如果在皮疹出现后72小时内开始用药,抗病毒药物可以显著缩短病程、减轻症状,并降低带状疱疹后神经痛的风险。这个窗口期虽然短暂,却可能决定患者未来的命运。
然而,抗病毒药物并非万能。对于已经形成的神经损伤,它们无能为力。一旦带状疱疹后神经痛确立,治疗选择就变得有限而艰难。从三环类抗抑郁药到抗癫痫药,从阿片类止痛药到局部麻醉贴片,医生们不得不动用各种工具来控制这种顽固的疼痛。即使如此,许多患者仍然无法获得完全缓解。
沉默的疫苗革命
在抗病毒药物之后,另一个更根本的解决方案正在孕育——疫苗。
水痘疫苗的故事始于1971年的日本。那一年,大阪大学的微生物学家高桥理明从一名叫冈的小孩(Oka是姓氏)的水泡中分离出了病毒。这个三岁男孩患的是典型水痘,高桥理明决定用这个病毒株开发一种减毒活疫苗。
这是一个大胆的想法。当时,大多数人认为水痘是一种"无害"的儿童疾病,不值得为之开发疫苗。然而,高桥理明看到了这种疾病被忽视的一面:在免疫功能低下的儿童——比如白血病患儿——中,水痘可能导致致命的全身感染。他希望通过疫苗来保护这些脆弱的生命。
经过数年的实验室传代减毒,高桥理明成功地研制出了世界上第一支水痘疫苗。1986年,日本批准了这种疫苗的使用。然而,真正让水痘疫苗走向世界的,是美国的决策。1995年,美国食品药品监督管理局批准了水痘疫苗用于常规儿童免疫接种,这标志着人类开始主动出击,而非被动等待这种"童年必经"的感染。
疫苗的影响是深远的。在水痘疫苗广泛接种之前,美国每年约有400万水痘病例,1万到1.3万人因此住院,100到150人死亡。在疫苗接种计划实施二十年后,水痘的发病率下降了90%以上,死亡人数更是减少了近95%。
然而,水痘疫苗的成功带来了一个意想不到的问题:如果孩子们不再得水痘,他们体内就不会产生针对病毒的免疫力。这是否意味着他们将在成年后面临更大的风险?更重要的是,成年人的带状疱疹发病率会如何变化?
答案来自另一种疫苗——带状疱疹疫苗。2006年,美国批准了第一代带状疱疹疫苗Zostavax,这是一种含有高剂量减毒活病毒的疫苗。然而,它的保护效果有限,尤其是在最需要保护的老年人群中的效力随年龄急剧下降。
真正的突破来自2017年。那一年,一种名为Shingrix的重组带状疱疹疫苗获得了批准。这种疫苗不含有活病毒,而是使用病毒的糖蛋白E抗原,配合一种强效的佐剂来激发强烈的免疫反应。临床试验显示,在50岁及以上人群中,Shingrix对带状疱疹的保护效力超过90%,对带状疱疹后神经痛的保护效力更高达88%。
这是一个划时代的成就。对于数以亿计的老年人来说,这种疫苗意味着他们可能永远不必经历那种被描述为"比癌症更痛"的折磨。
被遗忘的角落
尽管在发达国家,水痘疫苗和带状疱疹疫苗已经挽救了无数生命,但在世界的许多角落,这种病毒仍然在肆虐。
世界卫生组织估计,在疫苗广泛接种之前,全球每年约有420万严重水痘病例,约4200人因此死亡。这些数字主要集中在医疗资源匮乏的地区。在发展中国家,水痘仍然是儿童住院的重要原因之一,并发症如继发性细菌感染、肺炎和脑炎时有发生。
更令人担忧的是先天性水痘综合征。当孕妇在妊娠早期首次感染水痘时,病毒可能通过胎盘传播给胎儿,导致一系列严重的先天畸形:肢体发育不全、皮肤瘢痕、眼部异常和神经系统损伤。这种综合征虽然罕见——发生率约为感染孕妇的0.4%到2%——但对受影响家庭来说却是终身的悲剧。
在免疫功能低下的患者身上,水痘-带状疱疹病毒展现出它最致命的一面。艾滋病患者、器官移植接受者、正在接受化疗的癌症患者——当他们的免疫系统被疾病或药物抑制时,病毒的再激活可能演变成全身播散性感染。病毒可能侵入肺部、肝脏、大脑,造成多器官功能衰竭。在这些患者中,死亡率可以高达10%到30%。
2014年,美国报告了一起令人震惊的病例:一名免疫功能低下的患者在接种减毒活带状疱疹疫苗后,竟然发生了疫苗株病毒的全身播散感染,最终不治身亡。这个悲剧性的案例提醒人们,即使是"最安全"的疫苗,在特定的患者群体中也可能带来风险。它也推动了不含活病毒的第二代带状疱疹疫苗的开发。
进化的谜题
水痘-带状疱疹病毒从何而来?它是如何进化出如此精妙的潜伏机制?这些问题至今仍是病毒学研究的前沿课题。
分子进化学研究表明,人类疱疹病毒的祖先可以追溯到数千万年前。水痘-带状疱疹病毒属于α疱疹病毒亚科,与单纯疱疹病毒关系密切。然而,它们在大约6000万到8000万年前就已经分道扬镳,各自进化出了不同的生存策略。
一个有趣的假说认为,水痘-带状疱疹病毒最初可能是一种感染我们灵长类祖先的病毒,随着人类进化而共同演化。支持这一假说的证据来自对灵长类动物疱疹病毒的研究。猴水痘病毒与人类水痘-带状疱疹病毒高度相似,可以引起猴子类似的疾病。这暗示着,在灵长类进化的漫长岁月里,这种病毒一直伴随着我们的祖先。
病毒为什么选择背根神经节作为潜伏地点?神经生物学提供了一些线索。背根神经节是免疫系统监控相对薄弱的区域,血-神经屏障的存在限制了免疫细胞的进入。更重要的是,神经元是高度特化的终末分化细胞,不会分裂——这为病毒的长期潜伏提供了一个稳定的环境。病毒基因组可以在这些细胞中安静地存在数十年,而不必担心被细胞分裂所稀释。
在潜伏期间,病毒究竟在做什么?近年来的研究揭示了一个令人惊讶的事实:病毒的基因组并非完全沉默。即使在潜伏期,病毒也在进行低水平的转录活动。一种叫做潜伏相关转录本的RNA分子在神经节中持续存在,它们可能帮助病毒维持潜伏状态,并为未来的再激活做准备。
未解之谜
尽管科学家们已经对水痘-带状疱疹病毒进行了数十年的研究,这个古老的敌人仍然保留着许多秘密。
我们仍然不完全理解病毒是如何被压抑在潜伏状态的。我们知道T细胞在其中扮演关键角色——当CD4和CD8阳性T细胞的数量下降时,带状疱疹的风险就会上升——但具体的分子机制尚不清楚。病毒是如何"感知"免疫监控的松懈,从而开始再激活的?那些潜伏相关转录本在再激活过程中扮演什么角色?这些问题仍然是活跃的研究领域。
我们也不知道为什么有些人比其他人更容易发生带状疱疹后神经痛。年龄是一个明确的危险因素——老年人更容易发展成这种并发症——但即使考虑到年龄因素,个体之间的差异仍然巨大。遗传因素可能起作用,但具体涉及哪些基因仍不清楚。神经损伤的程度、炎症反应的强度、心理因素——所有这些都可能影响结果,但我们尚未建立起可靠的预测模型。
也许最令人困惑的问题是:带状疱疹疫苗的保护作用能持续多久?Shingrix的临床试验只追踪了参与者数年时间,而带状疱疹的风险可能持续终身。我们不知道在接种十年、二十年后,疫苗的保护效力是否仍然足够。更不知道是否需要加强接种,以及何时接种最为合适。
时间的炸弹
在人类与水痘-带状疱疹病毒的博弈中,有一个事实是无法回避的:世界上绝大多数成年人都携带着这个潜伏的敌人。据估计,超过90%的成年人体内潜伏着水痘-带状疱疹病毒,而其中约三分之一的人将在一生中经历至少一次带状疱疹发作。
随着年龄增长,这个风险不断攀升。在85岁时,约有一半的人将经历过带状疱疹。每一次发作都可能带来长期的疼痛,而那些幸运地避免了带状疱疹后神经痛的人,也可能在下次发作时没那么幸运。
这是一个关于时间的故事。病毒在神经节中耐心地等待,不在乎等待多久——它可以等待十年、二十年、五十年。当宿主变老,当免疫系统疲惫,当压力或疾病削弱了免疫监控,它就会苏醒。它不在乎宿主是谁——参议员也好,流行歌手也罢,在它眼中都是同样的目标。
这种病毒之所以能够如此成功地与人类共存,正是因为它的克制。它很少杀死宿主,因为死亡意味着它自己也将灭亡。相反,它选择了潜伏——一种近乎永生的策略。在每一代新的宿主中,它都能找到新的栖身之所。
这就是水痘-带状疱疹病毒的真面目:一个伪装大师、一个耐心的潜伏者、一个在时间中等待的幽灵。它以最无害的面貌初次登场,却在数十年后露出獠牙。它提醒着我们,在微生物的世界里,没有什么是真正"无害"的——只有暂时潜伏的危险。
而我们能做的,只有接种疫苗、保持健康、在被它袭击时及早治疗。这是一场漫长的战争,而我们手中的武器,比起这个进化了数千万年的敌人,仍然显得稚嫩。
主要参考资料:
- Weller TH. “Serial propagation in vitro of agents producing inclusion bodies with varicella-zoster virus.” Proc Soc Exp Biol Med. 1953.
- Arvin AM. “Varicella-zoster virus.” Clin Microbiol Rev. 1996.
- Gershon AA, et al. “Varicella vaccine.” Infect Dis Clin North Am. 2001.
- Cohen JI. “Strain differences of varicella-zoster virus.” J Infect Dis. 2008.
- Harpaz R, et al. “Prevention of herpes zoster: recommendations of the Advisory Committee on Immunization Practices (ACIP).” MMWR Recomm Rep. 2008.
- Yawn BP, et al. “Herpes zoster health-related quality-of-life.” J Infect Dis. 2021.
- Oxman MN, et al. “A vaccine to prevent herpes zoster and postherpetic neuralgia.” N Engl J Med. 2005.
- Gershon AA, Gershon MD. “Pathogenesis and current approaches to control of varicella-zoster virus infections.” Clin Microbiol Rev. 2013.
- Kennedy PG, et al. “Varicella-zoster virus latency.” Curr Top Microbiol Immunol. 2010.
- Takahashi M. “Development of varicella vaccine.” J Infect Dis. 2008.
- Elion GB. “Acyclovir: discovery, mechanism of action, and selectivity.” J Med Virol. 1993.
- Schmader KE, et al. “Efficacy, safety, and tolerability of herpes zoster vaccine in persons aged 50–59 years.” Clin Infect Dis. 2012.
- Lal H, et al. “Efficacy of an adjuvanted herpes zoster subunit vaccine in older adults.” N Engl J Med. 2015.
- Zerboni L, et al. “Molecular mechanisms of varicella zoster virus pathogenesis.” Nat Rev Microbiol. 2014.
- Hope-Simpson RE. “The nature of herpes zoster: a long-term study and a new hypothesis.” Proc R Soc Med. 1965.
- Gnann JW Jr, Whitley RJ. “Herpes zoster.” N Engl J Med. 2002.
- Dworkin RH, et al. “Recommendations for the management of herpes zoster.” Clin Infect Dis. 2007.
- Johnson RW, et al. “Herpes zoster epidemiology, management, and disease and economic burden in Europe.” Expert Rev Pharmacoecon Outcomes Res. 2019.
- Levin MJ. “Immune responses to herpes zoster.” J Infect Dis. 2018.
- Cohrs RJ, et al. “Varicella-zoster virus transcription.” Curr Top Microbiol Immunol. 2010.