雨后的幽灵
1993年5月14日,新墨西哥州盖洛普市的印第安医疗中心迎来了一位奇怪的病人。19岁的纳瓦霍族青年马拉松运动员,原本身体健康得像一匹野马,此刻却只能靠氧气面罩艰难呼吸。医生们起初以为这只是普通的流感或肺炎,但病情的发展速度让他们瞠目结舌。短短几个小时之内,这位年轻运动员的肺部就像被某种无形的力量淹没,X光片上原本清晰的肺野迅速被白色阴影吞噬。
医生们拼命尝试各种抗生素和抗病毒药物,但一切都徒劳无功。这位年轻人最终在入院后不到24小时内死于急性呼吸衰竭。最令人不寒而栗的是,当医生们试图为他的肺部充气时,涌出的不是空气,而是大量透明液体——他的肺泡已经被某种未知的力量彻底摧毁。

更令人惊恐的是,这只是开始。接下来的两周内,同一地区接连出现了数例相似病例。一位21岁的女性在参加完传统舞蹈仪式后突然发病,她的未婚夫在婚礼前夜被紧急送医,一对年轻夫妇在徒步旅行归来后双双倒下。所有患者都有一个共同特点:他们都是原本健康的年轻人,发病前都在四角地区活动过,并且都经历了相似的死亡过程——肺部被液体淹没,在极度缺氧中窒息而死。
四角地区是犹他州、科罗拉多州、亚利桑那州和新墨西哥州交界的一片广袤荒野,得名于四州交汇的地理坐标。这里是美国纳瓦霍民族的核心居住区,峡谷深邃,台地高耸,干旱的荒漠与翠绿的高山草甸交织。1993年的春天,这片古老的土地即将见证一场医学史上最神秘的疫情调查。
纳瓦霍预言
当疫情调查人员深入纳瓦霍保留地时,一位名叫阿尔文·纳利的部落长老告诉他们一个令人震惊的故事。他说,这种疾病在纳瓦霍人的口述历史中早已存在,被称作"沙漠诅咒"或"鼠疫之灵"。根据传统知识,每当松树果实在某些年份异常丰收,鹿鼠数量就会暴增,而这种疾病就会随之而来。

1992年至1993年的冬季,四角地区经历了罕见的厄尔尼诺现象。大量降雨让干旱的沙漠在一夜之间变得郁郁葱葱,松果、橡子和各种野生植物结出了前所未有的丰收。这种生态繁荣带来了一个意想不到的后果:鹿鼠(Peromyscus maniculatus)的数量呈指数级暴增。这种体型娇小的啮齿动物是北美西部最常见的哺乳动物之一,它们通常在沙漠和草原地带活动,以种子和坚果为食。
纳瓦霍长老们的预言并非迷信,而是世代相传的生态智慧。他们观察到,当鹿鼠数量异常增加时,部落中就会有人患上一种神秘的疾病,患者会在短时间内死于呼吸困难。传统的应对方法是焚烧受感染者的房屋和财物,避免与老鼠及其排泄物接触。这些看似原始的做法,实际上蕴含着深刻的流行病学智慧。
美国疾控中心的科学家们起初对这些传统知识持怀疑态度,但随着调查的深入,他们不得不承认纳瓦霍人的观察是正确的。生态学家发现,1993年春季四角地区的鹿鼠密度比正常年份高出十倍以上。在有些地区,研究人员设置的捕鼠笼几乎每一晚都被装满,鹿鼠的数量已经达到了生态学意义上的"暴发"水平。
追踪隐形杀手
美国疾控中心的特种病原体实验室是世界上最顶尖的病毒学研究机构之一,曾成功分离出埃博拉病毒、汉坦病毒等多种致命病原体。当四角地区的病例报告送达亚特兰大总部时,科学家们立即意识到这可能是一种前所未见的新型传染病。
起初,调查人员怀疑这可能是一种已知的病原体。他们测试了流感病毒、腺病毒、支原体、军团菌等多种常见呼吸道病原体,结果全部呈阴性。他们又测试了鼠疫、土拉菌病、炭疽等生物恐怖制剂可能使用的病原体,同样一无所获。随着死亡人数不断攀升,科学家们感受到了前所未有的压力。
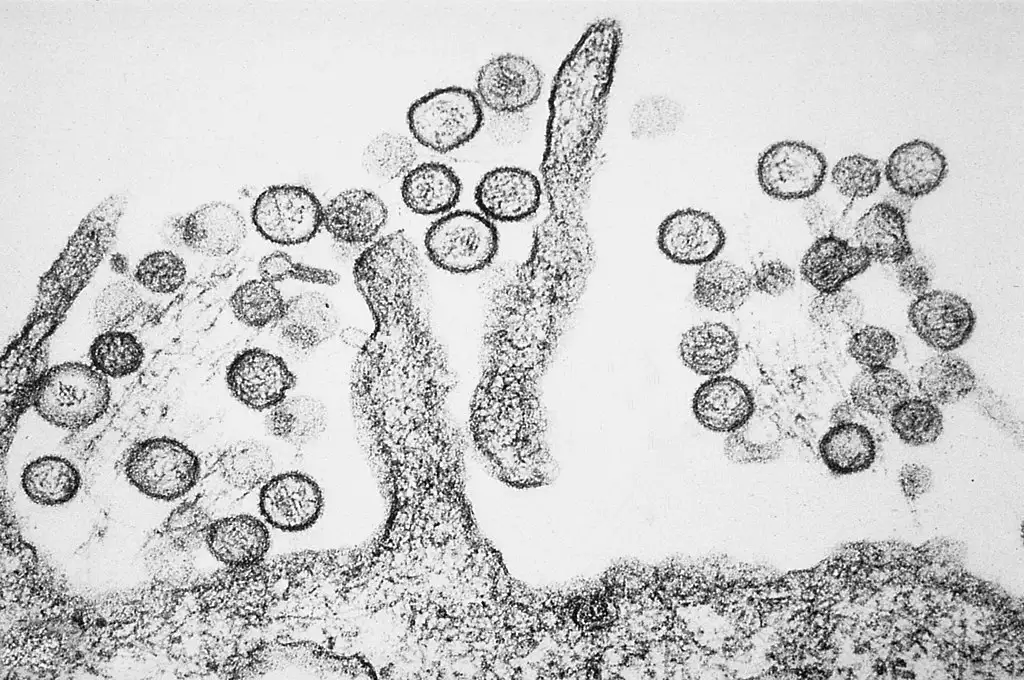
转机出现在6月初。一位年轻的病毒学家在使用电子显微镜观察患者肺组织样本时,发现了一种独特的病毒颗粒。这种病毒呈球形或卵圆形,表面覆盖着网格状的棘突,直径约100纳米。经验丰富的病毒学家立即认出这是布尼亚病毒科的特征形态——这个病毒家族包括多种已知的致病病毒,如裂谷热病毒、拉克罗斯脑炎病毒等。
进一步的血清学测试证实,患者的血清与已知的汉坦病毒存在交叉反应。汉坦病毒?这个发现让科学家们既兴奋又困惑。汉坦病毒是一类通过啮齿动物传播的病毒,最著名的代表是引起朝鲜出血热的汉坦病毒。但已知的汉坦病毒主要引起肾脏损害和出血热,从未有过引起肺部疾病的记录。
科学家们意识到,他们面对的是一种全新的汉坦病毒,一种专门攻击肺部的变异株。为了纪念这一发现,他们将这种病毒命名为"辛诺姆布雷病毒"(Sin Nombre virus),西班牙语意为"无名病毒"。这个名字既反映了科学家们最初对其一无所知的状态,也暗含了对纳瓦霍传统文化的尊重——在纳瓦霍传统中,直呼死者名字被视为禁忌。
分子层面的谋杀
当科学家们成功分离出辛诺姆布雷病毒后,他们开始深入研究这种病毒的致病机制。为什么一种原本攻击肾脏的病毒会突然转而攻击肺部?这个问题的答案隐藏在病毒的分子结构和人类细胞的受体分布中。
汉坦病毒是一类负链RNA病毒,其基因组分为三个片段:大片段(L)编码RNA聚合酶,中片段(M)编码包膜糖蛋白G1和G2,小片段(S)编码核衣壳蛋白。病毒表面的糖蛋白G1和G2负责识别和结合宿主细胞表面的受体。辛诺姆布雷病毒与其他汉坦病毒的关键区别在于其糖蛋白的结构变异,这决定了它的细胞嗜性和致病特点。
研究发现,汉坦病毒进入人体细胞的主要受体是β3整合素(β3 integrin)。这种跨膜蛋白广泛分布于血管内皮细胞、血小板和某些免疫细胞表面,在血管完整性和凝血功能中发挥重要作用。辛诺姆布雷病毒与β3整合素的亲和力特别强,这解释了为什么它能够如此有效地感染血管内皮细胞。

当病毒进入血管内皮细胞后,它并不直接杀死细胞,而是触发了一场失控的免疫风暴。病毒感染的细胞释放大量炎症因子,吸引免疫细胞聚集到感染部位。在肺部,毛细血管内皮细胞是病毒的主要靶标,当它们被感染后,血管壁的完整性遭到破坏,血浆成分大量渗漏到肺泡腔内。
这就是为什么患者的肺部会被"淹没"的原因。病毒并没有直接破坏肺泡上皮细胞,而是通过攻击血管内皮细胞,导致肺毛细血管发生大规模渗漏。患者的肺泡内充满了富含蛋白质的渗出液,这些液体阻碍了氧气进入血液,最终导致患者死于严重的低氧血症。
更可怕的是,这种病毒的潜伏期可以长达数周。患者可能在接触病毒后两到三周才开始出现症状,这让追踪感染源变得异常困难。许多患者回忆不起自己何时何地接触过老鼠或其排泄物,因为那次接触可能只是几个月前在清理车库时吸入的一粒灰尘。
战争中的发现
辛诺姆布雷病毒并非人类历史上遭遇的第一种汉坦病毒。事实上,人类与汉坦病毒的第一次大规模交锋发生在更加残酷的背景中——朝鲜战争。
1951年春天,联合国部队在朝鲜半岛与中国人民志愿军激战正酣。在战火纷飞的前线,一种神秘的疾病开始在士兵中蔓延。患者首先出现高热、头痛和肌肉酸痛,随后出现严重的低血压和休克,最后发展为急性肾衰竭。在最初的病例中,病死率高达15%,而那些幸存的患者往往需要长期透析治疗。
美国军方将这种疾病命名为"朝鲜出血热"或"流行性出血热",但它的真正病因一直是个谜。军医们测试了各种细菌、寄生虫和已知病毒,都无法找到致病源。直到战争结束后多年,科学家们才在1976年成功分离出致病病毒,并以汉坦河(Hantaan River)的名字将其命名为汉坦病毒。
朝鲜战争中的出血热疫情揭示了一个重要规律:汉坦病毒的传播与军事活动密切相关。士兵们在战壕和掩体中生活,这些简陋的住所往往也是啮齿动物的栖息地。当士兵们与老鼠共享有限的空间时,病毒的传播就变得不可避免。类似的疫情后来在巴尔干战争、两伊战争等冲突中多次出现,汉坦病毒几乎成为了战争的"隐形盟友"。

辛诺姆布雷病毒的发现揭示了汉坦病毒家族的另一面。与引起出血热的"经典"汉坦病毒不同,辛诺姆布雷病毒主要引起肺部疾病,被称为汉坦病毒肺综合征(HPS)。这种临床表现的差异与病毒的进化起源有关:引起出血热的汉坦病毒主要分布在欧亚大陆,它们的天然宿主是田鼠和姬鼠;而引起肺综合征的汉坦病毒主要分布在美洲,天然宿主是棉鼠和鹿鼠。
分子进化学研究表明,这两类汉坦病毒在大约4000万年前就开始了分化进化。在那段漫长的岁月里,病毒与其宿主共同进化,最终形成了今天我们所见的多样化病毒谱系。纳瓦霍人口述历史中描述的"鼠疫之灵",很可能已经在这片土地上存在了数千年,只是在特定条件下才会暴发成大规模疫情。
人传人的恐惧
1993年的四角地区疫情最终导致了27例确诊病例,其中17人死亡,病死率高达63%。这个数字让汉坦病毒肺综合征成为了当时美国最致命的传染病之一。然而,科学家们从这次疫情中学到的一个重要教训是:辛诺姆布雷病毒几乎不会在人与人之间传播。
几乎所有病例都可以追溯到直接或间接的啮齿动物接触史。患者要么在清理受老鼠污染的建筑时吸入了含有病毒的气溶胶,要么在户外活动时接触了老鼠的巢穴或排泄物。病毒通过呼吸道黏膜进入人体,然后开始其致命的复制过程。这种传播模式意味着,只要避免与啮齿动物接触,就能有效预防感染。
然而,这个令人安心的结论在2018年被打破了。那一年,阿根廷发生了一起前所未有的人传人疫情暴发。
疫情始于一位35岁的女性患者,她在清理乡间别墅时感染了安第斯病毒(Andes virus),这是南美洲最主要的汉坦病毒类型。患者在发病后几天内死于严重的肺综合征,这本身并不罕见。然而,接下来发生的事情让流行病学家们大惊失色:照顾她的医生、参加她葬礼的亲友,甚至从未去过乡间别墅的家庭成员,陆续出现了相同的症状。
最终的流行病学调查显示,这次疫情共导致32例确诊病例,其中11人死亡。更重要的是,基因测序证实所有患者的病毒序列几乎完全相同,这排除了独立感染的可能性。这是人类历史上第一次证实汉坦病毒可以在人与人之间传播。
安第斯病毒的人传人能力可能与它的生物学特性有关。研究发现,安第斯病毒在呼吸道分泌物中的载量明显高于辛诺姆布雷病毒,这增加了通过飞沫传播的可能性。此外,安第斯病毒表面的糖蛋白结构可能使其更容易在人际间传播。
这个发现改变了公共卫生界对汉坦病毒的认识。在此之前,医护人员在照顾汉坦病毒患者时只需要采取标准防护措施。而现在,对于安第斯病毒感染患者,必须采取类似应对埃博拉或SARS的严格隔离措施。幸运的是,目前仅在安第斯病毒中发现了明确的人传人能力,北美地区的辛诺姆布雷病毒仍然以动物传人为主。
死亡的诊断
汉坦病毒肺综合征的临床经过分为三个阶段:前驱期、心肺期和恢复期。每个阶段都有其独特的临床表现和病理生理特点。
前驱期通常持续3到5天,症状类似流感:发热、头痛、肌肉酸痛、乏力,有时伴有腹痛、恶心和呕吐。这个阶段最难诊断,因为症状缺乏特异性,很难与普通感冒或胃肠炎区分。大多数患者在这个阶段不会寻求医疗帮助,或者被医生当作普通感染处理。
心肺期是疾病的转折点。患者突然出现咳嗽、呼吸困难和低血压,病情在数小时内急剧恶化。胸部X光片显示双侧肺野出现弥漫性浸润阴影,被称为"蝙蝠翼"分布。血液检查显示血小板减少、白细胞增多和血液浓缩。这个阶段的病死率最高,患者往往死于顽固性低氧血症或心源性休克。

如果患者能够熬过心肺期,他们就会进入恢复期。肺部渗出开始吸收,氧合状况逐渐改善,肾功能恢复正常。大多数幸存者在数周内可以完全康复,不遗留明显的后遗症。但也有少数患者可能出现长期的肺功能损害或神经认知障碍。
汉坦病毒肺综合征的诊断一直是临床医生面临的挑战。在前驱期,症状缺乏特异性;在心肺期,患者的病情往往已经非常危重。实验室确诊需要检测血清中的特异性抗体或病毒RNA,但这些检测需要专门的实验室和较长的时间。在疫情初期,大多数病例都是通过回顾性诊断确认的。
1993年的四角地区疫情促使美国疾控中心开发了快速诊断方法。今天,医生可以在几小时内获得初步诊断结果,大大提高了抢救成功率。然而,治疗仍然是对症支持为主,没有特效的抗病毒药物。唯一被证实有效的治疗措施是体外膜肺氧合(ECMO),这是一种将血液引出体外进行氧合的技术,可以替代受损肺部的功能,为患者争取恢复时间。
优山美地的幽灵
2012年夏天,美国加州优山美地国家公园迎来了一场意想不到的危机。这座闻名世界的国家公园每年吸引数百万游客,其壮丽的瀑布和巨石景观是摄影师和户外爱好者的圣地。然而,这一年,公园内最普通的住宿设施——曲线帐篷小屋——成为了汉坦病毒的传播场所。
6月至8月间,共有10名曾在优山美地住过曲线帐篷小屋的游客被确诊感染辛诺姆布雷病毒,其中3人死亡。流行病学调查显示,这些帐篷小屋的隔热层中藏匿着大量鹿鼠,游客在睡觉时可能吸入了含有病毒的气溶胶。
这次疫情震惊了公共卫生界。优山美地是美国管理最完善的国立公园之一,每年接待数百万游客,此前从未发生过如此大规模的汉坦病毒疫情。调查发现,公园管理方虽然在帐篷小屋中设置了防鼠措施,但隔热层的密封性不足,让老鼠得以在墙体内筑巢。
这次疫情促使美国国立公园管理局重新审视了所有公园的啮齿动物防控措施。现在,公园工作人员定期检查和清理可能的啮齿动物栖息地,游客也被教育不要在露营地留下食物残渣。这些措施虽然简单,但被证明能够有效降低汉坦病毒的传播风险。
优山美地疫情还揭示了一个重要问题:汉坦病毒感染不仅仅是农村和偏远地区的问题。随着城市扩张和户外休闲活动的增加,越来越多的人可能与携带汉坦病毒的啮齿动物接触。如何在享受自然的同时保护公众健康,成为了一个需要全社会共同思考的问题。
生态学的警示
1993年四角地区疫情和2012年优山美地疫情有一个共同特点:它们都与异常的气候条件有关。1993年春天,厄尔尼诺现象为四角地区带来了罕见的降雨;2012年,加州经历了异常温和的冬季,鹿鼠的生存率大大提高。
这些观察揭示了一个重要的生态学规律:汉坦病毒的暴发往往是生态系统失衡的结果。当气候条件有利于啮齿动物繁殖时,病毒传播的风险就会增加。而这种生态失衡,往往与人类活动密切相关。
气候变化正在改变全球的降水模式和温度分布。一些地区正在经历更频繁的极端降雨事件,另一些地区则面临更长的干旱期。这些变化正在影响啮齿动物的分布和数量,进而影响汉坦病毒等野生动物传播疾病的流行模式。
2023年发表的一项研究预测,在中等排放情景下,北美地区汉坦病毒感染风险将在本世纪中叶增加约50%。这是因为气候变化正在扩大鹿鼠的栖息地范围,同时增加极端气候事件的发生频率。
人类对自然环境的改变也在影响汉坦病毒的传播。森林砍伐、农业扩张和城市化正在破坏啮齿动物的自然栖息地,迫使它们与人类居住区更加接近。当人类住宅和啮齿动物栖息地重叠时,病毒从动物传播到人类的机会就会大大增加。
生存的艺术
1993年疫情中有一位幸存者的故事特别令人动容。26岁的布鲁斯·安德森是一位户外运动爱好者,他在徒步旅行归来后开始出现发热和肌肉酸痛。最初他以为只是流感,但当呼吸困难的症状出现时,他意识到情况不对。
安德森被紧急送往阿尔伯克基的医疗中心,他的血氧饱和度已经降到了危险的水平。医生们决定使用ECMO进行支持治疗,这在当时还是一项相对新的技术。安德森在ICU中度过了三周,期间多次濒临死亡。他的肺部几乎完全被液体填满,只能依靠机器维持生命。
当安德森最终康复出院时,他失去了一个肾——汉坦病毒在攻击肺部的同时也损害了他的肾脏功能。但他活了下来,并且成为了汉坦病毒肺综合征幸存者支持网络的积极成员。他告诉后来者,恐惧是正常的,但希望永远存在。
安德森的经历也揭示了汉坦病毒肺综合征的一个特点:幸存者通常不会遗留严重的永久性肺损伤。与新冠等病毒引起的肺纤维化不同,汉坦病毒造成的肺部损害在很大程度上是可逆的。这意味着,只要患者能够在急性期获得适当的支持治疗,完全康复的希望是存在的。
今天,汉坦病毒肺综合征的病死率已经从1993年的60%以上下降到约35%。这主要归功于更早期的诊断和更先进的重症监护技术。ECMO的使用将最危重患者的生存率提高到了约50%,这在几十年前是不可想象的。
然而,特效治疗仍然缺席。利巴韦林是一种广谱抗病毒药物,在体外实验中对汉坦病毒有一定活性,但临床试验未能证实其对汉坦病毒肺综合征的治疗效果。科学家们正在开发针对汉坦病毒的特异性抗体和疫苗,但这些产品距离临床应用还有很长的路要走。
千年的智慧
1993年的疫情最终在当年6月得到控制。随着夏季高温的到来,鹿鼠的活动减少,新发病例逐渐消失。当流行病学调查完成时,科学家们确认了26例确诊病例,其中12人死亡。这个数字虽然远低于流感等其他传染病,但汉坦病毒肺综合征的高病死率让它成为了美国公共卫生界长期关注的重点。
疫情结束后,美国疾控中心与纳瓦霍民族建立了长期合作关系。纳瓦霍传统知识被纳入汉坦病毒防控策略,部落卫生工作者接受培训成为社区健康教育的主力军。这种合作模式成为了将传统知识与西方医学相结合的成功范例。
今天,当春季来临、松果丰收的时候,纳瓦霍社区会收到汉坦病毒风险预警。居民们知道要避免接触啮齿动物,清理可能藏匿老鼠的建筑时要佩戴防护装备。这些看似简单的措施,实际上是千年智慧的现代应用。
汉坦病毒肺综合征的故事告诉我们,人类与传染病之间的斗争远未结束。在人类不断扩张自己的生存空间的同时,新的病原体可能随时从野生动物的栖息地中浮现。只有尊重自然、理解生态、重视传统知识,我们才能在这场永恒的博弈中保持优势。
四角地区的荒野依旧广袤,峡谷中的风声依旧呜咽。鹿鼠在岩石缝隙中繁衍生息,它们携带的病毒也在沉默中等待下一个机会。当下一场大雨降临时,也许会有新的故事上演。但这一次,我们已经准备好了。
参考文献
-
Nichol ST, Spiropoulou CF, Morzunov S, et al. Genetic identification of a hantavirus associated with an outbreak of acute respiratory illness. Science. 1993;262(5135):914-917.
-
Hjelle B, Glass GE. Outbreak of hantavirus infection in the Four Corners region of the United States in the wake of the 1992-1993 El Niño. J Infect Dis. 2000;181(5):1569-1573.
-
Pini N. Hantavirus pulmonary syndrome in Latin America. Curr Opin Infect Dis. 2004;17(5):413-417.
-
Martinez VP, Bellomo C, San Juan J, et al. Person-to-person transmission of Andes virus. Emerg Infect Dis. 2005;11(12):1848-1853.
-
Macneil A, Nichol ST, Spiropoulou CF. Hantavirus pulmonary syndrome. Virus Res. 2011;162(1-2):138-147.
-
Watson DC, Sargianou M, Papa A, et al. Epidemiology of Hantavirus infections in humans: A comprehensive review. Viruses. 2014;6(6):2360-2387.
-
Dearing MD, Dizney L. Ecology of hantavirus in a changing world: the future of medical mammalogy. J Mammal. 2010;91(6):1292-1300.
-
Mackelprang R, Dearing MD, St Jeor SC. Evolutionary history of hantaviruses and their rodent hosts. J Virol. 2019;93(17):e00123-19.