1908年的北非,突尼斯巴斯德研究所的实验室里,两位科学家正埋头于显微镜前。查尔斯·尼科尔和路易·芒索正在研究一种名为甘迪的小型啮齿动物,这是从北非沙漠中采集而来的奇特生物。当他们将甘迪的脾脏组织置于显微镜下时,一个意想不到的发现呈现在眼前——一种从未被描述过的微小生物正在细胞间穿行。它有着新月状的优美身形,一端尖锐,一端圆润,在组织切片中显得既诡异又精致。两位科学家最初以为这是利什曼原虫的近亲,甚至打算将其命名为"甘迪利什曼原虫"。但进一步的观察让他们意识到,这是一个全新的物种。他们将这种寄生虫命名为"弓形虫"——希腊语中意为"弓形的形态"。他们无法想象,这个偶然的发现将打开一个怎样的潘多拉魔盒。就在同一年,远在巴西的阿尔方索·斯普伦多雷也在实验用兔子身上独立发现了这种寄生虫。两条平行的发现之路,共同揭开了这个隐形杀手的神秘面纱。
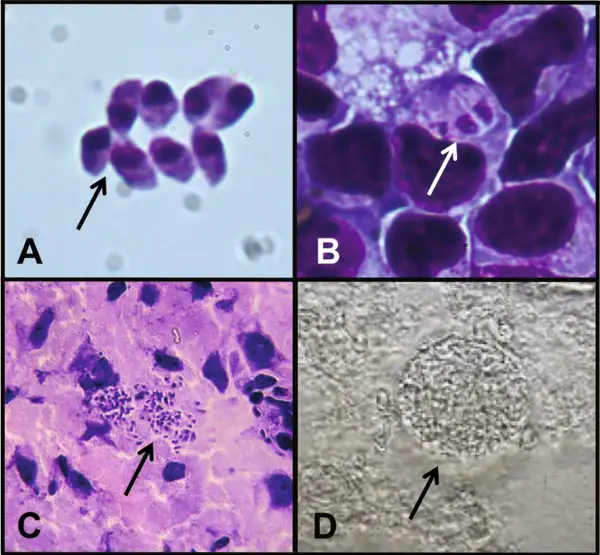
与猫的黑暗契约
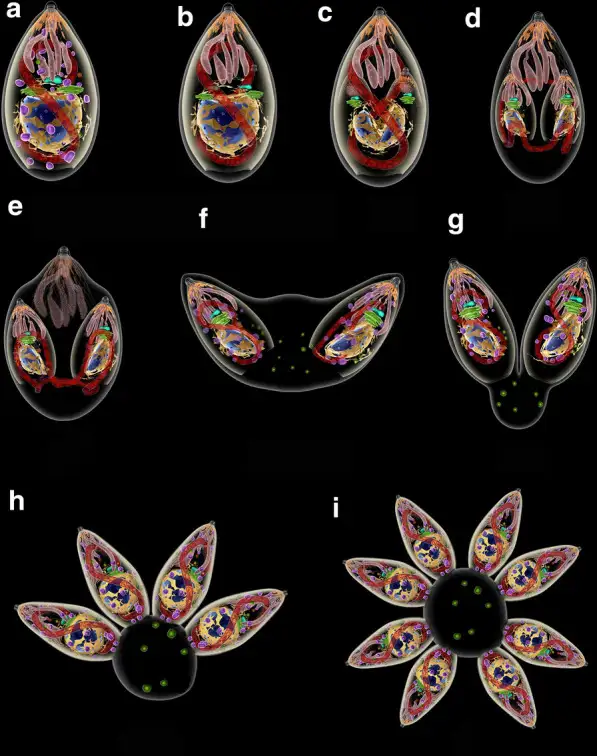
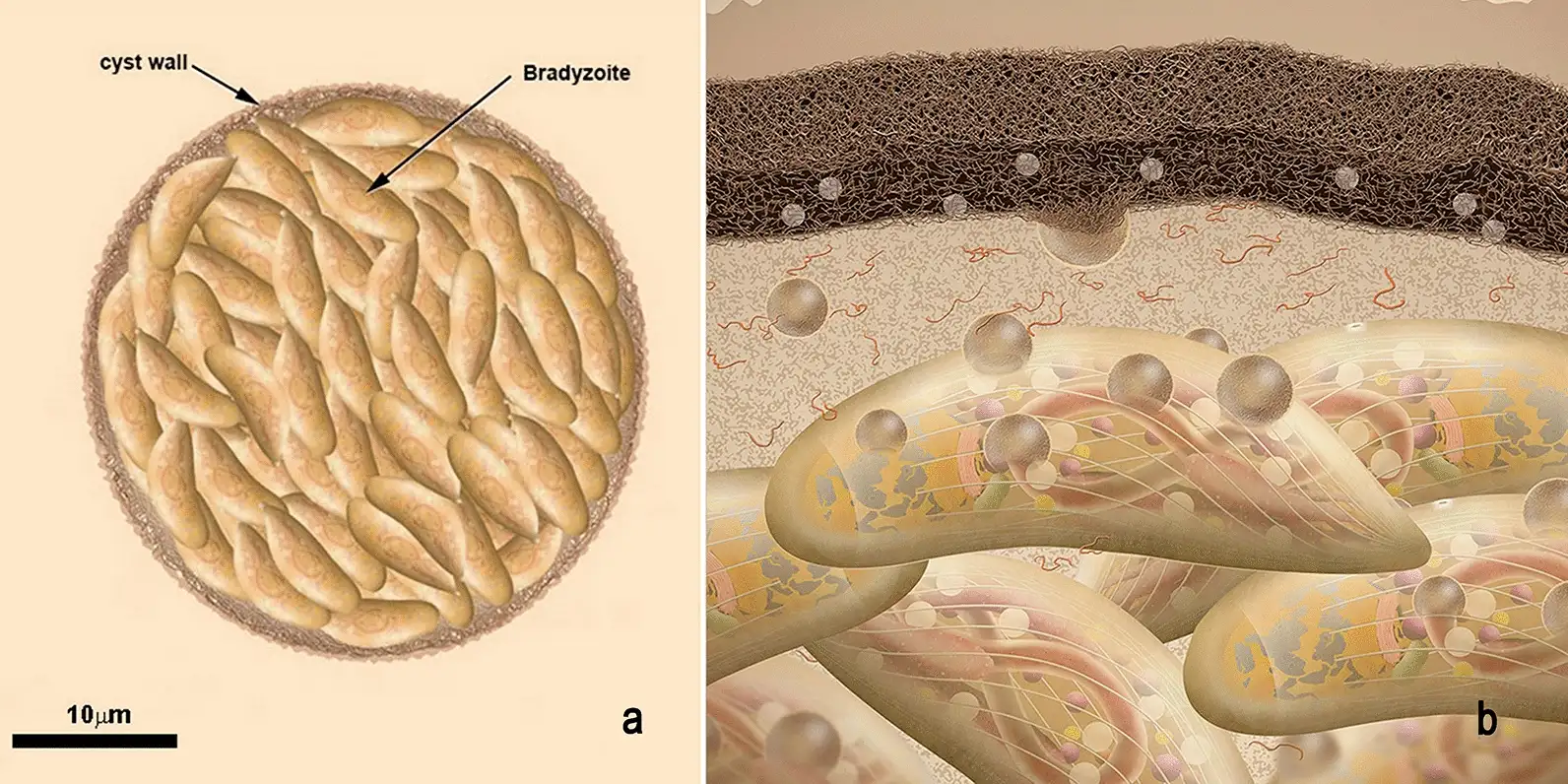
弓形虫最令人惊叹的特征在于其复杂而精巧的生命周期。它是一种专性细胞内寄生虫,能够感染几乎所有温血动物,但唯有猫科动物能够承载它的有性繁殖阶段。这意味着猫是弓形虫的终宿主,而包括人类在内的所有其他动物都只是中间宿主。当一只猫第一次感染弓形虫后,寄生虫在其小肠上皮细胞中进行一场隐秘的性爱狂欢。雌配子和雄配子融合形成合子,最终产生数以百万计的卵囊,随猫粪排出体外。这些卵囊直径仅约10至12微米,肉眼完全无法察觉。刚排出的卵囊尚未成熟,不具有感染性。但在适宜的温度和湿度下,它们会在1至5天内完成孢子化,每个卵囊内分裂出两个孢子囊,每个孢子囊内含四个子孢子。孢子化后的卵囊具有惊人的环境抵抗力——它们能在土壤中存活数月甚至数年,耐受冰冻、干燥和大多数消毒剂。一只新感染的猫在短短两周内可以排出上亿个卵囊,将弓形虫的种子撒向整个世界。中间宿主通过摄入被卵囊污染的水、食物或土壤而感染。一旦进入体内,卵囊壁被消化酶分解,释放出子孢子。这些微小的入侵者迅速穿透肠壁,进入血液循环,开始它们在宿主体内的长途跋涉。它们能够感染几乎所有类型的 nucleated 细胞,但似乎对神经细胞和肌肉细胞有着特殊的偏好。
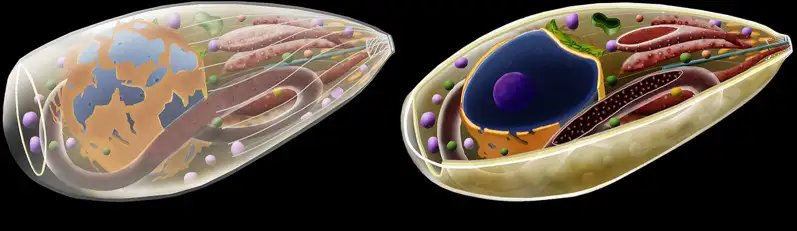
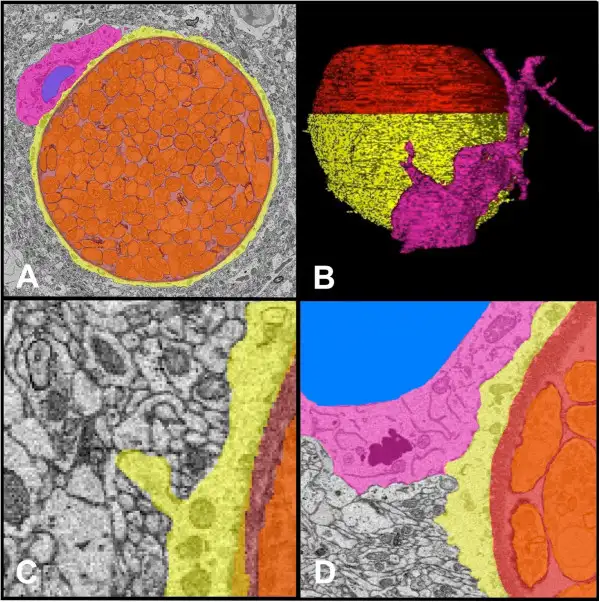
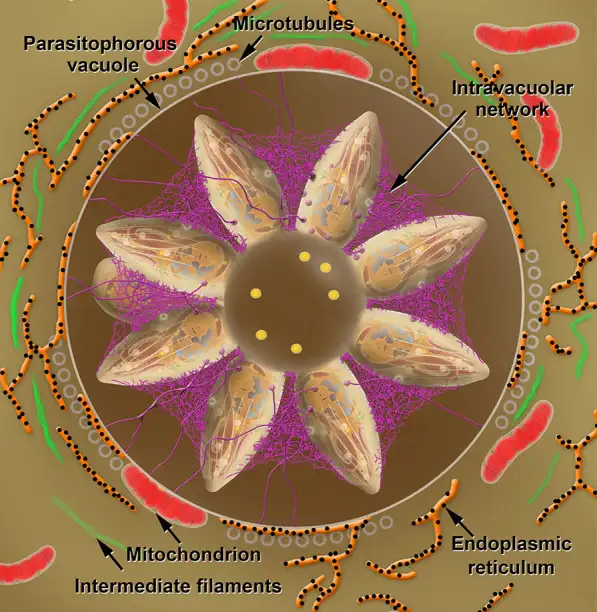
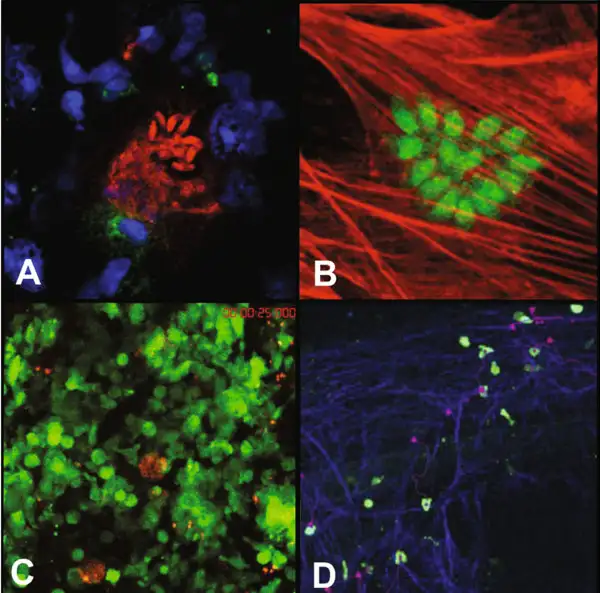
在感染的急性期,弓形虫以速殖子的形态存在。这些新月形的细胞以其惊人的繁殖速度著称——它们通过一种称为内双殖的无性繁殖方式,在24至48小时内就能从一个细胞中释放出数十个子代。速殖子主动入侵宿主细胞的过程堪称分子层面的精密军事行动。它们拥有一套被称为"顶端复合体"的特殊装备,包括锥体、微线体和棒状体等细胞器。当速殖子接近宿主细胞时,锥体向前伸出,微线体分泌黏附蛋白,与宿主细胞表面的受体结合。随后,棒状体蛋白被注入宿主细胞,形成一个被称为"移动连接"的特殊结构。速殖子就像穿针引线一般,沿着这个连接滑入宿主细胞内部。最神奇的是,这个过程不会触发宿主细胞的吞噬机制,寄生虫被包裹在一个由宿主细胞膜衍生的纳虫泡中,与宿主细胞的溶酶体系统完全隔离。纳虫泡成为寄生虫的完美庇护所,在这里,它们可以获得营养、进行繁殖,而不被宿主的防御系统察觉。但当宿主的免疫系统被激活后,一场无声的战争开始了。干扰素γ等细胞因子被释放,巨噬细胞被募集到感染部位。面对免疫系统的围剿,速殖子做出了一个惊人的战略转变——它们开始分化为缓殖子。
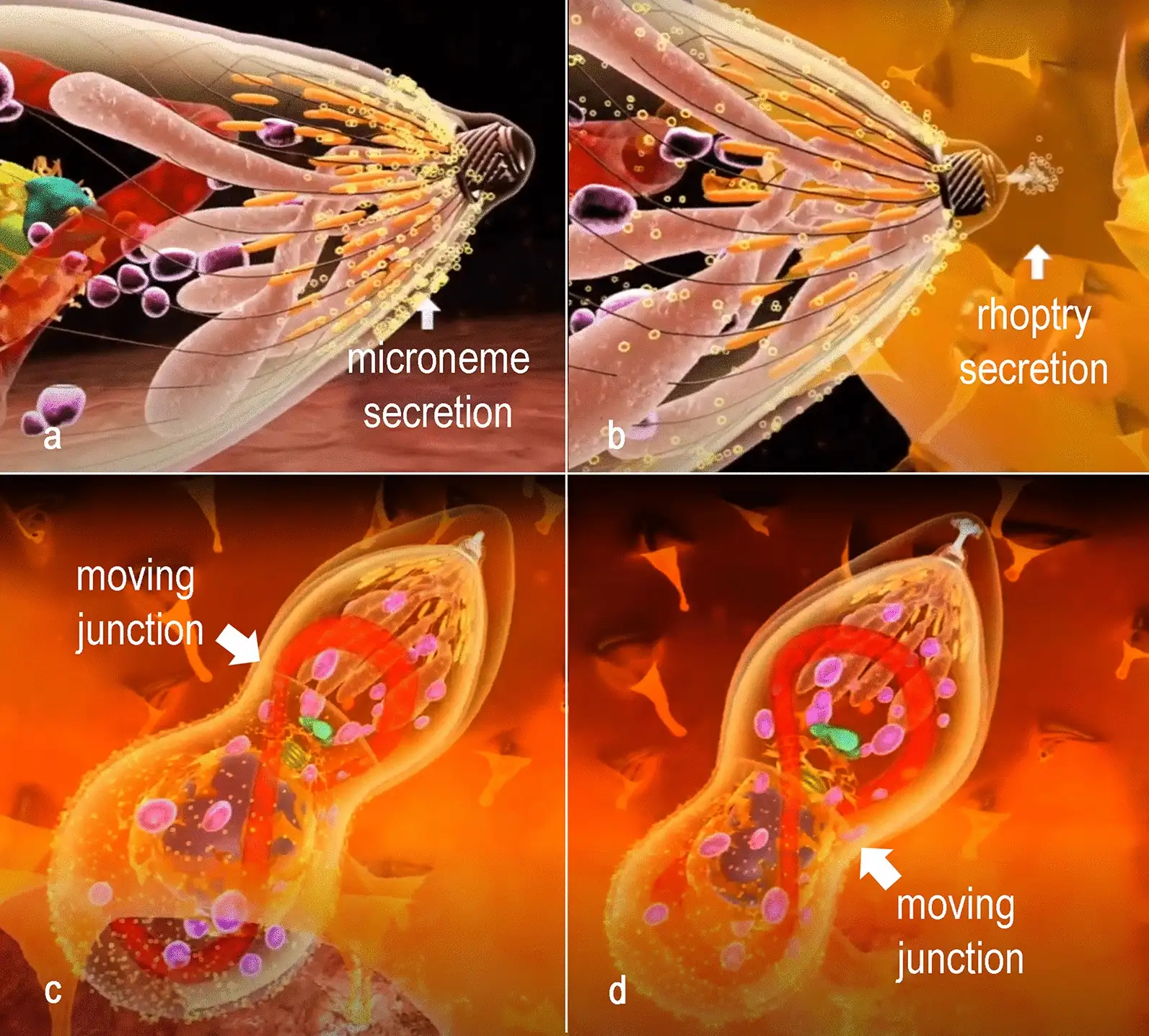
缓殖子的繁殖速度大大降低,它们在宿主细胞内建造一个坚固的堡垒——组织囊。这个囊壁由寄生虫分泌的蛋白质和宿主细胞来源的成分共同构成,厚度可达0.5微米,能够抵抗多种蛋白酶的消化。组织囊主要在大脑和肌肉组织中形成,大脑中的组织囊尤其令人不安。一个成熟的组织囊直径可达60微米,内含数千个缓殖子。它们静静地潜伏在神经元、星形胶质细胞和小胶质细胞中,与宿主达成一种微妙的休战状态。免疫系统无法彻底清除这些组织囊,而组织囊内的缓殖子也不会主动攻击宿主。这种僵持状态可以持续宿主的整个生命。但一旦宿主的免疫功能下降——比如艾滋病患者、器官移植接受者或接受化疗的癌症病人——缓殖子就会从组织囊中重新激活,转化为速殖子,再次引发急性感染。在大脑中,这种再激活可能导致致命的弓形虫脑炎。弓形虫的生命周期在1970年被完整揭示,这距离其发现已经过去了整整62年。英国科学家威廉·哈钦森等人在实验中发现,只有当猫摄入含有组织囊的肉类后,才能在其粪便中检测到卵囊。随后的研究证实,猫科动物是弓形虫唯一能完成有性繁殖的宿主。这一发现揭示了弓形虫与猫之间长达数百万年的共同进化历史,也解释了为什么这种寄生虫会进化出如此精巧的行为操控机制。
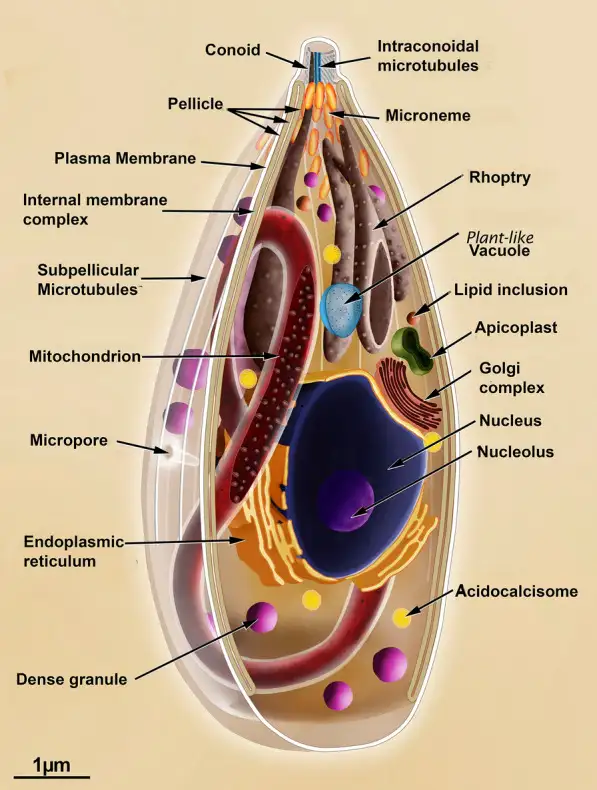
让老鼠爱上猫
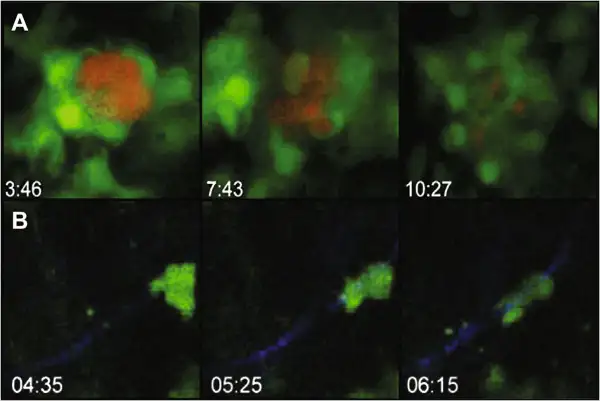
2000年,牛津大学的科学家在《英国皇家学会学报》上发表了一项令人震惊的研究。他们发现,感染了弓形虫的大鼠会丧失对猫尿液的先天恐惧,反而表现出一种诡异的"吸引力"。在正常情况下,大鼠闻到猫尿的气味会立即逃离,这是数百万年进化形成的生存本能。但感染弓形虫后,大鼠不仅不再逃避,甚至会主动接近猫尿的气味源。更令人毛骨悚然的是,研究发现这种"致命吸引力"具有高度特异性——感染的大鼠对狐狸尿液等其他捕食者的气味仍然保持正常的回避反应,唯独对猫的气味产生了致命的迷恋。这绝非偶然。这种行为改变对弓形虫而言是完美的生存策略:感染的老鼠主动走向猫口,被吃掉后,弓形虫就能回到其终宿主体内,完成有性繁殖,开启新一轮的生命循环。这是寄生虫操控宿主行为的终极案例,是自然选择在微观层面写就的恐怖剧本。
随后的研究揭示了这一操控机制的分子基础。弓形虫能够编码一种酪氨酸羟化酶,这种酶能够催化酪氨酸转化为左旋多巴,而左旋多巴正是多巴胺合成的前体。多巴胺是大脑中至关重要的神经递质,参与调控奖赏、动机、运动和情绪等多种功能。弓形虫在大脑中释放的多巴胺,可能改变了宿主对恐惧和奖赏信号的神经处理方式。感染大鼠的大脑中,负责处理恐惧的杏仁核区域活动发生了显著改变,而负责奖赏处理的伏隔核却被异常激活。当感染大鼠闻到猫尿时,本该触发恐惧和逃跑反应的神经通路被劫持,取而代之的是一种诡异的"奖赏感"。它们不是不再害怕猫,而是开始"喜欢"猫的气味。2011年的一项研究进一步发现,弓形虫感染还会改变大鼠睾酮水平,增加其冒险行为。雄性感染大鼠变得更加大胆,在开放区域停留的时间更长,探索行为更加频繁。这些行为改变不仅增加了它们被捕食的风险,也可能影响其在种群中的社会地位和繁殖机会。弓形虫的操控能力甚至延伸到了更微妙的层面。研究发现,感染的大鼠对猫尿气味的"迷恋"具有学习性——它们似乎发展出了一种对猫尿气味的"性吸引"。科学家在大鼠的大脑中观察到,弓形虫感染激活了与性唤起相关的神经通路。当感染大鼠闻到猫尿时,其大脑中与性吸引相关的区域被点亮,仿佛它们在面对求偶信号。这是何等精密的操控——寄生虫不是简单地抑制宿主的恐惧,而是将恐惧转化为欲望,将死亡信号转化为诱惑。
人类是否也在被操控
如果弓形虫能够操控大鼠的行为,那么感染了这种寄生虫的人类又会如何?全球约三分之一的人口血清学检测呈阳性,意味着数十亿人的大脑中潜伏着弓形虫组织囊。在法国、巴西等国家和地区,感染率甚至高达60%至80%。如此广泛的感染是否会对人类行为产生影响?这个问题自1990年代以来一直是科学研究的热点。捷克进化生物学家雅罗斯拉夫·弗莱格尔是这一领域的先驱。他在一系列精心设计的研究中发现,弓形虫感染与人类人格特征存在显著关联。感染者在人格测试中表现出更高的焦虑倾向、更强的冲动性和更低的社会服从性。更引人注目的是,这些效应似乎存在性别差异。感染男性往往更加多疑、嫉妒心更强、更不愿意遵守社会规范;而感染女性则表现出更高的热情、更低的焦虑和更高的社会服从性。弗莱格尔的研究还发现,弓形虫感染可能影响人类的反应时间和注意力。在一项针对布拉格居民的广泛研究中,感染者在计算机化反应时测试中的表现显著低于未感染者。这一发现引发了令人不安的联想:如果感染影响反应速度,是否也会影响驾驶安全?随后的大规模流行病学研究似乎证实了这一假设。2002年发表的一项捷克研究发现,在交通事故受害者中,弓形虫感染率显著高于普通人群。感染者的交通事故风险是未感染者的2.65倍。这一发现在随后的多项研究中得到了复制,尽管也有研究者对因果关系提出质疑。更为大胆的研究探讨了弓形虫感染与创业行为之间的关系。2018年发表在《英国皇家学会学报》上的一项跨国研究发现,弓形虫感染率较高的国家,其居民的创业意愿和实际创业率也更高。在美国,参加创业活动的专业人士中,感染者的创业可能性是未感染者的1.8倍。研究者推测,弓形虫感染可能通过降低风险厌恶、增加冲动性,从而促进冒险的商业行为。然而,这些发现也引发了激烈的学术争议。批评者指出,大多数关于弓形虫与人类行为的研究是相关性研究,难以证明因果关系。可能存在混杂变量——例如,某些人格类型可能更容易接触感染源,或者社会经济地位同时影响感染风险和行为模式。2023年发表的一项大规模队列研究分析了超过45000人的数据,发现弓形虫感染与多种精神健康指标之间的关联在控制混杂因素后大大减弱。
精神分裂症的隐形推手
关于弓形虫与人类健康最令人不安的关联,莫过于其与精神分裂症的关系。这一假说最早由捷克研究者于1950年代提出,但直到1990年代才受到严肃对待。多项流行病学研究一致发现,精神分裂症患者中弓形虫抗体阳性率显著高于普通人群。2015年发表的一项大规模荟萃分析综合了38项研究的数据,确认了这一关联的存在——感染者患精神分裂症的风险增加约2.7倍。更令人震惊的是,研究发现母亲孕期感染弓形虫与子代日后患精神分裂症的风险增加相关。2005年发表的一项丹麦全国性队列研究追踪了近200万人,发现母亲孕期弓形虫抗体阳性者,其子代在成年后患精神分裂症的风险增加了近50%。这提示弓形虫可能通过影响胎儿大脑发育,埋下精神疾病的种子。从生物学角度看,这一假说并非毫无根据。弓形虫组织囊在大脑中的存在、其对多巴胺代谢的影响、以及其引发的神经炎症反应,都可能构成精神分裂症发病的风险因素。斯坦利医学研究所的研究发现,感染特定弓形虫基因型的个体,其精神病性症状的严重程度更高。动物实验也显示,弓形虫感染会改变小鼠的行为模式,包括减少理毛行为、降低社会互动、增加刻板行为——这些都与精神分裂症的阴性症状相似。然而,因果关系仍然难以确立。是弓形虫感染增加了精神分裂症风险,还是精神分裂症患者更易暴露于感染源?或者两者共享某些风险因素?2022年发表的一项孟德尔随机化研究利用遗传变异作为工具变量,试图解开这一因果难题。研究发现了弓形虫感染与精神分裂症风险之间可能存在因果关联的证据,但效应量相对较小。这提示弓形虫可能是精神分裂症众多风险因素之一,而非唯一致病原因。无论如何,弓形虫与精神分裂症的关联研究已经改变了我们对精神疾病的理解。它提示我们,某些精神疾病可能具有感染性起源,而免疫系统、神经系统和精神健康之间存在复杂的交互作用。
孕妇的噩梦
1939年,纽约哥伦比亚大学的病理学家阿贝尔·沃尔夫、大卫·考恩和本杰明·佩奇在《科学》杂志上发表了一篇划时代的论文。他们描述了一个出生仅三天的女婴,她患有严重的脑炎,出生后即出现抽搐发作。病理检查显示,婴儿的大脑中存在广泛的炎症和坏死,显微镜下可见大量新月形的寄生虫。研究人员将婴儿的脑组织接种到小鼠和兔子体内,成功复制了感染,从而首次确认弓形虫是人类疾病的病原体。这例病例开创了先天性弓形虫病的概念——孕妇在妊娠期间首次感染弓形虫后,寄生虫可通过胎盘传播给胎儿。先天性弓形虫病是弓形虫感染最严重的后果之一。孕妇首次感染弓形虫后,寄生虫进入血液循环,穿越胎盘屏障,感染正在发育中的胎儿。传播风险随孕周增加而上升——早孕期感染传播率约15%,而晚孕期感染传播率可达60%以上。然而,感染的严重程度却与传播风险呈反比关系。早孕期感染虽传播率较低,但一旦发生,往往造成最严重的后果;而晚孕期感染虽传播率较高,但胎儿损害通常较轻。先天性弓形虫病的典型表现被称为"Sabin三联征":脉络膜视网膜炎、脑积水或小头畸形,以及颅内钙化。脉络膜视网膜炎是最常见的表现,累及约80%的有症状患儿。弓形虫侵犯视网膜和脉络膜,引起炎症、坏死和瘢痕形成,可导致严重的视力损害甚至失明。脑积水是另一个严重并发症,弓形虫感染引起的室管膜炎和导水管阻塞导致脑脊液循环障碍,颅内压急剧升高。如果不及时干预,脑积水可导致不可逆的脑损伤。颅内钙化则是弓形虫在脑组织中形成组织囊后留下的痕迹,在影像学检查中呈现为多发的高密度病灶。
先天性弓形虫病的预后差异巨大。约85%的感染婴儿出生时无明显症状,被称为"亚临床感染"。但这并不意味着他们安全无虞——这些孩子中约85%会在儿童期或青春期出现眼部病变、听力损失或神经发育障碍。对于出生时即有明显症状的患儿,预后更为严峻。未经治疗的有症状患儿死亡率可达12%,幸存者中约85%存在智力障碍,约80%发生癫痫,约50%存在严重的视力损害。2019年,芝加哥大学医学中心的研究者发表了一项令人鼓舞的研究。他们发现,即使是出生时伴有严重脑积水的先天性弓形虫病患儿,只要在出生后尽早开始抗寄生虫治疗并植入脑室-腹腔分流管,仍然可以获得相对良好的神经发育结局。这一发现改变了人们对先天性弓形虫病预后的传统认识,强调了早期诊断和治疗的重要性。法国是最早实施孕期弓形虫病系统筛查的国家之一。自1970年代起,法国规定所有孕妇在孕早期必须接受弓形虫血清学检测,血清阴性者需在孕期每月重复检测。一旦发现血清阳转,立即开始螺旋霉素治疗,以减少胎盘传播风险。研究显示,孕期治疗可将先天性感染风险降低约60%。然而,美国等国家并未采纳这一筛查策略,主要原因是成本效益争议和缺乏高质量证据证明治疗的实际效果。2024年的一项分析估计,美国每年约有4400名婴儿出生时患有先天性弓形虫病,其中大多数未被诊断。
眼睛里的风暴
除了先天性感染,弓形虫还可以在免疫功能正常的成年人中引起眼部疾病。眼弓形虫病是全球感染性后葡萄膜炎的首要原因,可在原发感染多年后突然发作。其典型表现为局灶性坏死性视网膜脉络膜炎,眼底检查可见边界模糊的黄白色病灶,常伴有玻璃体炎。患者主诉视力下降、飞蚊症和视野缺损。眼弓形虫病的发病机制尚不完全清楚。一种理论认为,当组织囊在大脑或视网膜中破裂时,缓殖子释放并转化为速殖子,引发局部炎症反应。另一种理论认为,眼弓形虫病可能是免疫介导的反应,而非直接的寄生虫感染。无论机制如何,眼弓形虫病的复发率很高。约四分之一的患者在首次发作后会经历至少一次复发,每次复发都可能造成新的视网膜损害。反复发作可导致严重的视力丧失,约四分之一的患者最终一眼视力低于20/200。治疗眼弓形虫病需要在控制感染和保护视力之间取得平衡。经典的治疗方案是乙胺嘧啶联合磺胺嘧啶,辅以叶酸预防骨髓毒性。对于威胁黄斑或视神经的病变,常联合使用糖皮质激素以减轻炎症反应。近年来,新型药物如阿托伐醌和克林霉素也显示出良好疗效。
治疗的困境
弓形虫病的治疗面临一个根本性的困境:现有药物只能杀灭速殖子,而对缓殖子和组织囊几乎无效。这意味着急性感染可以被控制,但慢性感染无法根治。一旦弓形虫组织囊在大脑中形成,它们将伴随宿主终生。乙胺嘧啶联合磺胺嘧啶是目前治疗急性弓形虫病的金标准方案。这两种药物通过序贯抑制叶酸代谢途径中的不同酶——乙胺嘧啶抑制二氢叶酸还原酶,磺胺嘧啶抑制二氢蝶酸合成酶——协同发挥杀虫作用。然而,这一方案存在明显的局限性。首先,两种药物都可能引起严重的副作用,包括骨髓抑制、皮疹和肝肾功能损害。其次,疗程较长,通常需要数周至数月。最重要的是,这一方案对缓殖子无效,停药后组织囊仍可能重新激活。螺旋霉素是另一种常用的抗弓形虫药物,主要用于孕期预防先天性传播。它能够浓集于胎盘,减少寄生虫向胎儿的传播,但对已经发生的胎儿感染疗效有限。对于免疫功能低下患者的弓形虫脑炎,治疗更为复杂。除了急性期的抗寄生虫治疗外,还需要长期维持治疗以预防复发。直到免疫系统功能恢复之前,患者可能需要终身服药。寻找能够清除组织囊的药物是当前弓形虫研究的重要方向之一。2019年,研究者发现一种名为瓜纳苯泽尔的药物在小鼠模型中能够有效清除大脑中的弓形虫组织囊。这种药物似乎通过靶向缓殖子独特的代谢途径发挥作用。然而,从动物模型到临床应用仍有漫长的道路。
古老的幽灵
弓形虫与人类的纠葛远比我们想象的更加久远。古埃及DNA研究显示,在距今数千年的人类木乃伊中已经能够检测到弓形虫的痕迹。这一发现提示,弓形虫感染在人类历史上的存在可能早于文字记载。在古埃及,猫被崇拜为神圣动物,大量的猫木乃伊和猫神雕像见证了这一独特的人猫关系。有人甚至推测,古埃及人对猫的痴迷可能部分源于弓形虫感染导致的行为改变——当然,这只是一个无法证实的有趣假说。弓形虫在全球的分布极不均匀。非洲大陆的平均感染率最高,约61%;法国和巴西等国家的感染率可达60%至80%;而美国和英国的感染率相对较低,约15%至30%;中国的感染率约为10%。这些差异可能与饮食习惯、卫生条件、气候因素和猫的饲养方式等多种因素相关。食用生肉或未煮熟的肉类是弓形虫感染的主要途径之一。猪和羊是弓形虫组织囊的主要动物宿主,它们的肉类中常含有活性的缓殖子。相反,牛似乎是弓形虫的"终点宿主"——寄生虫在牛体内可以存活但难以形成组织囊,因此牛肉的传播风险相对较低。水源污染是另一个重要的传播途径。1995年,加拿大不列颠哥伦比亚省发生了一起大规模弓形虫病爆发,超过100人感染,追踪调查发现污染源是一个被猫粪污染的蓄水池。这是首次确认的水源性弓形虫病爆发,揭示了城市供水系统的潜在脆弱性。
未解之谜
尽管一个多世纪的研究,弓形虫仍有许多谜团等待解开。缓殖子如何在组织囊中存活数十年而不被免疫系统清除?它们是如何感知宿主免疫状态的变化并决定重新激活的?弓形虫究竟如何在分子层面操控宿主行为?组织囊在大脑中的长期存在会对神经功能产生什么影响?这些问题不仅具有科学意义,也关系到数十亿感染者的健康。一个更深层的问题是:弓形虫感染是否真的是一种"疾病"?约90%的感染者终身无症状,寄生虫与宿主似乎达成了某种共生状态。从进化角度看,弓形虫可能是人类微生物组的一部分,而非纯粹的病原体。有研究者甚至推测,弓形虫感染可能带来某些未知的益处——例如增强免疫反应或提供某种神经保护作用。当然,对于先天性感染患者和免疫功能低下者而言,弓形虫无疑是致命的威胁。无论如何,弓形虫这个微型操控者的存在提醒我们:在这个星球上,人类并非唯一的行为主体。微生物世界中的无数生命,正在以我们难以想象的方式,参与塑造着我们的身体、大脑和行为。当我们凝视一只猫的眼睛时,也许应该想一想:是谁在凝视着谁?
参考资料
-
Nicolle C, Manceaux L. Sur une infection à corps de Leishman (ou organismes voisins) du gondi. Comptes Rendus de l’Académie des Sciences. 1908;147:763-766.
-
Splendore A. Un nuovo protozoa parassita de conigli. Revista da Sociedade Scientifica de Sao Paulo. 1908;3:109-112.
-
Wolf A, Cowen D, Paige B. Human toxoplasmosis: occurrence in infants as an encephalomyelitis verification by transmission to animals. Science. 1939;89(2306):226-227.
-
Hutchison WM, et al. The life cycle of the coccidian parasite, Toxoplasma gondii, in the domestic cat. Transactions of the Royal Society of Tropical Medicine and Hygiene. 1971;65(3):380-399.
-
Berdoy M, Webster JP, Macdonald DW. Fatal attraction in rats infected with Toxoplasma gondii. Proceedings of the Royal Society B. 2000;267(1452):1591-1594.
-
Flegr J. Effects of Toxoplasma on human behavior. Schizophrenia Bulletin. 2007;33(3):757-760.
-
Torrey EF, Yolken RH. Toxoplasma gondii and schizophrenia. Emerging Infectious Diseases. 2003;9(11):1375-1380.
-
Prandota J. The importance of Toxoplasma gondii infection in diseases presenting with headaches. Headache and “important” protection from headaches. International Journal of Neuroscience. 2009;119(12):2144-2182.
-
Flegr J, et al. Increased risk of traffic accidents in subjects with latent toxoplasmosis. BMC Infectious Diseases. 2002;2:11.
-
Stroebel C, et al. Risky business: linking Toxoplasma gondii infection and entrepreneurship behaviours across individuals and countries. Proceedings of the Royal Society B. 2018;285(1883):20180822.
-
Montoya JG, Liesenfeld O. Toxoplasmosis. Lancet. 2004;363(9425):1965-1976.
-
Dubey JP. History of the discovery of the life cycle of Toxoplasma gondii. International Journal for Parasitology. 2009;39(8):877-882.
-
Webster JP, McConkey GA. Toxoplasma gondii-altered host behaviour: clues as to mechanism of action. Folia Parasitologica. 2010;57(2):95-104.
-
Carruthers VB, Sibley LD. Sequential protein secretion from three distinct organelles of Toxoplasma gondii accompanies invasion of human fibroblasts. European Journal of Cell Biology. 1997;73(2):114-123.
-
Attias M, et al. The life-cycle of Toxoplasma gondii reviewed using animations. Parasites & Vectors. 2020;13(1):588.
-
Ferguson DJP, et al. The development of the macrogamete and oocyst wall in Toxoplasma gondii: an ultrastructural and cytochemical study. Parasitology. 1975;70(1):75-86.
-
Sabin AB, Feldman HA. Dyes as microchemical indicators of a new immunity phenomenon affecting a protozoon parasite (Toxoplasma). Science. 1948;108(2815):660-663.
-
Gazzinelli RT, et al. In the absence of endogenous IL-10, mice acutely infected with Toxoplasma gondii succumb to a lethal immune response dependent on CD4+ T cells and accompanied by overproduction of IL-12, IFN-γ and TNF-α. Journal of Immunology. 1996;157(2):798-805.
-
Boyle JP, Radke JR. A history of studies that examine the host-parasite relationship between Toxoplasma gondii and its intermediate host. Journal of Eukaryotic Microbiology. 2009;56(2):144-151.
-
Blader IJ, Sibley LD. Toxoplasma gondii: An evolving model of intracellular parasitism. Current Opinion in Microbiology. 2002;5(4):402-406.