天堂坠落
1999年8月末的纽约,空气中弥漫着那个夏天特有的闷热与躁动。在布朗克斯动物园,首席病理学家特蕾西·麦克纳马拉正经历着职业生涯中最诡异的时刻。动物园的地面开始出现死去的乌鸦——不是一只,而是成群。更令人不安的是,这些鸟类的死亡方式极不寻常:它们无法飞翔,身体颤抖,平衡尽失,仿佛大脑被某种看不见的力量摧毁。

麦克纳马拉打开第一只乌鸦的头骨时,她看到了让她脊背发凉的景象:脑组织布满出血点,心脏上散布着神秘的病变。这是某种致命的病原体,但它不属于任何已知的疾病。与此同时,在皇后区法拉盛医院,传染病专家德博拉·阿斯尼斯医生也在面对一个无法解释的谜团:两位老年患者因不明原因的脑炎濒临死亡,所有常规检测都显示阴性。
这两位女性即将共同揭开一个震惊世界的真相:一种从未在西半球出现过的致命病毒,已经悄然入侵美国人口最密集的城市。而这仅仅是开始——在接下来的二十五年里,这个名为西尼罗河病毒的隐形杀手将在美国造成超过三千人死亡,感染数百万人,并彻底改写人类对蚊媒传染病的认知。
来自尼罗河的幽灵
西尼罗河病毒的故事始于1937年的非洲腹地。在那一年,一位发热的妇女走进乌干达西尼罗河地区的一家医院。她的症状模糊不清——头痛、发热、肌肉酸痛——这本是热带地区最常见的抱怨。但医生们从她的血液中分离出了一种前所未见的病毒。他们以发现地将其命名为西尼罗河病毒。
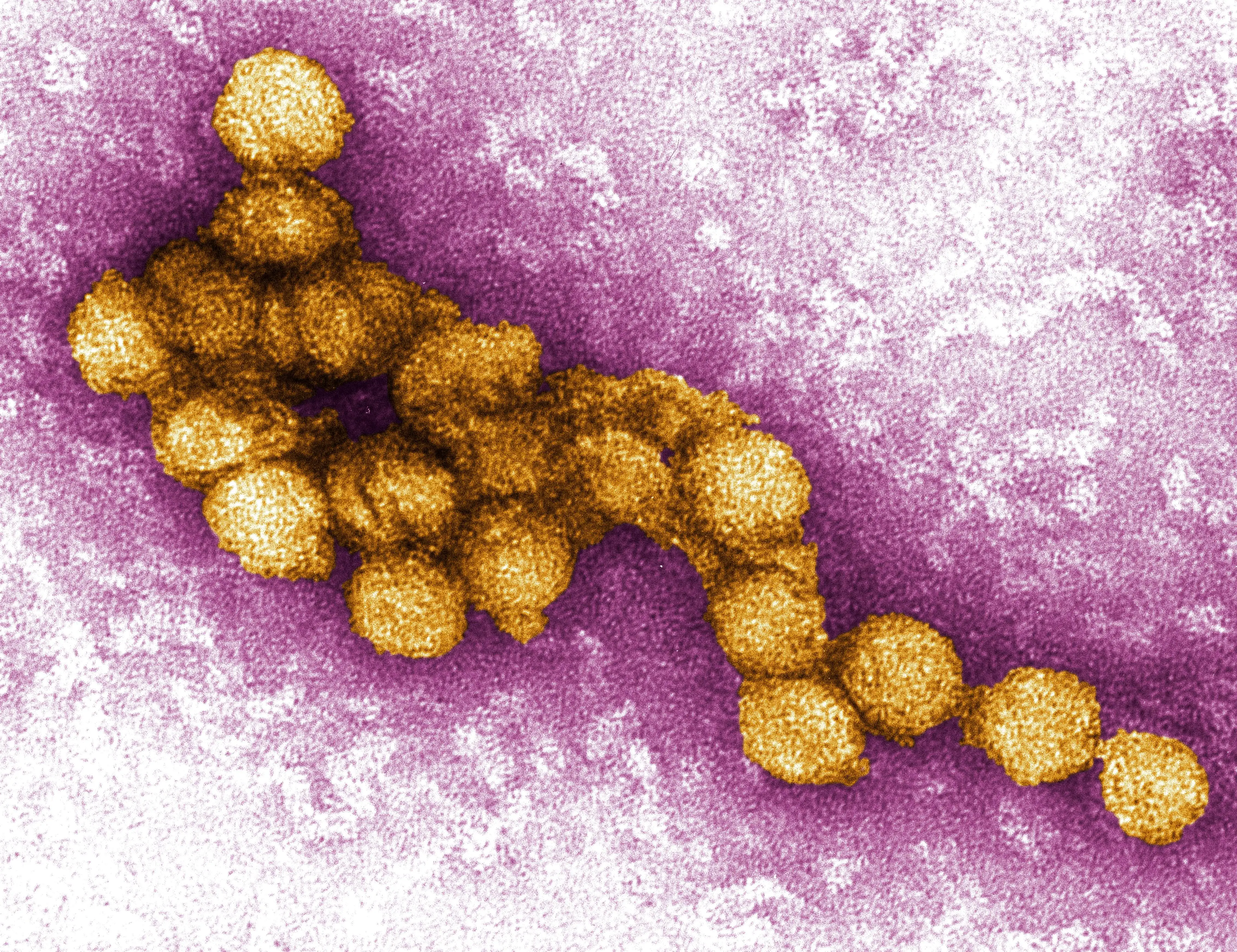
这个病毒的真正可怕之处,在于它的低调与耐心。在随后的几十年里,它在非洲、中东和欧洲悄然传播,感染了数以百万计的人,却很少有人因此死亡。在埃及尼罗河三角洲,约40%的成年人口在一生中曾被感染,大多数人在童年时期经历了一场类似流感的疾病后便获得了免疫力。病毒与人类之间似乎达成了某种微妙的平衡。
然而,这种平衡在1990年代开始破裂。1996年,罗马尼亚布加勒斯特爆发了一场规模空前的西尼罗河病毒脑炎疫情。超过800人出现神经系统症状,393人被确诊感染,17人死亡。这是人类历史上首次大规模的西尼罗河病毒脑炎爆发,也是科学家们第一次意识到,这个古老的病毒正在发生某种变化。
病毒的基因组揭示了一个令人不安的真相:西尼罗河病毒正在进化。它的包膜蛋白——病毒入侵细胞的关键武器——正在积累突变,使其更具攻击性。科学家们将病毒分为两个谱系:谱系1与人类疾病的爆发相关,谱系2则主要在非洲引起地方性感染。但到了1990年代末,谱系1的病毒开始在欧洲和西亚引发越来越严重的疫情。
1998年,以色列爆发了一场鸟类西尼罗河病毒疫情。科学家后来发现,1999年在纽约出现的病毒株与以色列1998年的病毒株基因序列最为接近。这暗示着病毒是如何跨越半个地球的:可能是一只被走私的宠物鸟,或是一只藏匿在飞机货舱中的感染蚊子,携带病毒从中东飞越大西洋,降落在人口稠密的纽约。
病毒的分子战争机器
要理解西尼罗河病毒为何如此致命,我们需要深入它的分子世界。这是一个完美的生物武器,由自然选择在数百万年中精心雕琢而成。
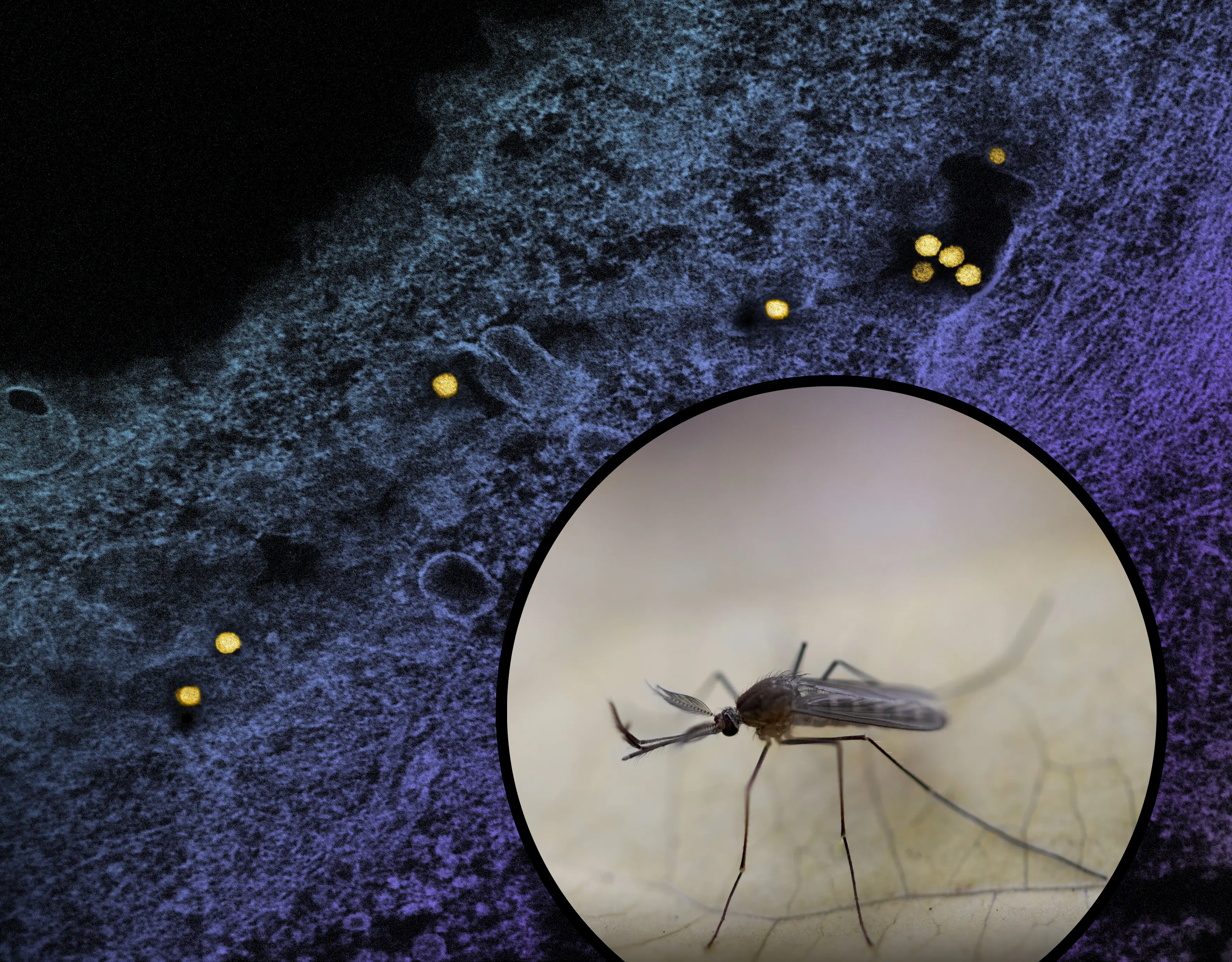
西尼罗河病毒属于黄病毒科,与登革热病毒、黄热病病毒、日本脑炎病毒和寨卡病毒是近亲。它的基因组极其精简:一条约11,000个碱基的单链RNA,仅编码一个多聚蛋白。这个多聚蛋白会被切割成10个成熟的病毒蛋白:3个结构蛋白和7个非结构蛋白。
病毒颗粒直径仅约50纳米,比人类头发丝的直径还小一千倍。在电子显微镜下,它呈现出完美的球形,表面覆盖着规则的棘突——这些是病毒的包膜蛋白(E蛋白),它们像钥匙一样精确地匹配宿主细胞表面的受体。当病毒接近细胞时,E蛋白会像弹簧刀一样弹开,插入细胞膜,启动感染过程。
病毒的入侵策略堪称艺术。它首先感染皮肤中的树突状细胞和巨噬细胞——这些本是人体免疫系统的前线哨兵。但病毒巧妙地将它们变成了自己的运输工具。感染后的免疫细胞会携带病毒进入淋巴系统,在那里病毒开始疯狂复制。短短几天内,数十亿病毒颗粒涌入血液循环。
对于大多数人来说,故事到此结束。免疫系统识别入侵者,产生抗体,清除病毒,整个过程可能只是一场轻微的发热。但对于少数不幸者——大约每150名感染者中有1人——病毒将发起最后的致命进攻:入侵中枢神经系统。
突破最后的堡垒
血脑屏障是人体最后的防御工事。这道由内皮细胞、星形胶质细胞和周细胞组成的屏障,将脆弱的脑组织与血液中的有害物质隔绝开来。它的紧密连接如同城墙上的城垛,阻挡着几乎所有病原体的入侵。
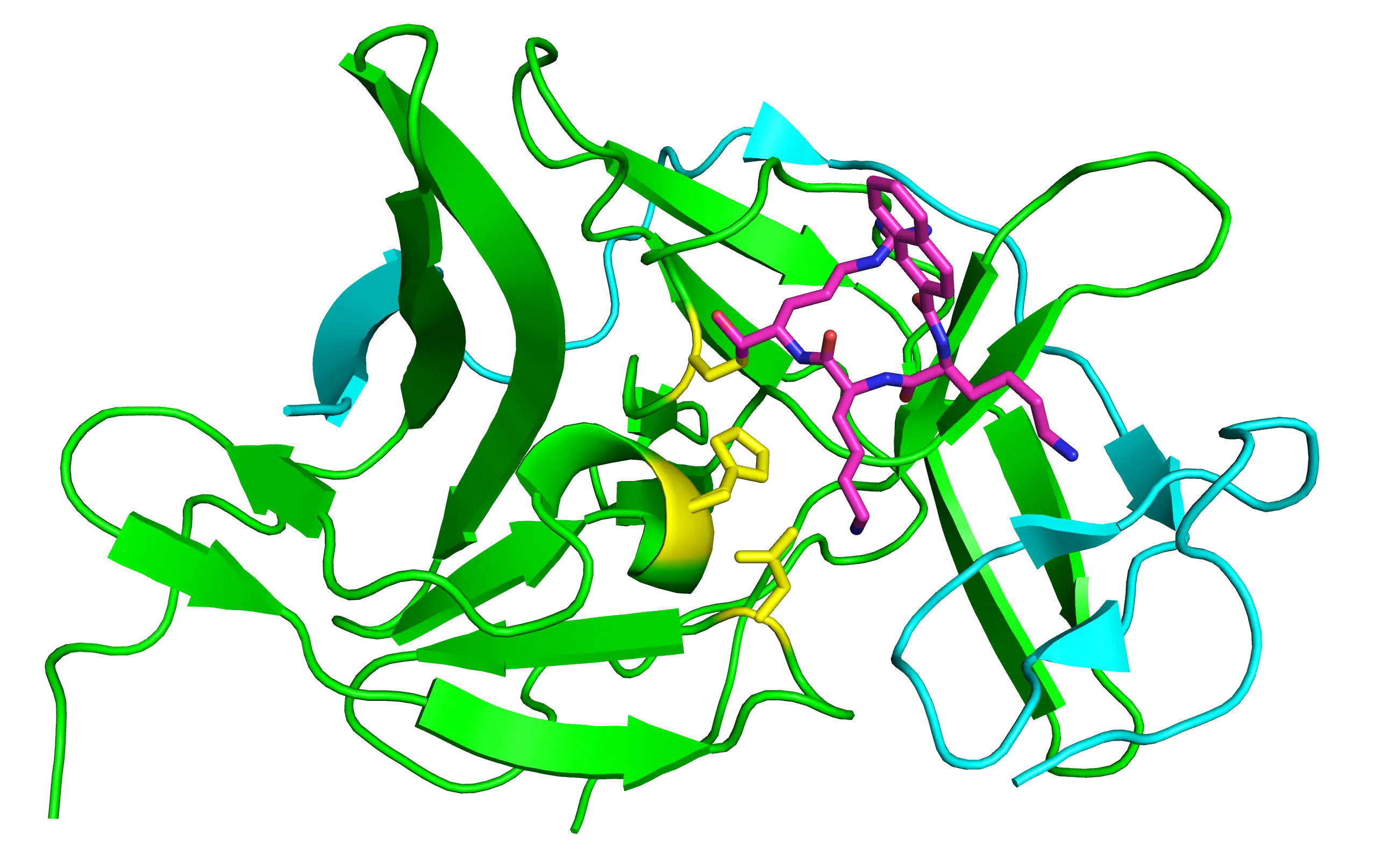
西尼罗河病毒却找到了突破这道堡垒的方法。科学家们至今仍在争论病毒是如何进入大脑的,但有几种可能的机制正在浮出水面。
第一种假说涉及"特洛伊木马"战术。病毒可以感染外周血中的单核细胞和T淋巴细胞。这些感染的白细胞能够穿过血脑屏障进入脑组织,病毒随之进入中枢神经系统。研究显示,西尼罗河病毒感染后,大脑中确实可以检测到携带病毒抗原的淋巴细胞。
第二种假说更为直接:病毒可能通过感染脑血管内皮细胞,直接穿过血脑屏障。在实验室培养的内皮细胞模型中,病毒颗粒可以在感染后数天内从细胞的一侧移动到另一侧,而不破坏细胞的完整性。这种跨细胞运输似乎涉及内吞囊泡——病毒被包裹在细胞膜形成的囊泡中,像乘坐电梯一样从血管腔侧到达脑实质侧。
第三种假说则涉及嗅觉神经。在动物实验中,病毒可以在感染后最早出现在嗅球——大脑处理嗅觉的区域。这暗示病毒可能通过感染鼻腔中的嗅觉神经元,沿着神经纤维逆行进入大脑。这种神经入侵途径在狂犬病病毒中已被证实,而西尼罗河病毒可能使用了类似的策略。
无论通过哪种途径,一旦病毒进入大脑,真正的灾难便开始了。神经元是病毒的主要靶标,尤其是脑干和脊髓前角中的运动神经元。病毒感染导致神经元大规模死亡,同时引发剧烈的炎症反应。大脑充血肿胀,颅骨内压力急剧升高。患者可能出现剧烈头痛、意识混乱、癫痫发作,最终陷入昏迷。
像脊髓灰质炎一样的瘫痪
西尼罗河病毒最令人恐惧的表现,是它能造成类似脊髓灰质炎的急性弛缓性瘫痪。2002年,密西西比州的医生们首次报告了这一令人震惊的现象:感染西尼罗河病毒的患者出现单侧或双侧肢体无力,肌肉反射消失,而感觉功能却保持完好。这些症状与脊髓灰质炎惊人地相似。
进一步的研究揭示了真相:西尼罗河病毒特异的攻击脊髓前角的运动神经元——正是脊髓灰质炎病毒靶向的同一群细胞。这些神经元负责将运动指令从大脑传递到肌肉,一旦被摧毁,患者就会失去对相应肢体的控制。
2005年夏天,59岁的约翰·肖在德克萨斯州经历了这场噩梦。在被蚊子叮咬几天后,他突然发现自己无法站立。“我当时正在穿短裤,然后就倒下了,“他后来回忆道,“我几乎走不了路,站不起来。我只能用手和膝盖爬下楼梯。”
肖在重症监护室度过了两周,他的大脑和神经系统遭受严重炎症。虽然他最终幸存下来,但他的双腿至今瘫痪。七年后的2012年,当CBS新闻采访他时,他仍然只能坐在轮椅上。当被问及最想念什么时,他简单地回答:“散步。”
研究表明,约三分之一出现严重西尼罗河病毒症状的患者会有长期后遗症:疲劳、视力模糊、认知障碍、肾脏疾病和瘫痪。更令人不安的是,科学家发现病毒可能在部分患者体内持续存在数年,造成慢性损害。这与教科书上关于西尼罗河病毒"急性感染后迅速清除"的传统认知完全相悖。
生态链中的死亡传递
西尼罗河病毒之所以能在北美迅速扎根,关键在于它找到了完美的生态位。这是一个关于蚊子、鸟类和人类的三重奏,每一个参与者都在无意中推动了病毒的传播。
病毒的主要传播媒介是库蚊,特别是尖音库蚊。这种蚊子在全球各地都能找到,它们喜欢在污水中繁殖——城市的排水沟、废弃轮胎积水、鸟浴盆都是它们的乐园。在纽约,它们被称为"家蚊”,因为它们常常在夜间飞入住宅寻找血液大餐。
鸟类是病毒的天然储存宿主。当一只感染的蚊子叮咬鸟类时,病毒进入鸟体内开始疯狂复制。在短短几天内,鸟类血液中的病毒载量可以达到天文数字——每毫升血液中可能含有数亿个病毒颗粒。这只鸟变成了一个病毒工厂,任何叮咬它的蚊子都会被感染。
然而,并非所有鸟类都是平等的病毒放大器。美国的研究发现,知更鸟、蓝松鸦和家雀是特别高效的病毒繁殖者。而乌鸦和渡鸦则更加悲惨——它们对病毒高度敏感,感染后几乎必定死亡。1999年纽约爆发的第一个预警信号,正是从天空坠落的乌鸦。
人类和马匹在这个生态链条中是"死端宿主”——我们体内的病毒载量通常不足以感染叮咬我们的蚊子。我们只是无辜的旁观者,偶然被卷入这场蚊子与鸟类之间的战争。但对于那些不幸发展出神经系统并发症的人来说,这场"旁观"可能是致命的。
纽约之战
1999年9月初,纽约市卫生部门接到了令人不安的报告:皇后区的医院在短短一个周末内收治了8例脑炎患者——而整个纽约市正常情况下全年只有约9例脑炎。更令人担忧的是,这些患者的症状异常严重,多人出现瘫痪。
美国疾病控制与预防中心(CDC)最初将诊断锁定为圣路易斯脑炎病毒——一种在美国中西部和南部已知的蚊媒病毒。但这个诊断存在问题:圣路易斯脑炎病毒在纽约从未出现过,而且它通常不会导致鸟类死亡。
与此同时,麦克纳马拉在布朗克斯动物园的发现越来越令人不安。她解剖了动物园死亡的鸟类——火烈鸟、鸬鹚、甚至一只国鸟白头海雕——它们都显示出相同的脑出血和心脏病变。她确信这些鸟类的死亡与人类的疾病有关,但她无法说服CDC的科学家。当时的CDC专注于圣路易斯脑炎,拒绝考虑其他可能性。
麦克纳马拉没有放弃。她将组织样本送到了爱荷华州的美国国家兽医服务实验室。那里的科学家成功培养了病毒,发现它与圣路易斯脑炎病毒相似但不完全相同。麦克纳马拉以此说服CDC对病毒进行基因测序。
1999年9月22日,CDC的研究人员震惊地发现:杀死纽约鸟类和人类的不是圣路易斯脑炎病毒,而是西尼罗河病毒——一种从未在西半球出现过的病原体。两天后,独立于CDC工作的加州大学欧文分校科学家伊恩·利普金也确认了这一发现。
消息传出后,纽约市迅速启动了大规模灭蚊行动。直升机在城市上空喷洒杀虫剂,市政部门分发了数百万瓶驱蚊剂。但这些措施为时已晚——病毒已经扎根。
1999年的爆发最终导致59人住院,7人死亡。但这只是前奏。病毒随着候鸟的迁徙向南传播,在接下来的几年里席卷整个美国大陆。到2003年,病毒已经传播到西海岸,完成了对北美大陆的征服。
最致命的一年
2012年,西尼罗河病毒在美国制造了有记录以来最致命的一年。CDC报告了5674例病例,其中51%为神经侵袭性疾病——这意味着病毒入侵了患者的中枢神经系统。这是美国历史上由虫媒病毒引起的神经侵袭性疾病病例最多的一年。
德克萨斯州成为重灾区。在达拉斯县,官员们目睹了一场前所未有的灾难:225例西尼罗热病例,173例神经侵袭性疾病病例,19人死亡。整个州报告了1868例病例和89例死亡。
这场爆发的严重程度引发了科学家们的反思。为什么2012年如此糟糕?答案指向了气候。那一年,美国经历了异常温和的冬季和异常潮湿的春季——这是蚊子繁殖的完美条件。更温暖的气温不仅加速了蚊子的繁殖周期,也加快了病毒在蚊子体内的复制速度。
研究表明,西尼罗河病毒在蚊子体内的复制速度与温度密切相关。在较温暖的温度下,病毒可以在更短的时间内达到足以传播的载量。这意味着蚊子在死亡前可以感染更多的鸟类和人类。气候变暖正在为这个古老的杀手提供更广阔的舞台。
一个病毒的进化
西尼罗河病毒并非静止不变。自1999年进入美国以来,它一直在进化。科学家们通过基因测序追踪了病毒的演变轨迹,发现了一个令人担忧的趋势:北美西尼罗河病毒的毒力似乎在增强。

2002年,科学家发现了一种新的病毒变异。这种变异使病毒能够更有效地复制,可能导致更严重的疾病。与此同时,病毒也在不断适应新的宿主。在北美,病毒遇到了超过150种鸟类宿主和62种蚊子媒介——这是它在非洲老家从未遇到过的多样性。
病毒的进化还体现在它的传播模式上。除了蚊子叮咬,病毒还可以通过输血、器官移植、母婴传播和实验室暴露传播。2002年,美国首次报告了通过输血传播西尼罗河病毒的病例。这促使美国对所有捐献血液进行西尼罗河病毒筛查,这一措施至今仍在执行。
医学界的困境
二十五年过去了,人类在西尼罗河病毒面前仍然束手无策。目前没有针对西尼罗河病毒的有效抗病毒药物,也没有可供人类使用的疫苗。马匹疫苗早在十多年前就已问世,但对于人类疫苗的开发,制药公司却兴趣寥寥——原因很简单:市场不够大。
西尼罗河病毒感染的大多数病例是亚临床的,这意味着大多数人感染后没有任何症状。即使出现症状,大多数人经历的也只是一场类似流感的发热。只有极少数人会发展成严重的神经系统疾病。从商业角度看,开发一种针对如此"罕见"并发症的疫苗,投资回报率实在太低。
但这并不意味着科学家们停止了努力。目前,几种有希望的治疗方法正在研究中。单克隆抗体——实验室制造的可识别并中和病毒的蛋白质——已在动物实验中显示出良好效果。一些科学家也在探索使用已批准的药物进行"药物重定位",寻找可以抑制西尼罗河病毒复制的现有药物。
气候变化的隐形遗产
西尼罗河病毒在北美的成功,为人类提供了一个关于气候变化如何重塑疾病版图的生动教材。科学家们预计,随着全球气温继续上升,西尼罗河病毒的传播范围将进一步扩大。
温度不是唯一的因素。降水模式的变化也在影响着蚊子的繁殖。极端天气事件——如暴雨和洪水——可以创造出蚊子繁殖的理想环境。与此同时,干旱也可能通过迫使鸟类聚集在有限的水源附近,促进病毒在鸟类之间的传播。
模型预测显示,到2050年,西尼罗河病毒可能在美国更北部和更高海拔的地区流行。在欧洲,病毒已经在多个国家扎根,从意大利到希腊,从西班牙到匈牙利,病例逐年增加。气候变化正在将这个古老的杀手带到它从未到达过的地方。
永恒的共存
西尼罗河病毒的故事,是人类与传染病永恒斗争的一个缩影。从1937年乌干达的一位发热妇女,到1999年纽约动物园坠落的乌鸦,再到今天全球数百万人携带的抗体,这个病毒已经在我们的世界中扎根。
它提醒我们,病原体没有国界,生态系统的微小变化可能产生深远的公共卫生后果。它也提醒我们,科学发现往往需要跨学科的合作——兽医病理学家、传染病医生、分子生物学家和公共卫生官员必须共同工作,才能拼凑出疾病的完整图景。
在布朗克斯动物园,特蕾西·麦克纳马拉的发现改变了流行病学的历史。她的执着和跨学科视野——将动物疾病与人类健康联系起来——催生了"全健康"的理念,这一理念今天已成为全球公共卫生的核心原则。
西尼罗河病毒不会消失。它已经成为北美生态系统的一部分,在蚊子、鸟类和人类之间循环往复。每个夏天,当蚊子从冬眠中苏醒,病毒便开始了新一轮的传播。我们能做的,是保持警惕,改善监测,投资研究,并记住这个教训:下一个新出现的传染病,可能就藏在一只坠落的鸟儿身上。
参考资料
-
Nash D, Mostashari F, Fine A, et al. The Outbreak of West Nile Virus Infection in the New York City Area in 1999. New England Journal of Medicine. 2001;344(24):1807-1814.
-
Hayes EB, Komar N, Nasci RS, et al. Epidemiology and Transmission Dynamics of West Nile Virus Disease. Emerging Infectious Diseases. 2005;11(8):1167-1173.
-
Colpitts TM, Conway MJ, Montgomery RR, Fikrig E. West Nile Virus: Biology, Transmission, and Human Infection. Clinical Microbiology Reviews. 2012;25(4):635-648.
-
Beasley DW. Antigenic Structure of the West Nile Virus Envelope Protein. Virology. 2011;416(1-2):119-120.
-
Diamond MS, Shrestha B, Marri A, et al. B Cells and Antibody Play Critical Roles in the Immediate Defense of Disseminated Infection by West Nile Encephalitis Virus. Journal of Virology. 2003;77(4):2578-2586.
-
Lanciotti RS, Roehrig JT, Deubel V, et al. Origin of the West Nile Virus Responsible for an Outbreak of Encephalitis in the Northeastern United States. Science. 1999;286(5448):2333-2337.
-
Murray KO, Walker C, Herrington E, et al. Risk Factors for Encephalitis and Death from West Nile Virus Infection. Epidemiology and Infection. 2012;140(6):1106-1113.
-
Sejvar JJ, Haddad MB, Tierney BC, et al. Neurologic Manifestations and Outcome of West Nile Virus Infection. JAMA. 2003;290(4):511-515.
-
Soverow J, Wellenius GA, Fisman DN, Mittleman MA. Infectious Disease in a Warming World: How Weather Influenced West Nile Virus in the United States. Environmental Health Perspectives. 2009;117(7):1049-1052.
-
Petersen LR, Brault AC, Nasci RS. West Nile Virus: Review of the Literature. Journal of the American Medical Association. 2013;310(3):308-315.