1958年的哥本哈根,一位名叫普雷本·冯·马格努斯的丹麦病毒学家正在他位于国家血清研究所的实验室里忙碌。这一年,他从新加坡进口的一批食蟹猴身上发现了一种奇怪的疾病——这些猴子出现了类似天花的症状,皮肤上布满了充满液体的疱疹,有些甚至不治身亡。冯·马格努斯用电子显微镜观察了这些疱疹中的病毒颗粒,他看到的画面令他震惊:在显微镜下,这些病毒颗粒呈现出独特的砖块形状,与天花病毒惊人相似,却又有着微妙的差异。他将这种病毒命名为"猴痘病毒",无意间揭开了人类与一种古老病原体之间漫长博弈的序幕。
那时的冯·马格努斯并不知道,他所发现的病毒实际上并不是猴子的疾病——猴子只是偶然的受害者,就像人类一样。这种病毒的真正宿主藏在非洲大陆深邃的雨林之中,在啮齿类动物的血管里静静繁衍了数千年,等待着被人类发现的那一天。
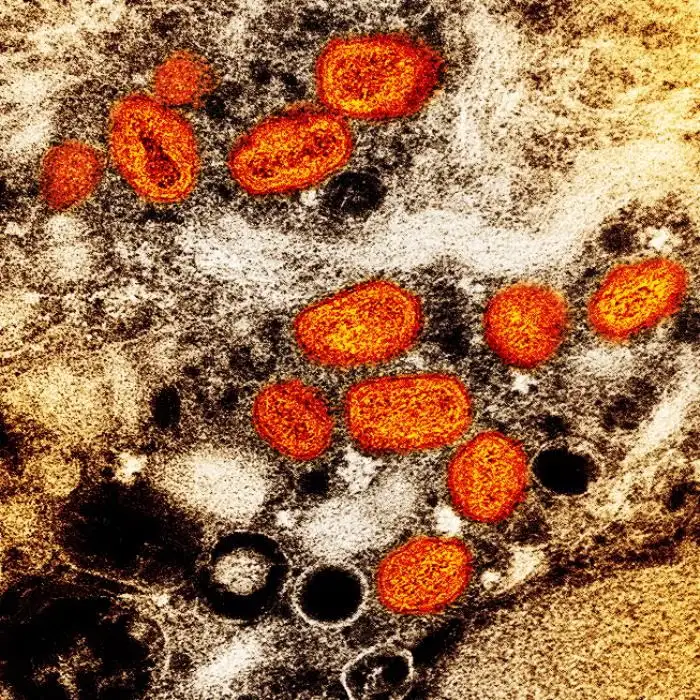
猴痘病毒属于正痘病毒属,这个家族中最著名的成员是天花病毒——人类历史上最致命的杀手之一。天花在二十世纪夺走了约三亿人的生命,直到1980年被世界卫生组织宣布彻底根除。猴痘病毒与天花病毒的基因组相似度高达96%,这意味着它们共享着大部分的基因组成,也意味着它们能够引起相似的临床症状。但这种相似性也带来了一个意想不到的后果:当天花疫苗在全球范围内停止接种后,人类对正痘病毒的群体免疫屏障也随之瓦解,为猴痘病毒的传播打开了大门。
猴痘病毒的结构堪称病毒界最复杂的典范。在电子显微镜下,它呈现出规则的砖块形状或椭圆形,长度在220至450纳米之间,宽度在140至260纳米之间。这个尺寸使它成为肉眼几乎可见的最大病毒之一——作为对比,流感病毒的直径约为100纳米,而引发新冠疫情的SARS-CoV-2病毒直径约为120纳米。猴痘病毒的巨大体积使它能够携带更多的遗传信息:它的基因组由一条约197,000个碱基对组成的双链DNA构成,编码约190个蛋白质。这些蛋白质中,一部分负责病毒的基本生命活动——复制、转录、翻译;另一部分则负责与宿主免疫系统的复杂博弈。
病毒颗粒的核心是一个哑铃状的DNA基因组,被一层称为"栅栏层"的蛋白质结构所包围。在栅栏层的外面是两层膜——内膜和外膜,以及被称为"侧体"的蛋白质结构。病毒颗粒的最外层是脂蛋白包膜,上面布满了表面小管结构,这些结构在病毒附着和入侵宿主细胞时发挥着关键作用。猴痘病毒能够产生四种不同类型的病毒颗粒:细胞内成熟病毒(IMV)、细胞内包膜病毒(IEV)、细胞相关包膜病毒(CEV)和细胞外包膜病毒(EEV)。每种颗粒都有其独特的功能:IMV稳定性高,负责在宿主之间传播;EEV则帮助病毒在宿主体内扩散,逃避免疫系统的攻击。

猴痘病毒的复制过程是一场精密的分子战争。当病毒颗粒附着在宿主细胞表面后,它会通过膜融合的方式进入细胞质——这与大多数DNA病毒不同,它们通常需要进入细胞核才能复制。猴痘病毒携带了所有复制所需的酶,因此能够在细胞质中独立完成整个生命周期。入侵后,病毒首先释放预先包装好的早期蛋白,这些蛋白会迅速抑制宿主的防御机制。随后,病毒的RNA聚合酶开始转录早期基因,产生更多的蛋白来帮助病毒脱壳和DNA复制。当DNA复制完成后,病毒开始组装新的颗粒,最终通过细胞裂解或出芽的方式释放出去,寻找新的宿主细胞。
但猴痘病毒最令人惊叹的能力在于其对宿主免疫系统的全面压制。它携带了一系列免疫逃逸基因,这些基因编码的蛋白能够干扰宿主的每一个免疫防御环节。在干扰素途径中,病毒蛋白能够阻断干扰素的产生、结合干扰素受体、或直接降解干扰素信号分子。在补体系统中,病毒产生补体抑制蛋白,阻止补体对病毒颗粒的攻击。在炎症反应中,病毒编码的IL-1β结合蛋白能够中和这种关键的炎症因子,削弱宿主的炎症反应。更为精妙的是,猴痘病毒感染的单核细胞能够阻止T细胞的激活——这种抑制不需要主要组织相容性复合体的参与,使得病毒能够在免疫系统毫无察觉的情况下复制和传播。
猴痘病毒并非单一实体,而是分为两个遗传和临床上截然不同的进化分支:进化支I(原称刚果盆地支或中非支)和进化支II(原称西非支)。进化支I主要流行于刚果盆地地区,致病力更强,在未接种疫苗的人群中病死率可达10%。进化支II则主要发现于西非地区,致病力相对较弱,病死率通常低于1%。进化支II又进一步分为两个亚支:IIa和IIb,后者正是引发2022年全球大流行的罪魁祸首。
这两个进化支之间的差异不仅体现在致病力上,更体现在基因组层面。进化支I携带了进化支II所缺失的多个毒力基因,包括D14L(补体抑制蛋白)、B10R(凋亡调节蛋白)、B14R(IL-1β结合蛋白)和B19R(丝氨酸蛋白酶抑制剂样蛋白)。这些基因的缺失使得进化支II的致病力大幅降低,但也可能意外地增强了它的人际传播能力——有研究显示,进化支II样本中约17%发生了附属基因的缺失,这种缺失与人际传播能力的增强相关。
猴痘病毒的天然宿主至今仍是一个未解之谜。虽然病毒的名字中有"猴"字,但猴子实际上只是偶然宿主。多年的流行病学调查指向非洲的啮齿类动物——尤其是火足绳鼠,这种生活在非洲雨林中的小型啮齿动物被认为是病毒最主要的天然储存宿主。2026年发表在《自然》杂志上的研究首次证实了这一假设:研究人员在喀麦隆发现,一只死亡的火足绳鼠携带了猴痘病毒,而且病毒的基因序列与随后在同一地区白眉猴群体中爆发的猴痘疫情完全匹配。这是人类首次发现猴痘病毒从自然储存宿主直接传播给灵长类动物的证据。
1970年,在天花即将从地球表面消失的历史性时刻,另一个故事的序幕在刚果民主共和国(当时称为扎伊尔)悄然拉开。在赤道省巴萨恩苏地区的一个偏远村庄里,一名年仅九个月大的婴儿突然出现了高烧、全身淋巴结肿大和遍布全身的水疱样皮疹。当地医生最初怀疑这是天花——毕竟,这种可怕的疾病在非洲大陆仍然存在。但流行病学调查揭示了一个令人困惑的事实:这个婴儿从未离开过他居住的村庄,也没有与任何天花患者有过接触。天花疫苗的接种记录显示,这个婴儿也没有接种过疫苗——当时的天花疫苗接种年龄是1岁。
病毒样本被送往位于亚特兰大的美国疾病控制中心进行鉴定。在那里,科学家们用电子显微镜观察到了典型的正痘病毒颗粒——砖块形状,与天花病毒几乎无法区分。但进一步的实验室测试揭示了真相:这是猴痘病毒,这是人类历史上第一例有记录的人类猴痘感染病例。这个发现震惊了整个公共卫生界——在天花即将被根除之际,一个与之亲缘关系极近、能够感染人类的病毒出现了。
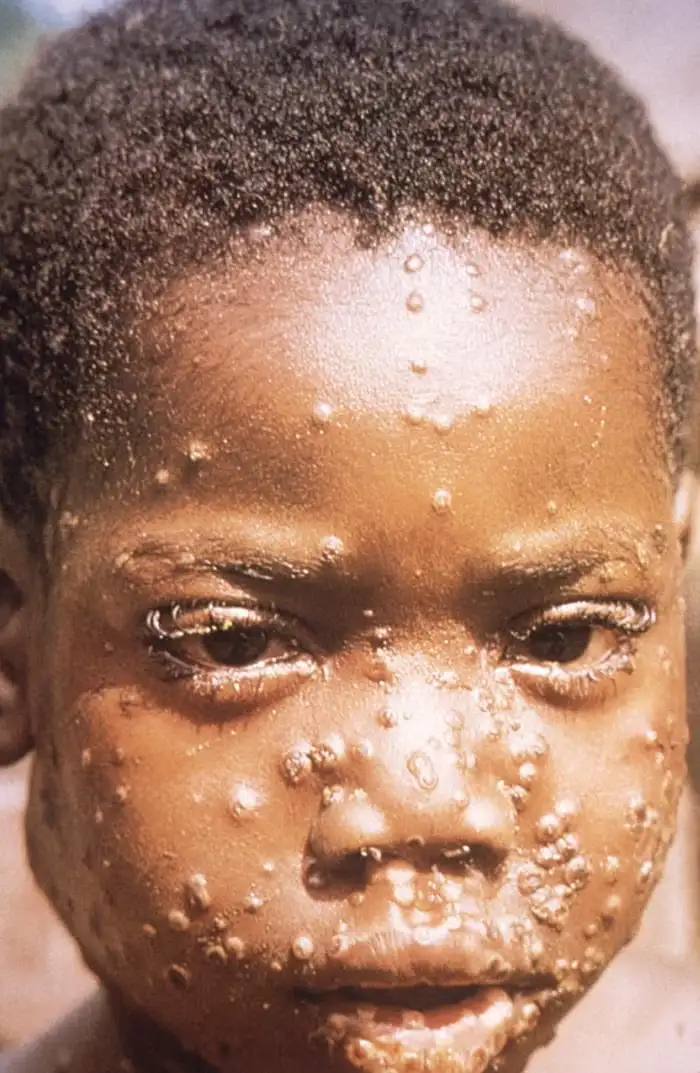
这个九个月大婴儿的命运没有被详细记录在医学文献中,但他的病例开启了一个新的时代——猴痘作为人类疾病的时代。在接下来的几年里,更多的病例在非洲大陆被陆续发现:1970年至1971年间,利比里亚、塞拉利昂和尼日利亚相继报告了人类猴痘病例。这些病例有一个共同特点:患者都是儿童,大多数生活在农村地区,与森林和野生动物有着密切接触。
世界卫生组织在1981年至1986年间在刚果民主共和国开展了一项大规模的猴痘监测研究。这项研究记录了338例人类猴痘病例,其中67%通过病毒培养确诊。研究发现,猴痘的人际传播效率远低于天花——天花的基本再生数(R0)约为5至7,而猴痘的R0估计仅为0.6至1.0。这意味着在没有持续输入的情况下,猴痘疫情会自然消退,不太可能造成大规模流行。但研究也揭示了一个令人担忧的趋势:在家庭成员中,继发感染率约为10%,表明病毒确实具有人际传播的能力。
1996年至1997年,刚果民主共和国卡塞东部地区爆发了有记录以来最大规模的猴痘疫情。在五个月的时间里,共报告了511例疑似病例。这次疫情的规模超出了所有人的预期,也引发了人们对猴痘病毒正在适应人际传播的担忧。调查发现,许多病例发生在天花疫苗接种率较低的地区,这一发现支持了停止天花疫苗接种后人群对正痘病毒免疫力下降的假设。
2003年,猴痘病毒第一次离开非洲大陆,在地球另一端的美国引发了恐慌。这场疫情可以追溯到一张从加纳运往德克萨斯州的托运单上:2003年4月9日,一批来自非洲的啮齿类动物被运抵美国,包括冈比亚巨鼠、绳鼠和睡鼠。这些动物被分销到多个州的宠物店,在运输和储存过程中,它们与当地的草原犬鼠——一种在美国家庭中作为宠物饲养的啮齿动物——混在了一起。
草原犬鼠对猴痘病毒高度易感,感染后会排出大量病毒。当这些被感染的草原犬鼠被作为宠物出售后,病毒开始向人类传播。截至2003年7月,威斯康星州、印第安纳州、伊利诺伊州、密苏里州、堪萨斯州和俄亥俄州共报告了71例确诊或疑似病例。所有患者都有与患病草原犬鼠直接接触的历史。幸运的是,没有人死亡,但这次疫情揭示了猴痘病毒跨越地理屏障的能力——只要有合适的条件和足够的疏忽,病毒可以在几天之内从非洲雨林传播到美国家庭的客厅。
这次疫情也暴露了外来宠物贸易中的巨大公共卫生漏洞。在此之前,美国对进口活体动物的监管主要关注农业安全和生态入侵风险,而非人兽共患病的传播。疫情发生后,美国食品药品监督管理局和疾病控制中心紧急禁止了来自非洲的啮齿类动物进口,并对宠物贸易实施了更严格的监管。
2022年5月6日,英国卫生安全局确认了一例猴痘病例——一名最近从尼日利亚返回的英国居民。这似乎只是又一起偶发性的输入病例,在过去几年里,类似的病例在以色列、新加坡和美国都曾发生过。但接下来的发展超出了所有人的预期。5月12日,英国报告了另外两例病例——这两例患者没有旅行史,也不清楚与首例患者有任何联系。5月17日,葡萄牙报告了5例确诊和15例疑似病例。同一天,西班牙报告了7例确诊病例。到5月底,疫情已经蔓延到美国、加拿大、澳大利亚和多个欧洲国家。
这次疫情的传播模式与以往非洲的猴痘疫情有着根本性的不同。传统上,猴痘主要通过与感染动物接触传播,人际传播有限。但在2022年的疫情中,绝大多数病例是通过人与人之间的密切接触传播的,尤其是通过性接触传播。流行病学调查显示,超过95%的病例发生在男男性行为者群体中,多数患者报告在发病前有多个性伴侣或匿名性行为。皮疹通常首先出现在生殖器和肛门周围,而非传统的面部和四肢。
病毒基因组的测序揭示了更多信息。引发这场疫情的病毒属于进化支IIb,与2018年至2019年从尼日利亚输出到英国、以色列和新加坡的病毒株高度相似。但与早期分离株相比,2022年的病毒株积累了大量的突变——约50个单核苷酸变异。这些突变中,许多发生在病毒基因组的末端区域,那里编码着病毒与宿主免疫反应相互作用的蛋白质。有科学家推测,病毒可能正在经历适应性进化,增强其人际传播的能力。
2022年7月23日,世界卫生组织宣布猴痘疫情为"国际关注的突发公共卫生事件"——这是该组织的最高级别警报。截至2022年底,全球110多个国家共报告了超过87,000例病例,超过140人死亡。这是人类历史上猴痘病毒最大规模的爆发,也是第一次在非流行地区发生如此广泛的人际传播。
疫情的应对措施面临着前所未有的挑战。由于猴痘此前被视为一种被忽视的热带病,诊断工具、治疗药物和疫苗都十分有限。唯一获批用于猴痘的疫苗是JYNNEOS(也称Imvamune或Imvanex),这是一种改良的安卡拉牛痘病毒疫苗,最初是为天花准备的。由于供应有限,各国不得不采取剂量节约策略——将标准剂量从皮下注射改为皮内注射,这样可以用五分之一的剂量产生类似的免疫反应。唯一获批的治疗药物是替考韦瑞(商品名TPOXX),这是一种通过抑制病毒包膜蛋白来阻止病毒传播的小分子药物。但临床试验显示,替考韦瑞对于轻度至中度的进化支II猴痘感染效果有限——这与动物实验中的良好效果形成了鲜明对比。
到2023年初,全球疫情开始消退。疫苗的推广、行为的改变和自然免疫的形成共同遏制了病毒的传播。2023年5月,世界卫生组织宣布猴痘不再构成国际关注的突发公共卫生事件。但这个宣告可能为时过早——在非洲大陆,另一个威胁正在酝酿。
刚果民主共和国是猴痘病毒最古老的流行区,进化支I已经在这里流行了半个世纪。但自2019年以来,这个国家的猴痘疫情出现了令人担忧的变化。病例数逐年攀升,从2020年的约4,000例增加到2023年的超过14,000例。更令人担忧的是,疫情开始向城市蔓延——传统上,猴痘主要发生在与森林接触较多的农村地区,但2023年的病例有相当一部分报告自人口密集的城市地区。
2024年初,一个新变种的出现引发了全球关注。这个被称为进化支Ib的新变种似乎具有更强的人际传播能力。与传统的进化支I不同,进化支Ib正在通过性网络传播,类似于2022年的进化支IIb。同时,进化支Ib的病死率仍然保持在较高水平——与进化支II低于1%的病死率相比,进化支I的病死率可达10%。
2024年8月14日,世界卫生组织再次宣布猴痘为国际关注的突发公共卫生事件。这是历史上第一次,猴痘病毒两次触发这一最高级别警报。截至2024年8月,刚果民主共和国已报告超过15,000例病例和超过500例死亡。疫情已经蔓延到布隆迪、卢旺达、乌干达和肯尼亚等邻国,这些国家此前从未报告过猴痘病例。
猴痘病毒的传播途径是理解这场疫情的关键。病毒可以通过直接接触感染动物的体液、病变组织或呼吸道分泌物传播;也可以通过直接接触患者的皮肤病变、体液或呼吸道飞沫传播;还可以通过接触被病毒污染的物品(如床单、衣物)间接传播。在2022年的疫情中,性接触成为主要的传播方式——病毒能够在精液和肛门拭子中检测到,尽管它是否能够通过性传播独立于皮肤接触仍存在争议。
感染后的临床表现通常分为三个阶段:潜伏期、前驱期和出疹期。潜伏期通常为7至14天,但也可能长达21天。在此期间,感染者没有症状,也不会传播病毒。前驱期持续1至3天,患者可能出现发热、头痛、肌肉疼痛、背痛和乏力。淋巴结肿大是猴痘区别于天花和其他皮疹性疾病的关键特征——肿大的淋巴结可能出现在颈部、腋下或腹股沟,可以是单侧或双侧。淋巴结肿大的存在是猴痘诊断的重要线索。
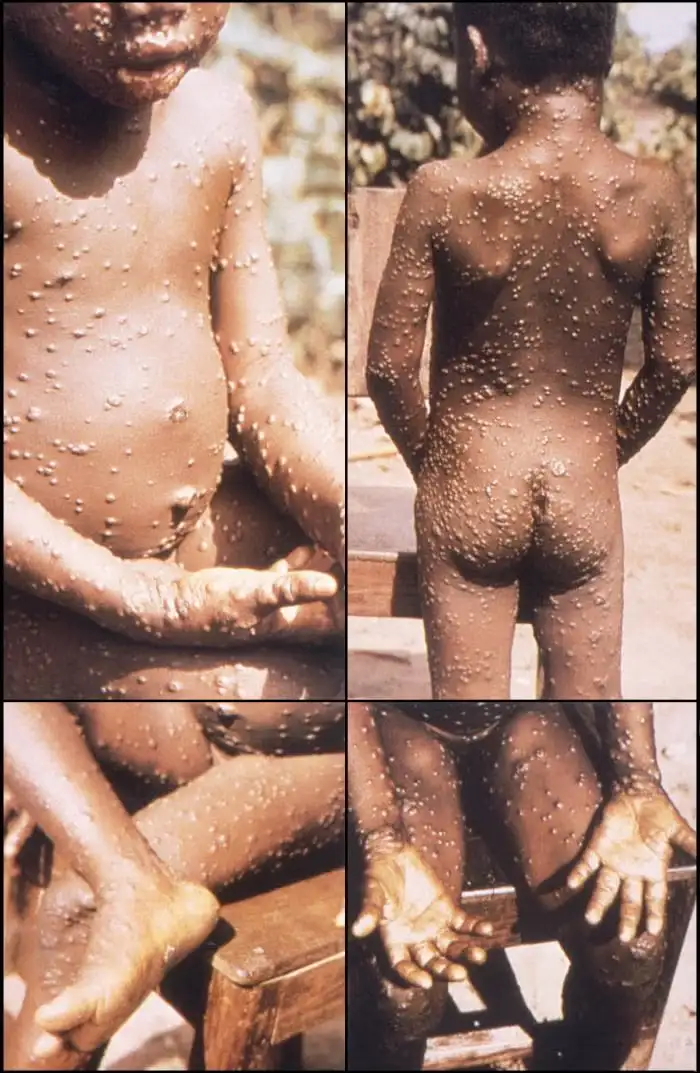
出疹期通常在前驱期开始后1至3天出现。皮疹通常首先出现在面部,然后蔓延到身体其他部位,包括手掌和脚底。皮疹的发展经历四个阶段:斑疹(平坦的红色区域)、丘疹(略微隆起的坚实皮损)、水疱(充满清亮液体的隆起皮损)和脓疱(充满浑浊或淡黄色液体的皮损)。在脓疱阶段,皮损通常中心凹陷,形成特征性的脐凹外观。最后,脓疱干燥结痂,痂皮脱落后留下可能永久存在的色素沉着或瘢痕。
在2022年的疫情中,临床表现出现了一些变化。许多患者的皮疹数量较少,有时仅限于生殖器和肛门区域。一些患者甚至没有经历典型的前驱期,皮疹成为首发症状。这些非典型的表现使得猴痘的诊断更加困难,有时会被误诊为性传播疾病如梅毒、疱疹或软下疳。
严重的猴痘感染可能导致一系列并发症,包括肺炎、脑炎、眼部感染和继发性细菌感染。儿童、孕妇和免疫功能低下者面临更高的重症和死亡风险。在2022年的疫情中,大多数死亡病例发生在免疫功能严重受损的患者中,尤其是未接受有效抗逆转录病毒治疗的晚期HIV感染者。
猴痘的诊断依赖于实验室检测。聚合酶链式反应(PCR)是确诊的金标准,通常使用来自皮损的拭子样本进行检测。血液检测和血清学检测在诊断中的价值有限,因为病毒血症通常短暂且病毒载量较低。在流行地区,临床诊断仍然重要——典型的皮疹加上淋巴结肿大和流行病学史可以高度提示猴痘的诊断。
治疗方面,目前没有针对猴痘的特效药物获批。替考韦瑞(TPOXX)是唯一获得美国食品药品监督管理局批准用于治疗天花的药物,它通过抑制病毒包膜蛋白VP37来阻止病毒的包装和释放。动物实验显示,替考韦瑞对猴痘病毒感染有效,但人体临床试验的结果令人失望——在2024年发表的随机对照试验中,替考韦瑞未能显著缩短皮损消退时间。布林西多福韦是另一种有潜力的药物,它是一种口服的前药,在体内转化为西多福韦后具有抗病毒活性。但布林西多福韦也有明显的局限性——它可能引起肝毒性,而且需要较长的给药周期。
疫苗是预防猴痘的基石。JYNNEOS是一种基于改良安卡拉牛痘病毒(MVA)的非复制型疫苗,它不能在人体细胞中完成复制周期,因此安全性极佳,可以用于免疫功能低下者和孕妇。ACAM2000是一种复制型疫苗,基于与消灭天花运动中使用的Dryvax疫苗相似的牛痘病毒株。ACAM2000的免疫原性更强,但安全性较差——可能导致心肌炎、心包炎和进行性牛痘等严重不良反应。
一项发表在《新英格兰医学杂志》上的研究评估了JYNNEOS疫苗在2022年疫情中的有效性。研究发现,完整接种两剂疫苗后,预防猴痘感染的有效性约为66%至89%。但疫苗的保护作用并非立竿见影——在接种第一剂后14天内,疫苗的保护效果仍然有限。这提示我们,在暴露后尽快接种疫苗(暴露后预防)可能对高危人群有益。
猴痘病毒的未来走向仍然充满不确定性。一种可能性是,病毒将继续在特定人群中低水平流行,成为一种地方性传播的性传播疾病。另一种可能性是,病毒将发生进一步的适应性进化,增强其人际传播能力,最终成为一种更广泛的公共卫生威胁。还有第三种可能性——猴痘病毒可能在新的人群和环境中找到新的动物宿主,建立独立的传播循环,使其成为全球性的地方性动物病。
2022年疫情给人类留下了一个深刻的教训:在一个高度互联的世界中,任何一个角落发生的疫情都可能迅速演变为全球性危机。猴痘病毒在非洲雨林中潜伏了数十年,因为它被视为"别人的问题"而被国际社会忽视。当病毒最终跨越边界、进入非流行地区时,人类发现自己对此毫无准备——诊断工具短缺、疫苗供应不足、治疗药物缺乏临床证据。
猴痘病毒的故事远未结束。随着人类对自然环境的不断侵入,随着全球旅行的日益便捷,随着免疫屏障的持续降低,正痘病毒家族的其他成员可能也会走出阴影。猴痘病毒只是人类与古老病原体之间漫长博弈的最新篇章——而这场博弈的最终结果,取决于我们今天做出的每一个选择。
在结束这篇文章之前,让我们回到1970年的那个刚果村庄,回到那个九个月大婴儿的病床边。他可能不知道,自己身上那些痛苦的疱疹正在书写医学史上一个新的篇章。他可能不知道,半个世纪后,他所感染的病毒会引发一场全球性的公共卫生危机。但这个故事告诉我们,在人类与病毒的永恒战争中,忽视是最危险的敌人。每一例被忽视的病例,每一起被忽视的疫情,都可能成为下一场大流行的序曲。
猴痘病毒不会是最后一个从动物宿主跳跃到人类的病原体。在地球的某个角落,另一种病毒可能正在经历着与猴痘相似的进化旅程,等待着被人类发现的那一刻——或者,等待着在人类毫无防备的情况下突然爆发的那一刻。我们唯一能做的,就是保持警惕,加强监测,投资研究,在全球范围内建立强大的公共卫生系统。因为在病毒的世界里,没有国界,没有"别人的问题"——每一个被忽视的角落,都可能成为下一个全球危机的起点。
参考资料
-
Magnus PV, Andersen EK, Petersen KB, Birch-Andersen A. A pox-like disease in cynomolgus monkeys. Acta Pathologica et Microbiologica Scandinavica. 1959;46(2):156-176.
-
Ladnyj ID, Ziegler P, Kima E. A human infection caused by monkeypox virus in Basankusu Territory, Democratic Republic of the Congo. Bulletin of the World Health Organization. 1972;46(5):593-597.
-
Bunge EM, Hoet B, Chen L, et al. The changing epidemiology of human monkeypox—A potential threat? A systematic review. PLOS Neglected Tropical Diseases. 2022;16(2):e0010141.
-
Thornhill JP, Barkati S, Walmsley S, et al. Monkeypox Virus Infection in Humans across 16 Countries. New England Journal of Medicine. 2022;387(8):679-691.
-
Amero L, Earl PL, Lapa D, et al. Virulence differences of mpox (monkeypox) virus clades I, IIa, and IIb. Proceedings of the National Academy of Sciences. 2023;120(8):e2204115120.
-
World Health Organization. WHO Director-General declares mpox outbreak a public health emergency of international concern. August 14, 2024.
-
Alkhalil A, Strandberg T, Rillahan CD, et al. Gene expression profiling of monkeypox virus-infected cells identifies host factors for virus replication. Virology. 2009;393(2):238-249.
-
Hutson CL, Carroll DS, Self J, et al. Dosage comparison of 2 licensed smallpox vaccines with the U.S. national stockpile. Journal of Infectious Diseases. 2015;211(8):1260-1265.
-
Seang Y, Burrel S, Todesco E, et al. Evidence of human-to-dog transmission of monkeypox virus. The Lancet. 2022;400(10353):658-659.
-
Desgranges C, Lhomme E, Babinet G, et al. Transmission of MPXV from fire-footed rope squirrels to sooty mangabeys. Nature. 2026;638:123-130.