引言:一场完美的医疗风暴
2011年的一个寒冷冬日,马萨诸塞州综合医院的传染病病房里,一位68岁的退休教师正在经历她人生中最黑暗的时刻。三个月前,她只是因为一次普通的尿路感染住进了这家医院,医生给她开了为期十天的环丙沙星——一种被广泛使用的氟喹诺酮类抗生素。那是她一生中第一次需要住院治疗,她以为自己很快就能回家。
十天后的确回家了,但仅仅过了三天,严重的腹泻开始了。起初是每天四五次,然后变成十几次,最后她几乎无法离开卫生间。粪便带着一种独特的、令人作呕的恶臭,像是马厩里发酵的稻草。高烧吞噬着她的体力,腹部绞痛让她蜷缩在床上无法动弹。急诊室的医生看着她脱水的脸庞和剧烈腹痛,立即安排了结肠镜检查。
镜头进入她结肠的那一刻,年轻的住院医师倒吸了一口冷气。原本应该光滑粉红的肠黏膜上,覆盖着一层层黄白色的斑块,像是融化的奶酪,又像是某种真菌的菌落。这些斑块融合在一起,形成了一片可怕的"伪膜"——这是肠道正在死亡的标志。在这些伪膜下面,黏膜已经溃烂、出血,肠壁肿胀得几乎堵塞了整个肠腔。
诊断书上写着:伪膜性肠炎,艰难梭菌感染,重症。
这不是故事的开始,而是故事的中段。这位退休教师的经历,在过去几十年里,在全球各地的医院中重复上演了数百万次。根据美国疾病控制与预防中心的数据,仅2011年一年,美国就有约四十五万三千人感染艰难梭菌,其中约二万九千人直接因此死亡。这个数字超过了艾滋病、流感和肝炎的总和。而这还只是美国的数据。
更令人不安的是,这个杀手的出现,与人类医学史上最伟大的发明之一——抗生素——有着密不可分的关系。它就像是抗生素时代的幽灵,潜伏在我们创造奇迹的地方,等待着最佳时机发动致命一击。
1935年:一个被遗忘的婴儿肠道居民
故事要从1935年说起。那一年,美国爱荷华大学的细菌学家伊万·霍尔和伊丽莎白·奥图尔正在研究一个看似与疾病无关的问题:新生儿的肠道菌群是如何建立的。
在显微镜还不足以看清细菌世界的时代,霍尔和奥图尔使用的是最传统的方法:培养。他们将新生儿的粪便样本接种到各种培养基上,试图分离出那些在婴儿肠道中安家的微生物。在大多数情况下,他们分离出的都是已知的细菌——大肠杆菌、肠球菌、双歧杆菌。但在一个样本中,他们发现了一种奇怪的厌氧菌。
这种细菌在培养皿上生长极其缓慢,需要几天时间才能形成可见的菌落。它的形态也很独特:长杆状,末端膨大,像是一个鼓槌或纺锤。革兰染色呈阳性,但这在厌氧菌中并不罕见。最让霍尔和奥图尔困惑的是,这种细菌似乎很难培养——他们尝试了多种培养基和方法,才最终让它在实验室里存活下来。
正是这种"培养困难"的特性,让霍尔和奥图尔给它起了一个看似随意却预言般的名字:Bacillus difficilis——“困难杆菌”。
他们注意到一个有趣的现象:这种细菌在健康的新生儿肠道中相当常见,但在成人中却很少分离出来。霍尔和奥图尔在他们的论文中写道,这种细菌"可能是新生儿肠道正常菌群的一部分",并没有表现出任何致病性。
论文发表后,这种细菌很快被重新分类到梭菌属,名字也变成了C. difficile——艰难梭菌。在接下来的四十年里,它一直是一个默默无闻的存在,偶尔出现在微生物学教科书的角落里,被归类为"可能无害的厌氧菌"。
很少有人注意到,这个"无害"的标签,是建立在肠道菌群完整的基础上的。
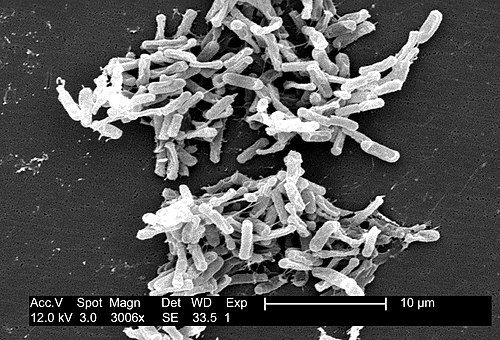
1978年:被揭开的真相
1970年代中期,一场神秘的流行病正在美国的医院里悄然蔓延。患者们——大多是刚刚接受过抗生素治疗的病人——开始出现严重的腹泻和腹痛。结肠镜检查显示,他们的结肠内壁覆盖着特征性的黄白色伪膜。这种疾病被称为"伪膜性肠炎",但没有人知道是什么引起的。
当时的主流理论认为,伪膜性肠炎可能是由金黄色葡萄球菌引起的。毕竟,金黄色葡萄球菌是医院感染的主要元凶之一,而且也有过抗生素治疗后葡萄球菌过度生长的报道。但有一个问题:在伪膜性肠炎患者的粪便中,很少能分离出大量的金黄色葡萄球菌。
转折点出现在1978年。那一年,波士顿塔夫茨新英格兰医学中心的约翰·巴特利特和他的同事们正在研究一种从伪膜性肠炎患者粪便中分离出的毒素。他们将患者的粪便滤液加入到培养的人类细胞中,观察到一种独特的细胞病变效应:细胞变圆、脱落、死亡。
这不是金黄色葡萄球菌毒素的表现。
与此同时,弗吉尼亚大学的科学家们正在研究艰难梭菌。他们发现,某些艰难梭菌菌株能产生一种强效的细胞毒素,其效应与巴特利特观察到的惊人地相似。
当两组科学家进行交叉验证时,真相浮出水面:伪膜性肠炎患者粪便中的毒素,可以被艰难梭菌的抗毒素中和。更关键的是,当他们将产生毒素的艰难梭菌培养物喂给仓鼠时,这些小动物出现了与人类伪膜性肠炎相似的病变,并在几天内死亡。
科赫法则——判定某种微生物是否为疾病病原体的金标准——被满足了。艰难梭菌,这个被忽视了四十多年的"无害"细菌,终于露出了它的真面目。
更令人震惊的是进一步的发现:艰难梭菌产生的伪膜性肠炎几乎总是与抗生素使用相关。抗生素杀死了肠道中竞争营养的其他细菌,艰难梭菌趁机大量繁殖,释放出致命的毒素。这是一种典型的"机会性感染",而且它的发生直接与人类对抗微生物的战争相关。

两枚分子炸弹:毒素A与毒素B
要理解艰难梭菌为何如此致命,我们需要深入到分子层面,看看它的武器是如何工作的。
致病性艰难梭菌菌株主要产生两种大分子毒素:毒素A(TcdA,也称为肠毒素)和毒素B(TcdB,也称为细胞毒素)。这两者都是巨大的蛋白质分子,分子量分别约为308和270千道尔顿,是已知最大的细菌毒素之一。它们的基因位于一个被称为"致病岛"的染色体区域上,与调控基因一起,形成了一个精密的武器制造工厂。
毒素A和毒素B在结构上约有百分之六十三的相似性,但它们的功能和靶点却有着微妙而重要的差异。当艰难梭菌在结肠中繁殖时,这两种毒素被释放到肠腔中,开始了它们对宿主细胞的系统性攻击。
攻击的第一步是结合。毒素分子上有一个特殊的受体结合域,能识别并结合到宿主细胞表面的特定碳水化合物结构上。毒素A主要结合到人类结肠上皮细胞表面的Galα1-3Galβ1-4GlcNAc结构,而毒素B的受体至今仍未完全确定,但已知它能结合到更广泛的细胞类型上。
结合后,毒素通过受体介导的内吞作用进入细胞。这是一个精巧的入侵策略:毒素"欺骗"细胞,让细胞以为它是在摄取有用的营养物质,主动将其包裹在内吞泡中带入细胞内部。
进入细胞后,毒素面临着一个关键挑战:如何从内吞泡中逃逸到细胞质?这是通过毒素的pH依赖性构象变化实现的。当内吞泡与溶酶体融合时,泡内的pH值下降到酸性范围。这种酸性环境触发毒素分子发生剧烈的构象变化,暴露出一个疏水区域,插入内吞泡膜并形成孔洞。毒素的活性部分通过这个孔洞进入细胞质,而这一过程只需要几秒钟。
接下来发生的事情,堪称分子生物学的杰作——或者,从受害者的角度看,噩梦。
进入细胞质后,毒素释放出它的催化结构域。这是一个葡萄糖转移酶,专门针对Rho家族的小G蛋白——Rho、Rac和Cdc42。这些G蛋白是细胞骨架系统的关键调控者,它们就像细胞的"指挥官",控制着肌动蛋白的聚合和排列,维持着细胞的形状、运动和连接。
毒素通过一个精确的化学反应,将一个葡萄糖基团从UDP-葡萄糖转移到Rho蛋白的一个关键氨基酸残基上。这个修饰就像给指挥官戴上了手铐,让它完全失去功能。Rho蛋白无法再激活它的下游效应分子,整个细胞骨架系统开始崩溃。
后果是灾难性的。肌动蛋白丝解聚,细胞失去形状,变成球形。细胞之间的紧密连接被破坏,肠道屏障功能丧失。更重要的是,受损的细胞会释放炎症介质,引发中性粒细胞和其他炎症细胞的浸润。在显微镜下,可以看到结肠黏膜上形成特征性的"伪膜"——由坏死的上皮细胞、纤维蛋白、黏液和炎症细胞组成的混合物。
毒素B比毒素A更加致命。研究表明,毒素B在体外对人类细胞的毒性比毒素A强约一千倍。它能够更有效地进入多种类型的细胞,造成更广泛的损害。动物实验中,单纯敲除毒素B基因的艰难梭菌几乎完全丧失了致病能力,而单纯敲除毒素A基因的菌株仍然能够引起疾病,只是症状较轻。
除了这两种主要毒素,部分高毒力菌株还产生第三种毒素:艰难梭菌转移酶(CDT),一种二元毒素。它通过破坏肌动蛋白骨架形成微管突起,增强细菌对上皮细胞的黏附,从而进一步加剧感染。

抗生素悖论:当救星变成帮凶
艰难梭菌感染最令人困惑的特性是它的发病机制:抗生素,这个人类对抗感染最强大的武器,竟然是它最重要的帮凶。这被称为"抗生素悖论"——我们用来拯救生命的药物,却在创造另一种致命的威胁。
在健康的成人肠道中,居住着数以万亿计的微生物,它们形成了一个复杂而稳定的生态系统。这些微生物——主要是各种厌氧菌——通过竞争营养、产生抑菌物质、占据生态位等方式,形成了一道抵御外来入侵者的屏障。艰难梭菌在这个系统中只是一个边缘角色,它的数量被严格控制在很低水平,没有机会释放足够的毒素造成伤害。
当广谱抗生素被使用时,情况发生了剧变。抗生素无差别地杀灭肠道中的敏感细菌,打破了原有的生态平衡。一些细菌完全消失,另一些数量大幅减少。这个过程中,艰难梭菌的芽孢——那些在环境中可以存活数月甚至数年的休眠形式——在肠道中萌发,找到了一个几乎没有竞争对手的肥沃土壤。
研究表明,克林霉素、头孢菌素和氟喹诺酮类药物是诱发艰难梭菌感染风险最高的抗生素。这些药物对肠道正常菌群的杀伤力特别强,而艰难梭菌本身就对它们有天然的抗性。一个典型的场景是:患者因为一次普通的呼吸道感染接受了为期一周的阿莫西林-克拉维酸治疗,一周后感染痊愈,但肠道菌群已经被严重破坏。此时,如果患者接触到艰难梭菌芽孢——可能来自医院环境,也可能来自社区——细菌就会迅速定植并大量繁殖。
更微妙的是,抗生素对肠道菌群的影响远比我们想象的持久。一项研究显示,单次一周的克林霉素治疗可以使肠道菌群紊乱持续长达两年。在这两年中,患者都处于艰难梭菌感染的高风险状态。这解释了为什么很多患者在抗生素使用后很长时间才发病。
但抗生素并不是唯一的风险因素。质子泵抑制剂——那些广泛用于治疗胃酸过多的药物——也与艰难梭菌感染风险增加相关。胃酸是杀灭摄入微生物的第一道防线,当这道防线被药物削弱后,更多的艰难梭菌芽孢能够活着通过胃部,到达它们的目的地——结肠。
年龄是另一个关键因素。六十五岁以上的老年人感染风险显著增加,这可能与免疫系统功能下降、肠道菌群多样性减少以及更多的基础疾病有关。住院和长期护理机构居住也是重要风险因素,因为这些地方往往存在大量的艰难梭菌芽孢和抗生素使用。

2003-2005年:魁北克的噩梦
2003年春天,加拿大魁北克省的医院开始报告一种奇怪的疾病爆发。患者们——大多是老年人——出现了严重的腹泻和全身症状,对标准治疗反应不佳,死亡率远高于以往观察到的水平。
起初,人们以为这只是一次常规的艰难梭菌感染季节性高峰。但随着病例数量的急剧增加和死亡率的异常攀升,流行病学家们意识到情况不对劲。2003年至2005年间,魁北克省报告了超过七千例艰难梭菌感染,其中约一千四百例直接导致死亡。在某些医院,死亡率高达百分之八到十,而历史平均水平只有百分之一到二。
分子流行病学调查揭示了原因:这次爆发的元凶是一种前所未见的高毒力艰难梭菌菌株,被称为BI/NAP1/027。这个命名反映了三种不同的分子分型方法得到的一致结果:限制性内切酶分析分型为BI组,脉冲场凝胶电泳分型为NAP1型,核糖体分型为027型。
这种菌株携带多种毒力因子。首先,它产生的毒素A和毒素B量远超普通菌株——研究显示,在相同培养条件下,NAP1/027株产生的毒素量可以是其他菌株的十六到二十三倍。其次,它还携带二元毒素基因,可能进一步增强致病性。最后,它对氟喹诺酮类抗生素高度耐药,这意味着广泛使用这类药物实际上在筛选和促进这种高毒力菌株的传播。
更令人担忧的是,NAP1/027株似乎具有更强的芽孢形成能力,这意味着它在医院环境中更难被清除。常规的酒精消毒对芽孢完全无效,只有含氯消毒剂或过氧化氢蒸汽才能杀灭它们。在很多医院,艰难梭菌芽孢可以从地板、床栏、呼叫按钮、甚至是血压计袖带上分离出来。
魁北克爆发之后,NAP1/027株迅速蔓延到北美和欧洲。英国在2004年至2008年间经历了艰难梭菌感染的大幅上升,部分地区的死亡率翻了一番。美国疾病控制与预防中心估计,2000年至2007年间,美国艰难梭菌相关死亡增加了百分之四百。
这次爆发震惊了整个医学界,也让艰难梭菌从一个"医院获得性感染"的注脚,跃升为公共卫生的头号威胁之一。

复发:无休止的循环
对于很多艰难梭菌感染患者来说,第一次感染只是噩梦的开始。
标准治疗——口服万古霉素或非达霉素——对初次感染通常有效。大约百分之八十的患者在十天疗程后症状消失,粪便检测结果转阴。但在接下来的几周里,大约百分之二十到三十的患者会经历复发。症状再次出现:腹泻、腹痛、发热,一切都从头开始。
更令人绝望的是,复发的风险随着每一次发作而增加。第一次复发后,第二次复发的风险上升到百分之四十。第二次复发后,第三次复发的风险高达百分之六十。有些患者经历了五次、六次甚至十几次复发,他们的生活被彻底打乱。每一次复发都意味着另一次抗生素疗程,而每一次抗生素使用又为下一次复发创造了条件。
复发的机制很复杂。一部分复发是由同一菌株的持续存在引起的——抗生素可能杀死了大部分艰难梭菌,但芽孢在肠道中存活下来,在停药后重新萌发。另一部分复发是由不同菌株的再次感染引起的——患者在医院或社区环境中接触了新的芽孢。还有一部分复发可能与肠道菌群的持续紊乱有关——抗生素治疗后,肠道生态系统没有完全恢复,仍然处于脆弱状态。
复发的治疗比初次感染更加困难。标准疗程可能需要延长,或者采用"脉冲式"给药——在初始疗程后,逐渐减少给药频率,持续数周甚至数月。这种策略的理论基础是,在肠道菌群逐渐恢复的过程中,间歇性的药物压力可以抑制艰难梭菌的反弹。
但对于那些经历了多次复发的患者,即使是最优化的抗生素方案也可能失败。在这种情况下,一种听起来近乎疯狂的疗法进入了医学界的视野:粪便微生物移植。
粪便移植:从民间偏方到医学奇迹
2013年1月,新英格兰医学杂志发表了一项可能改变医学史的临床试验结果。荷兰的研究者将复发性艰难梭菌感染患者随机分为两组:一组接受标准万古霉素治疗,另一组接受万古霉素联合粪便微生物移植——简单来说,就是把健康人的粪便移植到患者肠道中。
试验原本计划招募更多患者,但在进行到一半时就被提前终止了。原因是:粪便移植组的效果实在太好了。
在接受单次粪便移植的患者中,百分之八十一在三个月内实现了症状缓解。如果包括接受第二次移植的患者,总体治愈率超过百分之九十。相比之下,标准万古霉素组的治愈率只有百分之三十一。差异如此显著,以至于继续随机分配患者接受可能无效的标准治疗被认为是不道德的。
粪便移植并不是全新的概念。在中国,早在四世纪就有使用粪便治疗腹泻和食物中毒的记载。明代医学家李时珍在《本草纲目》中记载了"黄龙汤"——用粪便和水制成的药剂——治疗腹痛和腹泻的方法。在西方,1958年,科罗拉多的外科医生本·艾斯曼曾用粪便灌肠成功治疗了四例严重的伪膜性肠炎患者——那时艰难梭菌还不是已知病原体。
但这些早期案例一直被视为医学奇闻,没有进入主流医学实践。直到艰难梭菌复发问题日益严重,人们才开始认真考虑这种看似"不卫生"的疗法。
粪便移植的工作原理是恢复肠道菌群的多样性和功能。健康供体的粪便中含有数百种细菌,以及它们的代谢产物、噬菌体和其他微生物成分。当这些物质被引入患者肠道后,它们开始重建正常的微生物群落。产生短链脂肪酸的细菌恢复生长,这些脂肪酸不仅滋养肠上皮细胞,还能抑制艰难梭菌的萌发和生长。次级胆汁酸代谢恢复正常,这些物质同样具有抗艰难梭菌活性。更重要的是,正常的微生物群落重建了"定植抗性"——一个新的艰难梭菌芽孢很难在这样的环境中萌发和繁殖。
移植的方式多种多样。最初是使用结肠镜将粪便悬液直接注入盲肠。后来发展出鼻十二指肠管、保留灌肠等方法。最简便的是口服胶囊——将处理过的粪便物质封装在耐酸的胶囊中,患者只需吞服即可。
2022年11月,美国食品药品监督管理局批准了第一个粪便微生物产品Rebyota,用于预防复发性艰难梭菌感染。2023年4月,第一个口服粪便微生物产品Vowst也获得了批准。这标志着粪便移植从一个边缘疗法,正式进入了主流医学的殿堂。
但粪便移植并非没有风险。2019年,一名患者在接受粪便移植后因耐药细菌感染而死亡,原因是供体粪便中携带了未被检测到的多重耐药大肠杆菌。这一事件促使FDA加强了粪便移植的监管,要求更严格的供体筛查。

诊断与治疗的现代战场
现代艰难梭菌感染的诊断已经远远超出了简单的培养。最常用的是核酸扩增测试(NAAT),如聚合酶链反应(PCR),检测细菌的毒素基因。这种方法敏感性高、速度快,几小时内就能出结果。但它的缺点是可能检测到无症状携带者——那些携带有毒力基因但并未发病的人。
另一种常用方法是酶联免疫吸附试验(ELISA),直接检测粪便中的毒素A和毒素B。这种方法特异性高——阳性结果通常意味着活动性感染——但敏感性相对较低。很多实验室采用两步法:先用PCR筛查,阳性样本再用ELISA确认是否存在毒素。
对于重症患者,额外的评估是必要的。血清白蛋白水平、白细胞计数和肌酐水平被用来判断疾病的严重程度。重症患者可能需要额外支持治疗,甚至外科干预。在极少数情况下,当结肠严重扩张(毒性巨结肠)或有穿孔风险时,可能需要紧急切除结肠。
治疗方面,万古霉素口服仍然是轻中度感染的一线选择。它在大肠中达到高浓度,直接作用于艰难梭菌,同时对肠道正常菌群的破坏相对较小。非达霉素是一种更新的窄谱大环内酯类抗生素,与万古霉素疗效相当,但复发率更低。它的缺点是价格昂贵——一个疗程可能花费数千美元。
对于重症感染,可能需要联合使用口服万古霉素和静脉甲硝唑。甲硝唑曾是轻中度感染的一线用药,但由于耐药率上升和疗效不如万古霉素,现在主要用于重症的辅助治疗。
贝佐洛单抗是一种单克隆抗体,能中和毒素B。它不是抗生素,而是作为辅助治疗,与标准抗生素一起使用,可以降低复发风险。对于那些有高复发风险的患者——比如老年人、免疫功能低下者——这可能是一个有价值的选择。
预防方面,手卫生至关重要。但与大多数医院感染不同,艰难梭菌芽孢对酒精消毒剂有抵抗力。有效的手卫生需要使用肥皂和流动水,通过机械摩擦去除芽孢。环境清洁同样关键——使用含氯消毒剂或过氧化氢产品,而不是常规的季铵盐消毒剂。
更重要的是合理使用抗生素。抗生素管理项目在减少艰难梭菌感染方面发挥着越来越重要的作用。这些项目通过限制高风险抗生素的使用、缩短疗程、优化给药途径等方式,从源头上降低感染风险。研究表明,减少氟喹诺酮类药物的使用可以直接降低艰难梭菌感染率。
未来:疫苗与新的战场
尽管治疗手段不断进步,但艰难梭菌感染仍然是一个重大公共卫生挑战。感染率在某些人群中持续上升,复发问题困扰着成千上万的患者。因此,研究者们将目光投向了更根本的解决方案:预防。
艰难梭菌疫苗的研发已经进行了多年。2022年,辉瑞公司宣布其艰难梭菌候选疫苗在三期临床试验中达到了主要终点,显示出显著的预防效果。这种疫苗针对毒素A和毒素B,旨在诱导产生中和抗体,防止毒素造成的损害。对于高危人群——如计划接受抗生素治疗的住院患者——疫苗可能成为预防感染的重要工具。
另一个活跃的研究领域是微生物组疗法。除了粪便移植,研究者正在开发更精确的方法来恢复肠道健康微生物群落。这些方法包括:特定菌株组合的培养细菌产品、细菌代谢产物制剂、以及噬菌体疗法。目标是找到粪便移植中最关键的成分,并将其标准化、规模化生产,避免使用完整粪便带来的风险和不确定性。
抗生素研发也在继续。新的窄谱抗生素正在临床试验中,这些药物专门针对艰难梭菌,对正常肠道菌群的影响更小。另一种思路是使用非抗生素方法抑制艰难梭菌,比如针对芽孢萌发的药物、针对毒素的单克隆抗体、或者针对细菌黏附的抑制剂。
基础研究方面,科学家们正在深入理解艰难梭菌的生物学特性。最近的研究发现,艰难梭菌的表面有一层被称为"S层"的盔甲样结构,可能帮助它抵抗宿主的防御机制和抗生素。破坏这种结构可能成为新的治疗靶点。另一个有趣的发现是,艰难梭菌能够产生对甲酚——一种抑制其他细菌生长的化学物质,这可能解释了它为什么能在抗生素干扰后迅速占据生态位。
流行病学方面,研究者们正在追踪新的高毒力菌株。除了NAP1/027,其他核糖体型如078也在某些地区成为主要流行株。理解这些菌株的传播模式和毒力机制,对于制定有效的防控策略至关重要。
令人担忧的是,艰难梭菌感染正在从医院扩展到社区。越来越多的病例发生在没有近期住院或抗生素使用史的人群中。这提示我们,艰难梭菌可能正在适应新的生态位,或者社区环境中存在我们尚未认识的传播途径。
尾声:与幽灵共存
回到文章开头的那位退休教师。她在经历了三个月的治疗、两次复发、一次粪便移植后,终于摆脱了艰难梭菌的纠缠。但她的肠道菌群——那个曾经稳定、多样化的生态系统——可能需要数年才能完全恢复,甚至可能永远不会回到感染前的状态。
她的故事是现代医学困境的一个缩影。抗生素是医学史上最伟大的发明之一,它们拯救了无数生命。但它们也创造了新的生态空位,让艰难梭菌这样的机会性病原体得以崛起。这是一种进化的博弈:我们越广泛地使用抗生素,就越强烈地筛选出耐药和抵抗的微生物。
艰难梭菌不是唯一的例子。耐甲氧西林金黄色葡萄球菌、耐碳青霉烯肠杆菌、多重耐药鲍曼不动杆菌……这些名字代表着另一个战场,一个正在变得越来越艰难的战场。而艰难梭菌之所以特别,是因为它直接利用了我们对抗感染的武器——抗生素——作为它自己的机会。
在某种程度上,艰难梭菌是抗生素时代的一个警示。它提醒我们,医学干预从来不是没有代价的。当我们消灭一种病原体时,我们也在重新塑造微生物世界,创造新的生态平衡。有时,这种新的平衡对我们有利;有时,它会产生意想不到的后果。
未来,我们可能需要更精细的医疗干预方式——不是用"核武器"级别的广谱抗生素摧毁整个微生物群落,而是用更精确的手段针对特定的病原体。我们可能需要更多地关注微生物组的健康,将其视为一个需要维护和保护的器官。我们可能需要重新思考感染控制策略,不仅仅关注单个患者的治疗,而是关注整个医疗生态系统的平衡。
艰难梭菌,这个在1935年被发现、在1978年被定罪的"幽灵",至今仍在全球各地的医院和社区中游荡。它每年夺走近三万条生命,感染数百万人。但与此同时,针对它的研究也推动了微生物组医学的革命,催生了粪便移植等创新疗法,深化了我们对肠道微生物世界的理解。
在抗生素时代最辉煌的时刻,艰难梭菌悄然崛起,提醒我们自然的复杂性。在与它的斗争中,我们学会了谦卑,学会了精细,也学会了用全新的视角看待我们与微生物的关系。这场战争远未结束,但至少现在,我们知道了敌人是谁,以及它的武器是什么。
主要参考资料:
-
Hall IC, O’Toole E. Intestinal flora in new-born infants: with a description of a new pathogenic anaerobe, Bacillus difficilis. American Journal of Diseases of Children. 1935;49(2):390-402.
-
Bartlett JG, et al. Clindamycin-associated colitis due to a toxin-producing species of Clostridium in hamsters. Journal of Infectious Diseases. 1978;136(5):701-705.
-
Lessa FC, et al. Burden of Clostridium difficile infection in the United States. New England Journal of Medicine. 2015;372(9):825-834.
-
van Nood E, et al. Duodenal infusion of donor feces for recurrent Clostridium difficile. New England Journal of Medicine. 2013;368(5):407-415.
-
Kordus SL, Thomas AK, Lacy DB. Clostridioides difficile toxins: mechanisms of action and antitoxin therapeutics. Nature Reviews Microbiology. 2022;20(5):285-298.
-
McDonald LC, et al. An epidemic, toxin gene-variant strain of Clostridium difficile. New England Journal of Medicine. 2005;353(23):2433-2441.
-
Cornely OA, et al. Fidaxomicin versus vancomycin for infection with Clostridium difficile in Europe, Canada, and the USA: a double-blind, non-inferiority, randomised controlled trial. Lancet Infectious Diseases. 2012;12(4):281-289.
-
Mullish BH, et al. The use of faecal microbiota transplant as treatment for recurrent or refractory Clostridium difficile infection. Gut. 2018;67(11):1920-1941.
-
Centers for Disease Control and Prevention. Antibiotic Resistance Threats in the United States, 2019.
-
Vehreschild MJ, et al. Effectiveness and safety of fecal microbiota transplantation for Clostridioides difficile infection: A systematic review and meta-analysis. Gastroenterology. 2022;163(4):1001-1011.
