1909年4月14日,巴西米纳斯吉拉斯州一个叫Lassance的偏远火车站小镇,29岁的年轻医生卡洛斯·查加斯正在例行检查当地居民。这位来自奥斯瓦尔多·克鲁兹研究所的研究员原本是被派来抗击疟疾的,却在这片荒凉的内陆发现了某种更加致命的东西。当他检查一名叫贝雷尼塞的两岁女孩时,发现她发着高烧,肝脏和脾脏都肿大,最引人注目的是她的一只眼睛周围有明显的肿胀。查加斯在她的血液中看到了一个让他心跳加速的东西——一种从未在人类血液中发现的鞭毛虫。那个下午,这位年轻的医生并不知道,他刚刚发现了人类医学史上唯一一种由同一个人完整描述了病原体、传播媒介、临床表现和流行病学的疾病。
查加斯的发现堪称医学史上最传奇的侦探故事之一。故事要从一年前说起。1907年,奥斯瓦尔多·克鲁兹将查加斯派往Lassance,因为那里的疟疾正在阻碍巴西中央铁路的建设。这位年轻医生把一节火车车厢改造成了实验室和住所,开始了他的工作。1908年中,一位名叫坎塔里诺·莫塔的工程师告诉查加斯,当地有一种叫"chupão"或"barbeiro"的昆虫,会在夜间吸食居民的血液,白天则躲在泥砖房的缝隙中。查加斯在显微镜下检查这些昆虫的肠道内容物时,发现了一种他称为"critidias"(现在称为上鞭毛体)的微生物。他推断这些携带寄生虫的昆虫可能通过吸血将它们传播给人类。但Lassance没有条件进行动物实验,于是查加斯将感染的昆虫标本寄给了在里约热内卢的克鲁兹,请他将昆虫与未感染的狨猴放在一起。三周后,克鲁兹在狨猴的血液中发现了寄生虫,立即召回了查加斯。
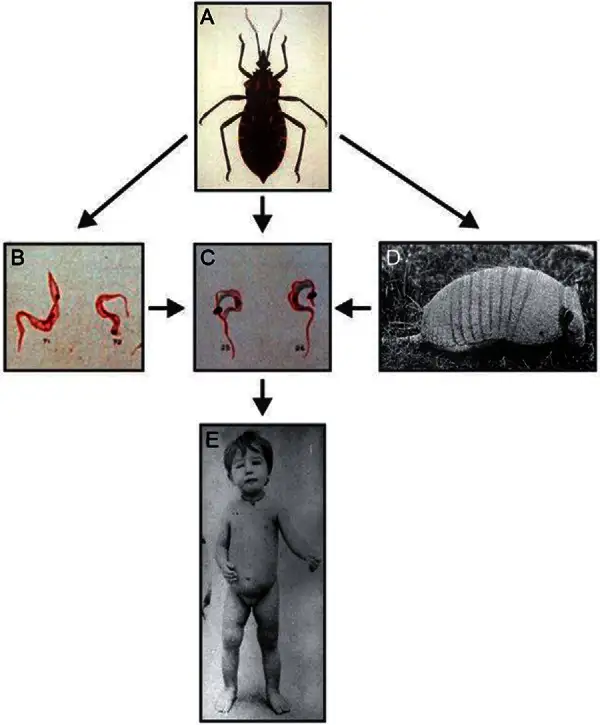
从1908年11月开始,查加斯在老鼠、豚鼠、兔子、狗和猴子上进行实验,确认这些哺乳动物都会被感染。1909年4月,当他回到Lassance时,确信自己发现了一种新的疾病。他开始检查居住在泥砖房中的居民和家畜,首先发现了一只感染的猫,然后在4月14日发现了贝雷尼塞——这个两岁的白人女孩成为史上第一个被确诊的恰加斯病患者。查加斯以他导师的名字将这种新发现的寄生虫命名为Schizotrypanum cruzi(后改为Trypanosoma cruzi,克氏锥虫)。第二天,奥斯瓦尔多·克鲁兹就在国家医学科学院公布了这一发现。
但查加斯并没有就此止步。1912年,他在一只犰狳体内发现了克氏锥虫,而这只犰狳正与野生锥蝽生活在同一个洞穴中——由此发现了恰加斯病的野生动物循环。他是历史上唯一一个独自完整描述一种传染病全部要素的科学家:病原体、传播媒介、野生宿主、临床症状和流行病学特征。如此卓越的成就让他两次被提名诺贝尔奖,但每次都与奖项失之交臂。更令人唏嘘的是,贝雷尼塞本人——这个被载入医学史的女孩——在感染后并未发展出严重的心脏病变,她一直活到73岁才因其他原因去世。查加斯于1934年去世,年仅55岁,他没能亲眼看到"他的疾病"如何成为拉丁美洲最严重的公共卫生问题之一。
夜访者的真面目
锥蝽,这种在英语中被称为"接吻虫"的昆虫,拥有一个极具欺骗性的名字。它们之所以获得这个温柔的称呼,是因为它们倾向于在受害者脸部周围叮咬,尤其是嘴唇和眼睛附近的皮肤。但在拉丁美洲,它们有着更加直白和令人恐惧的名字:阿根廷、玻利维亚、智利和巴拉圭人叫它"vinchuca",意为"让自己掉下来的东西";巴西人称它为"barbeiro",即"理发师",因为它总是在脸部附近活动;哥伦比亚人叫它"pito";中美洲人称它为"chinche";委内瑞拉人则称它为"chipo"。所有这些名字背后,都是几代人积累下来的恐惧与警觉。
锥蝽属于半翅目猎蝽科锥蝽亚科,目前已发现超过140种,分为19个属和5个族。其中大多数是野生种类,与哺乳动物和鸟类的栖息地相关;一些生活在人居周围,如鸡舍、猪圈和牲口棚;少数则进入了人类住宅,成为最重要的传播媒介。在这些家居种类中,最著名的是南锥体地区的Triatoma infestans、安第斯地区和中美洲的Rhodnius prolixus,以及Panstrongylus megistus。这些昆虫体型较大,成年个体可长达2-3厘米,身体扁平呈椭圆形,有着长长的头部和明显的颈部。它们通常呈棕色或黑色,但腹部边缘常有红色或橙色的斑纹——这是它们作为"红带锥蝽"的标志性特征。

锥蝽是严格的吸血昆虫,它们的生命周期包括卵、五个若虫期和成虫期,每个阶段都需要吸血才能发育到下一阶段。它们在夜间活动,被二氧化碳和体温吸引,能够感知宿主的存在。在吸血时,锥蝽会注入含有麻醉成分的唾液,使受害者感觉不到叮咬——这正是它们能够饱餐一顿而不被发现的关键。一只成虫一次可以吸入自身体重数倍的血液。但致命的并非叮咬本身,而是发生在叮咬之后的某种行为。
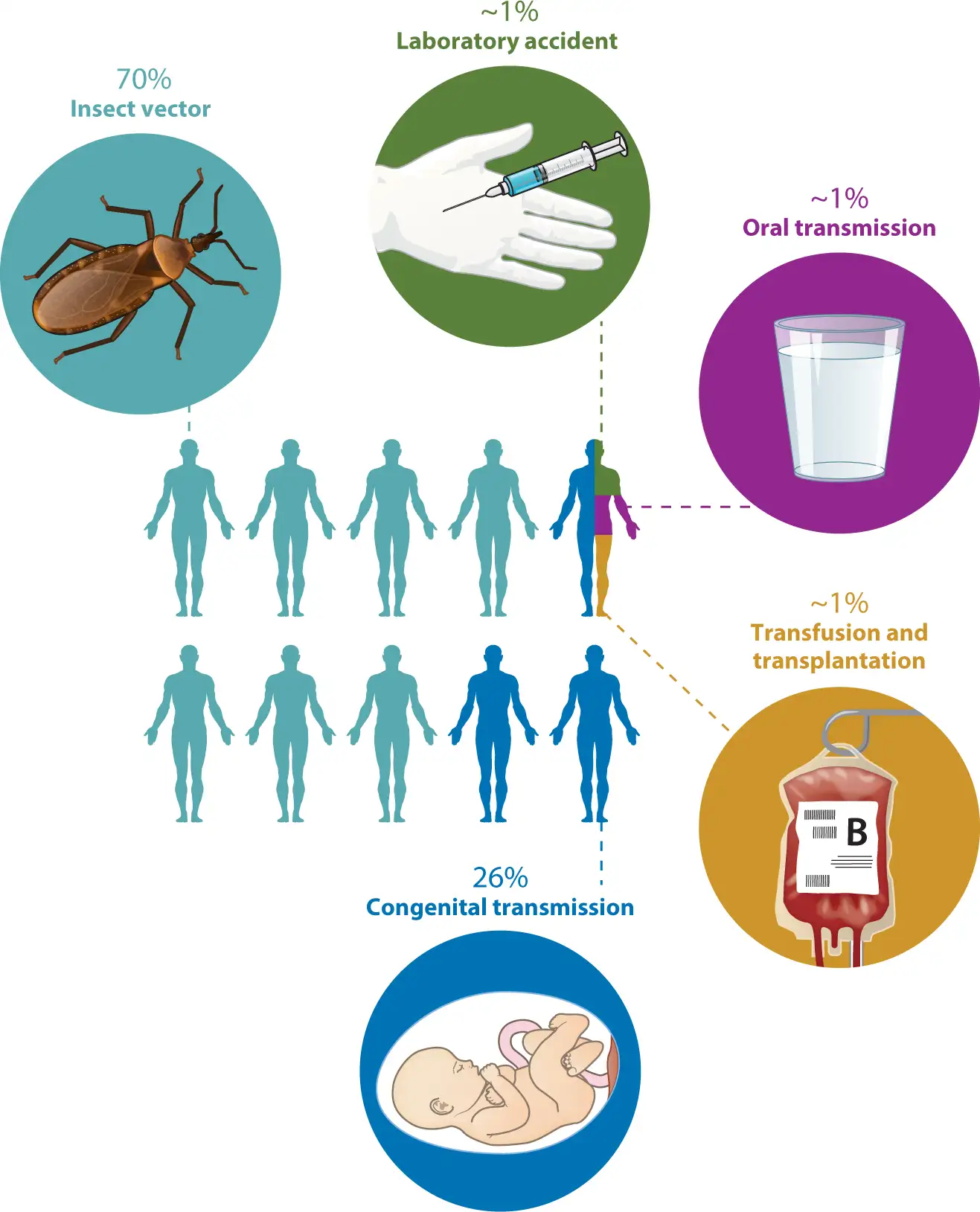
锥蝽有一个独特的生理特征:它们在吸血的同时会排便。这看似是一个奇怪的进化设计,但实际上有着深刻的生态学意义。为了腾出空间容纳新的血液餐,它们必须排出旧的废物。而正是在这些粪便中,潜伏着数以千计的克氏锥虫感染性形态——后循环锥鞭毛体。当受害者在睡梦中感觉到瘙痒并抓挠叮咬部位时,就无意中将含有寄生虫的粪便擦入伤口或粘膜,感染就此发生。这就是为什么恰加斯病的传播不是通过昆虫的唾液,而是通过它们的粪便——这与蚊子传播疟疾的方式完全不同。
锥蝽从野生环境进入人类家园的过程,是砍伐森林和农业扩张的直接后果。数百万年前,恰加斯病就在野生动物之间通过锥蝽传播而存在。当人类开始砍伐森林、开垦农田时,野生动物——锥蝽原本的宿主——被迫离开,锥蝽不得不寻找新的食物来源。人居周围的鸡舍、猪圈和牲口棚成为了它们的新猎场,而最终,它们进入了人类住宅。泥砖房的裂缝、茅草屋顶、土坯墙壁,都成为了锥蝽白天的藏身之处。在那些最贫穷的农村地区,房屋结构简陋、缺乏粉刷,锥蝽可以轻易地找到栖身之所,在墙壁缝隙中建立庞大的群落。一只雌性锥蝽一生可以产下数百枚卵,一个严重的房屋侵染可以容纳数百甚至上千只锥蝽。
显微镜下的幽灵
克氏锥虫是一种单细胞鞭毛虫,属于动基体目锥虫科。它的名字来自希腊语"tryp anon"(钻孔)和"soma"(身体),描述了它蠕动的运动方式;种加词"cruzi"则是为了纪念奥斯瓦尔多·克鲁兹。这个微小的生物体长度仅为12-30微米,却拥有令人惊叹的复杂生命周期和适应能力。
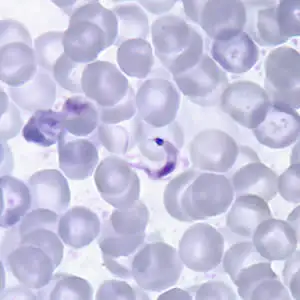
克氏锥虫的生命周期涉及两种宿主——锥蝽和脊椎动物——以及三种不同的形态:上鞭毛体、锥鞭毛体和无鞭毛体。在锥蝽的中肠中,被摄入的血液锥鞭毛体转化为上鞭毛体,开始繁殖。这些上鞭毛体向锥蝽的后肠迁移,在那里分化为具有感染性的后循环锥鞭毛体。当锥蝽再次吸血并排便时,这些后循环锥鞭毛体就随粪便排出,等待进入新的宿主。
一旦进入哺乳动物宿主体内,后循环锥鞭毛体可以侵入多种细胞类型。事实上,几乎任何有核细胞都可能被克氏锥虫感染,包括心肌细胞、内皮细胞、神经元、成纤维细胞和脂肪细胞。这种广泛的细胞嗜性是克氏锥虫能够影响多个器官系统的根本原因。进入细胞后,锥鞭毛体分化为无鞭毛体——这是寄生虫在哺乳动物宿主体内唯一进行繁殖的阶段。无鞭毛体通过二分裂大量增殖,最终重新分化为锥鞭毛体,冲破宿主细胞释放到血液循环中,去感染新的细胞或被新的锥蝽摄入。
在显微镜下,血液中的锥鞭毛体呈现出独特的C形或S形,有一个大的亚末端或末端动基体、一个位于中央的细胞核、一条波动膜和一根沿膜延伸的鞭毛。动基体是克氏锥虫最显著的特征之一,它是一个含有大量DNA的细胞器,负责产生鞭毛运动所需的能量。这个动基体相对较大,是区分克氏锥虫与其他感染人类的锥虫物种的关键特征。
克氏锥虫具有惊人的遗传多样性,被分为至少七个离散分型单位(DTU),命名为TcI至TcVI以及Tcbat。这些基因型在地理分布、宿主特异性和致病性上都有所不同。例如,TcI主要流行于北美和南美北部地区,与野生传播循环相关;而TcII、TcV和TcVI则主要分布在南锥体地区,与家居传播和慢性心脏病、消化道病变的发生率相关。这种基因型的差异可能解释了为什么恰加斯病在不同地区呈现出不同的临床特征。
急性期:无声的入侵
恰加斯病的临床病程分为急性期和慢性期。急性期从感染开始,持续约2个月,但大多数感染者(约90%)完全没有症状或仅有轻微的非特异性症状——低热、疲劳、头痛、肌肉疼痛、食欲不振,这些症状很容易被误认为是普通的病毒感染。这种无症状的特征使得恰加斯病成为医学史上最难以早期发现的疾病之一。大多数人根本不知道自己被感染了,他们继续生活,毫无觉察地成为了这个沉默杀手的宿主。
然而,在某些情况下,急性感染会留下一些独特的痕迹。当克氏锥虫通过皮肤伤口进入时,可能在感染部位形成一个红肿的硬结,称为"恰加斯肿"(chagoma)。更加特征性的表现发生在寄生虫通过眼结膜感染时:患者的一侧眼睑会出现无痛性肿胀,伴有结膜炎,这就是著名的"罗马尼亚征"(Romaña’s sign),以阿根廷医生塞西利奥·罗马尼亚的名字命名。这个征象在1-2周后出现,是急性恰加斯病最可靠的诊断线索之一。但即便如此,许多患者和医生也不会联想到恰加斯病——这种疾病在农村贫困人群中太过常见,以至于人们习以为常。

在极少数情况下(约1-5%),急性感染会导致严重的、可能致命的疾病。患者可能发展为急性心肌炎,出现心律失常、心包积液甚至心力衰竭;也可能发生脑膜脑炎,这是儿童急性恰加斯病最常见的死亡原因。这些严重病例的病死率可以高达5-10%,但幸运的是,绝大多数急性感染会自行缓解,患者进入一个漫长的、看似平静的阶段——慢性期的"未定型"阶段。
慢性期:三十年的沉默
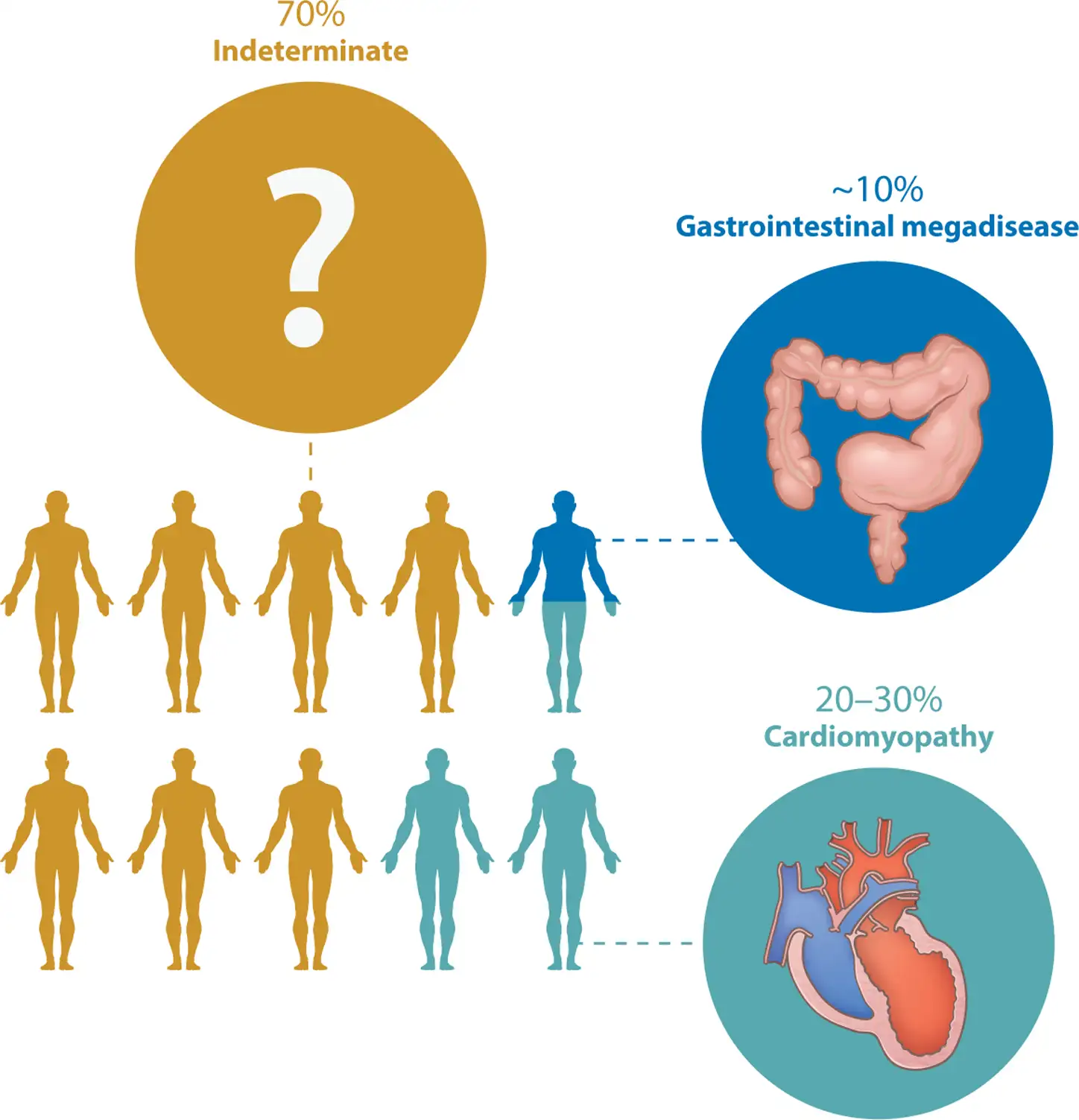
急性期过后,如果未经治疗,感染者将终生携带克氏锥虫。大约70%的人将永远保持"未定型"状态——他们血清学检测阳性,证明体内有针对克氏锥虫的抗体,但没有任何器官功能损害的症状。这些人可以正常生活、工作、繁衍后代,完全不知道自己体内潜伏着一个定时炸弹。然而,剩下的30%将在感染后的10到30年间,逐渐发展出严重的器官损害——心脏或消化系统,或两者兼有。这个过程如此缓慢而隐秘,以至于当症状最终出现时,患者早已忘记了童年时期那只"在脸上爬过的虫子",医生也鲜少会将一个中年人的心力衰竭与几十年前的一次昆虫叮咬联系起来。
慢性恰加斯病的临床表现因地理区域而异。在南锥体地区(巴西、阿根廷、智利、巴拉圭、乌拉圭、玻利维亚),心脏病和消化道病变都很常见;而在北半球(中美洲、墨西哥、南美北部),心脏病是主要的临床表现,消化道病变极为罕见。这种差异被认为与克氏锥虫不同基因型的致病性差异有关。
心脏:沉默杀手的终极目标
恰加斯心脏病是慢性恰加斯病最常见、最严重的表现形式,也是该病导致死亡的主要原因。它是一种炎症性心肌病,在20-30%的慢性感染者中发展,通常在初次感染后20-30年才出现症状。这个过程极其缓慢而隐蔽:在症状出现之前,心肌已经历了多年的进行性损伤。
慢性恰加斯心脏病的病理特征是独特而复杂的。肉眼观察,心脏通常呈现全局性扩大,心室扩张比肥厚更为明显,使心脏呈现球形外观。心外膜可能有密集的纤维炎性斑块,沿着冠状动脉分布,有时呈"念珠状"排列。最具特征性的发现之一是左心室心尖部的壁变薄并膨出,形成动脉瘤——这在其他类型的心肌病中很少见到。这些动脉瘤内常有附壁血栓,是血栓栓塞事件的重要来源。
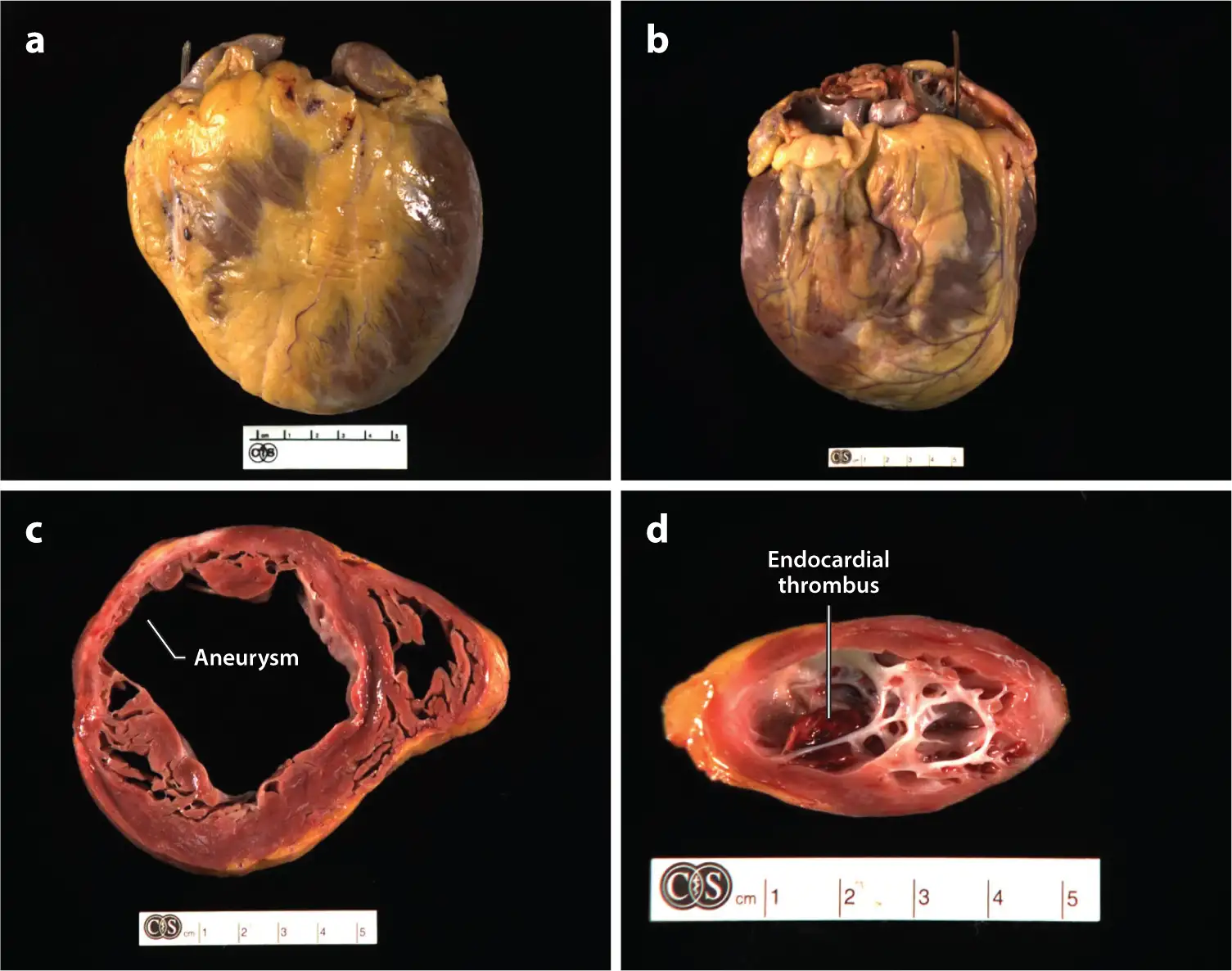
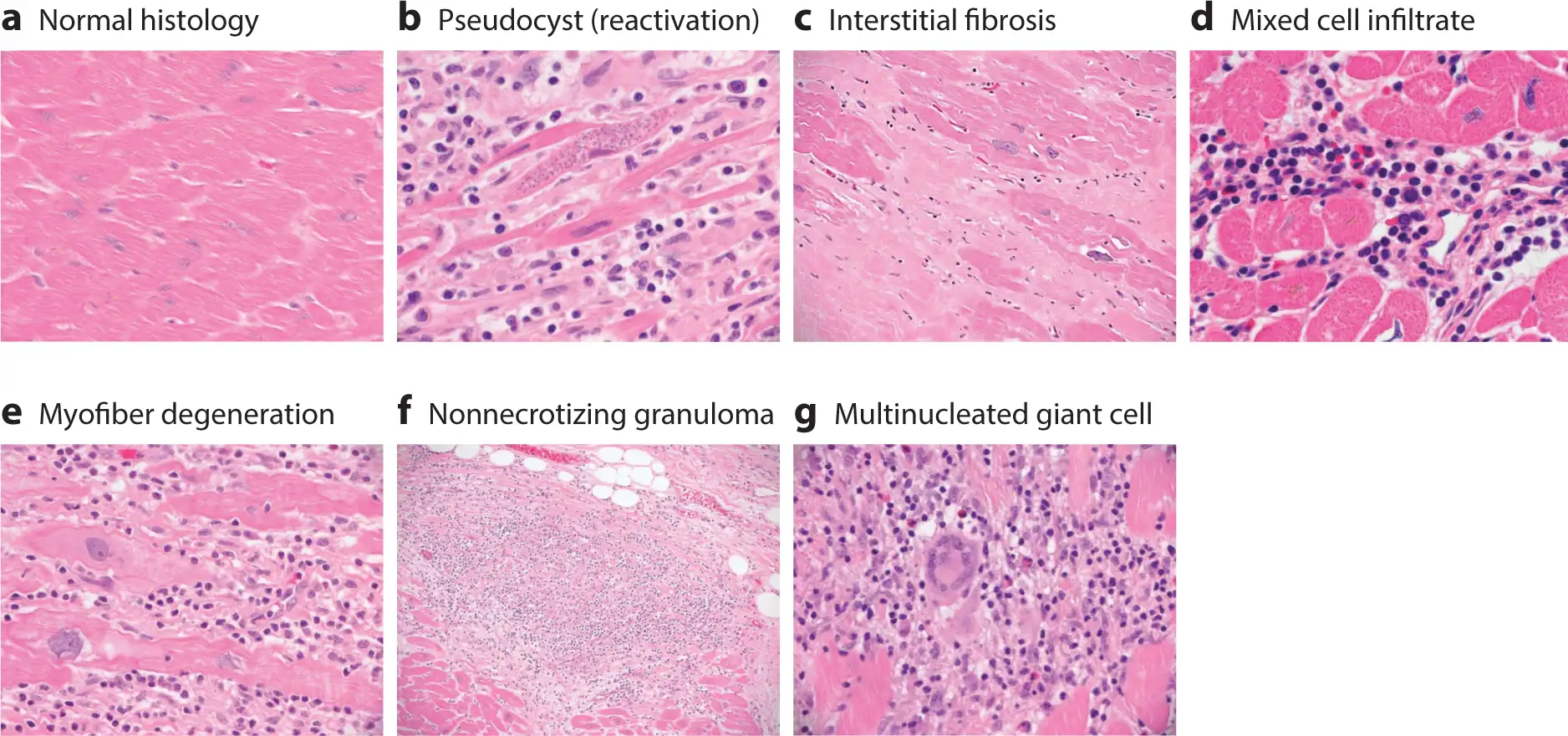
显微镜下,恰加斯心脏病的组织学图像几乎包含了心肌炎的所有可能表现:局灶性或弥漫性的单核细胞浸润、心肌纤维变性、肌纤维溶解、间质纤维化、肌纤维肥大。炎症细胞主要由T细胞和巨噬细胞组成,伴有少量嗜酸性粒细胞、浆细胞和肥大细胞。一个显著的特征是:与急性期不同,慢性期的寄生虫在常规显微镜下几乎看不到——即使使用免疫组化或PCR技术,也只有约57%的心脏组织能检测到克氏锥虫DNA。寄生虫如此稀少,却造成了如此严重的损害,这正是恰加斯心脏病最令人困惑的谜团之一。
临床症状的出现通常标志着疾病已经相当晚期。患者可能经历心悸、晕厥(由心律失常引起)、呼吸困难(心力衰竭的表现),或突发中风(心内血栓脱落)。最令人不寒而栗的是,许多恰加斯心脏病患者的第一个症状就是猝死——由恶性室性心律失常导致的心脏骤停。据统计,猝死占恰加斯心脏病死亡原因的60%,是这种疾病最常见的死亡方式。一个人可能在感染30年后毫无预警地倒下,而直到尸检时,医生才发现他的心脏已经伤痕累累。
恰加斯心脏病的另一个独特之处在于它对心脏传导系统的损害。病变经常累及房室结和希氏束,导致各种程度的心脏传导阻滞。右束支传导阻滞合并左前分支阻滞是恰加斯心脏病的典型心电图表现,被称为"恰加斯病心电图三联征"。这种传导系统受损的模式解释了为什么许多患者需要植入心脏起搏器。
消化系统:从巨食管到巨结肠
在南锥体地区,约10-21%的慢性恰加斯病患者会出现消化系统症状,主要是巨食管和巨结肠。这些病变的发生机制与心脏病不同:它们是由于肠神经丛(奥厄巴赫神经丛和迈斯纳神经丛)的神经元被破坏所致。当控制消化道运动的神经细胞大量死亡,食管或结肠就会失去正常的蠕动能力,逐渐扩张、延长,最终形成巨大的、功能失调的器官。
巨食管是最常见的消化系统表现。患者最早的症状通常是吞咽困难——感觉食物卡在胸骨后方。随着疾病进展,吞咽困难加重,患者可能出现反流、胸痛、咳嗽(尤其是夜间平卧时)、体重下降。在晚期,食管可以扩张到惊人的程度,在胸部X光片上呈现为一个巨大的纵隔阴影,内有气液平面。食物滞留还增加了食管癌的风险。
巨结肠的症状主要是顽固性便秘,可能持续数周甚至数月。患者可能需要反复使用泻药或灌肠才能排便。严重时,结肠可以扩张到占据整个腹腔,甚至导致肠扭转——一种需要紧急手术的危及生命的并发症。与巨食管一样,巨结肠也是不可逆的结构性改变,严重病例可能需要手术切除。
这些消化道病变的地理分布很有趣:它们几乎只出现在赤道以南地区,特别是从巴西中部到南锥体国家的地带。研究者认为,这与当地流行的克氏锥虫基因型有关——TcII、TcV和TcVI似乎更容易引起消化道病变。另一个假说是环境因素或宿主遗传背景可能影响病变类型。
免疫逃逸:一场细胞层面的战争
克氏锥虫能够在宿主体内长期存活并造成慢性损害,其免疫逃逸机制是理解恰加斯病病理学的关键。这个微小的寄生虫在与哺乳动物免疫系统的长期进化斗争中,发展出了一套令人叹为观止的生存策略。
首先,克氏锥虫能够抵抗补体系统的攻击。补体是人体先天免疫的重要组成部分,能够直接裂解入侵的病原体。大多数锥鞭毛体对补体介导的裂解具有抵抗力,这是因为它们的表面覆盖着特殊的糖蛋白,能够抑制补体的激活。有趣的是,研究发现补体沉积反而可能促进克氏锥虫入侵宿主细胞——寄生虫利用补体片段作为"桥梁",更容易进入细胞。
其次,克氏锥虫能够调控宿主的免疫反应。寄生虫分泌的钙网蛋白(TcCalr)是一种多功能蛋白,能够抑制补体激活、促进寄生虫入侵细胞、并调控宿主的免疫反应。克氏锥虫还产生一种模拟宿主转化生长因子-β(TGF-β)的分子,能够诱导宿主细胞表达有利于寄生虫入侵的表面受体。
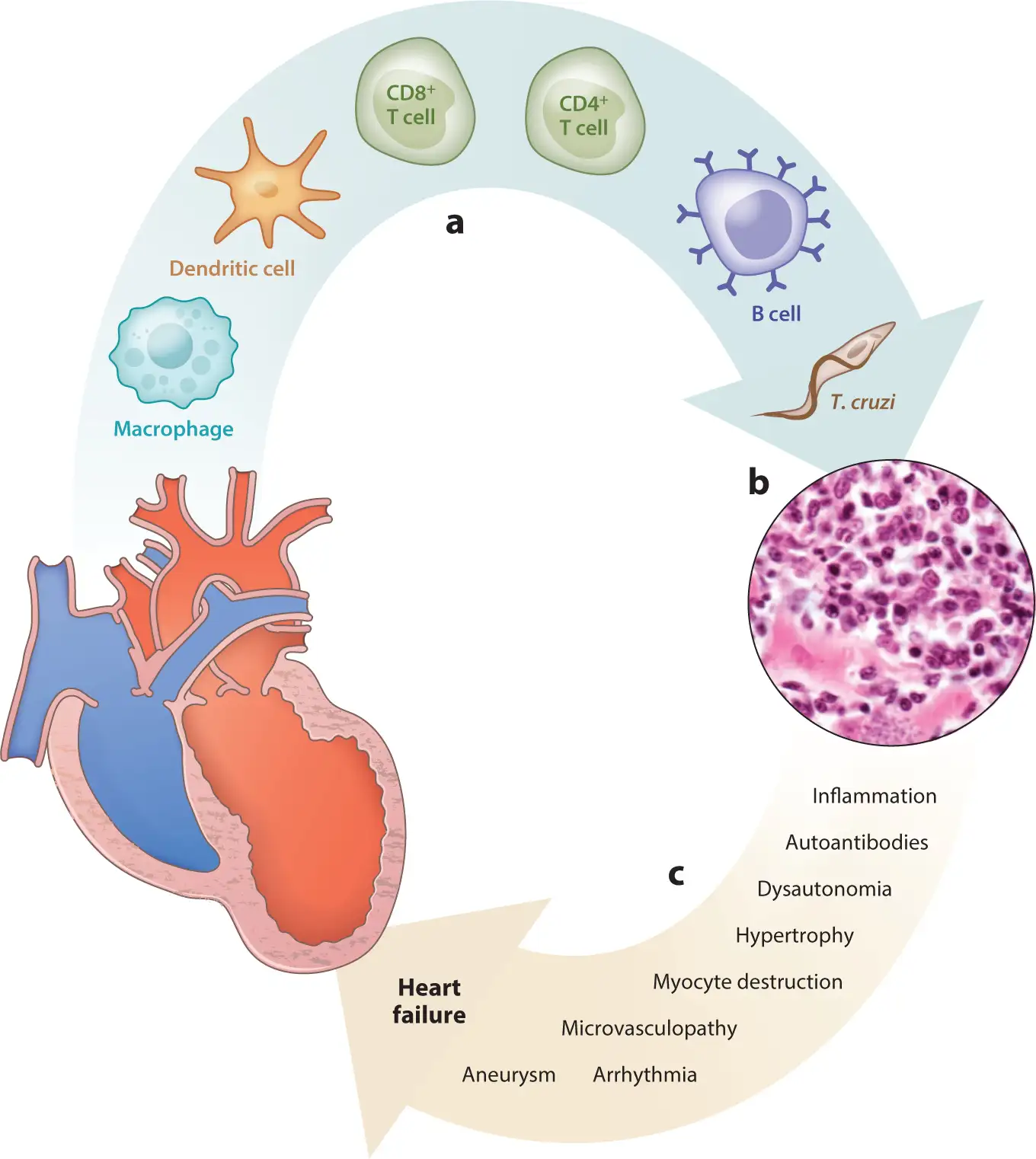
第三,分子模拟可能是慢性恰加斯病自身免疫反应的基础。克氏锥虫的某些抗原与宿主蛋白质具有相似性,当免疫系统攻击寄生虫时,可能产生交叉反应,攻击宿主自身的组织。例如,研究发现克氏锥虫的β-微管蛋白与人类β-微管蛋白存在分子模拟,可能导致针对心肌细胞的自身免疫反应。然而,这一理论仍有争议,因为自身免疫反应通常在清除寄生虫后消失,而恰加斯心脏病的炎症却持续存在。
第四,克氏锥虫能够将其动基体DNA(kDNA)插入宿主细胞基因组——这是一种罕见的水平基因转移现象。被插入的kDNA可以垂直遗传给后代细胞,在小鸡实验中,携带插入kDNA的后代即使没有活寄生虫也会出现心脏病症状。在人类中,也发现了五个家族存在kDNA整合现象。这一发现可能为理解没有活寄生虫存在时炎症仍持续存在的现象提供了线索。
诊断:在沉默中寻找线索
恰加斯病的诊断方法取决于疾病的阶段。在急性期,寄生虫可以在血液中大量存在,通过显微镜检查新鲜血液或吉姆萨染色的厚薄血涂片就能看到。锥鞭毛体呈C形或S形,有一个大的动基体和波动膜,这些特征使它们在显微镜下相对容易辨认。然而,即使在急性期,寄生虫血症也不是很高,血涂片的敏感性只有34-85%。使用微血细胞比容离心等浓缩技术可以提高敏感性。
在慢性期,寄生虫血症极低,几乎不可能通过显微镜检测到。此时,诊断主要依靠血清学检测——寻找针对克氏锥虫的抗体。最常用的方法包括酶联免疫吸附试验(ELISA)、免疫荧光抗体试验(IFA)和免疫印迹(Western blot)。世界卫生组织建议使用两种不同原理的血清学检测方法来确认诊断,以减少假阳性的可能性。
分子诊断(PCR)在恰加斯病诊断中的角色正在增长。PCR在急性期和先天性感染的诊断中比显微镜更敏感,也被用于监测器官移植受者和免疫抑制患者的感染或复发。然而,在慢性恰加斯病中,PCR的敏感性有限,因为寄生虫载量太低。血清学检测仍然是慢性期诊断的主要方法。
克氏锥虫在心脏组织中的无鞭毛体(箭头所指):
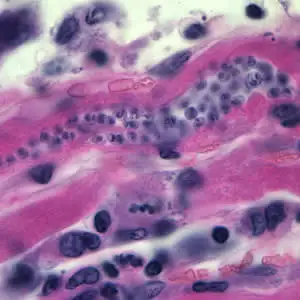
一种古老而独特的诊断方法是"异体诊断"(xenodiagnosis)——让未感染的实验室饲养锥蝽叮咬患者,30-60天后检查这些昆虫的粪便是否有寄生虫。这种方法在慢性期的敏感性约为50%,现在已经很少使用,但在一些流行地区仍有应用。
治疗:两把生锈的武器
恰加斯病的治疗选择极其有限。截至2024年,只有两种药物被批准用于治疗克氏锥虫感染:苯硝唑(benznidazole)和硝呋替莫(nifurtimox)。这两种药物都是在1960年代和1970年代开发的——在恰加斯病被发现半个多世纪后,医学界才有了第一把对抗它的武器。而在此后的五十年里,我们没有开发出任何新的抗恰加斯病药物。
苯硝唑是一种硝基咪唑化合物,通过在克氏锥虫体内产生自由基和活性氧物种来杀死寄生虫。硝呋替莫的作用机制类似,也是通过硝基还原产生活性氧。两种药物对急性期感染都相当有效,治愈率可达50-80%(世界卫生组织称"接近100%")。早期治疗是关键:感染时间越短,治愈的可能性越大。对于先天性感染,如果在出生后第一年内治疗,治愈率接近100%。
然而,这两种药物都有明显的缺点。它们需要每天口服2-3次,持续60-90天,治疗周期长,患者依从性差。更严重的是副作用。苯硝唑最常见的副作用包括皮疹、消化系统问题、食欲下降、乏力和睡眠障碍,约29%的患者因副作用而中断治疗。硝呋替莫的副作用更加严重,影响高达97.5%的用药者,包括食欲不振、体重下降、恶心呕吐,以及各种神经系统问题如情绪变化、失眠、感觉异常和周围神经病变。中断治疗率高达75%。
对于慢性恰加斯病,治疗的争议更大。药物治疗不能逆转已经形成的心脏或消化道损害。2015年发表的一项大型临床试验(BENEFIT研究)显示,对已有心脏病变的慢性恰加斯病患者,苯硝唑治疗并未改善临床结局。然而,对于尚未发展出器官损害的患者,治疗可能减少或延缓疾病的进展。因此,早期发现和早期治疗仍然是恰加斯病管理的核心原则。
对于发展出心脏病或消化道病变的患者,治疗主要是对症处理。心力衰竭的治疗与其他原因的心肌病类似,包括利尿剂、血管紧张素转换酶抑制剂、β受体阻滞剂等。心律失常可能需要抗心律失常药物或植入起搏器/除颤器。严重的心脏病可能需要心脏移植,而恰加斯病患者心脏移植的预后甚至优于其他原因的心肌病患者——这可能是因为慢性感染导致的免疫抑制状态减少了排斥反应。巨食管和巨结肠的严重病例可能需要手术治疗。
全球流行:从雨林到世界
恰加斯病是全球最被忽视的热带病之一。根据2019年的数据,全世界约有650万人感染克氏锥虫,每年新增约17.3万例感染,造成约9490人死亡。疾病每年导致超过80万残疾调整生命年(DALYs)的损失。但这些数字很可能被低估,因为大多数感染者从未被诊断。
恰加斯病是21个拉丁美洲大陆国家的流行病,从墨西哥南部一直延伸到阿根廷和智利北部。流行率最高的国家是玻利维亚(6.1%)、阿根廷(3.6%)和巴拉圭(2.1%)。约7500万人生活在感染风险区。在流行地区,恰加斯病不成比例地影响最贫穷的人群——那些住在泥砖房、茅草屋顶、缺乏基本卫生设施的人们。这是一种"穷人的疾病",正因为如此,它长期以来被国际社会忽视。
自1990年代以来,大规模的媒介控制项目和血液筛查使得拉丁美洲的恰加斯病发病率显著下降。传播率从1980年代的峰值下降了67%,死亡率下降了73%以上。乌拉圭(1997年)、智利(1999年)和巴西(2006年)已经通过媒介控制和血液筛查中断了克氏锥虫的传播。这些成就主要归功于"南锥体倡议"(INCOSUR),这是一个由阿根廷、玻利维亚、巴西、智利、巴拉圭和乌拉圭卫生部于1991年共同发起的区域合作项目。
然而,恰加斯病的问题并未消失。在一些地区,如大查科地区(阿根廷、玻利维亚和巴拉圭交界处),媒介传播仍在继续,部分原因是锥蝽对拟除虫菊酯类杀虫剂产生了抗性。在亚马逊地区,口服传播(通过污染的食物或饮料)正在上升,这与森林砍伐和城市化将人们带入与野生锥蝽更密切的接触有关。在委内瑞拉,人道主义危机导致此前已中断传播的地区重新出现病例。
更令人担忧的是,恰加斯病正在全球化。来自拉丁美洲的移民将感染带到了北美、欧洲、亚洲和大洋洲。据估计,美国有约30万感染者,欧洲有约8-12万例。在这些非流行国家,传播主要通过血液制品、器官移植和母婴传播(先天性感染)。美国自2007年开始对献血者进行克氏锥虫筛查,到2025年已在8个州确认了本地获得性病例。一些专家呼吁将恰加斯病重新归类为美国的地方性流行病。
达尔文的谜题
在恰加斯病的历史上,一个最引人入胜的谜题涉及查尔斯·达尔文。1835年,年轻的达尔文乘坐贝格尔号航行到南美洲。在阿根廷,他遭遇了一种当地称为"vinchuca"的昆虫,并在他的《贝格尔号航行记》中详细描述了被咬的经历:“夜晚,我遭受了布宜诺斯艾利斯、门多萨和智利北部的那种巨大黑色虫子的攻击。它们是无翅的,属于一种猎蝽,在非常柔软的床垫上爬行……它们最令人讨厌的是在被咬后的第二或第三天,被咬的地方会肿胀起来……”
达尔文在航行期间和之后饱受慢性疾病的折磨,症状包括心悸、胸痛、乏力、消化问题、头晕、颤抖和抑郁。他在余生中几乎无法工作,经常卧床不起。这些症状困扰了他40年,直到他于1882年去世,享年73岁。一个多世纪以来,医生们提出了各种诊断,从"达尔文病"(一种被认为与他相关的神秘疾病)到卟啉症、乳糖不耐受、克罗恩病、慢性疲劳综合征等。
1959年,一位名叫索尔·贾德森的医生首次提出,达尔文的症状可能与恰加斯病一致。他指出达尔文描述的昆虫叮咬、随后出现的发热,以及多年后出现的心脏和消化道症状,都与恰加斯病的临床过程吻合。达尔文的心脏问题——心电图显示的传导异常、心悸和可能的扩张型心肌病——也可以用恰加斯心脏病解释。
然而,这一假说仍有争议。批评者指出,达尔文的症状不符合恰加斯病的所有特征:他没有明显的巨食管或巨结肠症状,而且他的疾病似乎有波动性,这在恰加斯病中不太常见。另一些人认为,达尔文的症状更可能是心身疾病或惊恐障碍的表现。2010年的一项研究分析了达尔文的症状,认为恰加斯病仍然是一个"合理的可能性",但不能确定。直到今天,达尔文的疾病仍然是一个未解的医学谜题。
尾声
一百多年过去了,从卡洛斯·查加斯在Lassance火车站车厢里发现那个改变他一生的寄生虫,到今天成千上万的研究者仍在努力解开恰加斯病的谜团。这种疾病揭示了人类与寄生虫之间复杂而漫长的斗争:一个微生物如何在数百万年的进化中发展出如此精妙的生存策略,如何在人类的血管和细胞中穿行几十年而不被发现,如何在最终爆发时以最残酷的方式摧毁宿主的心脏。
恰加斯病也是一面镜子,映照出人类社会的深层不平等。它选择性地攻击最脆弱的人群——那些住在简陋房屋中的农村贫困人口、那些没有机会获得早期诊断和治疗的人们、那些被全球卫生议程遗忘的人们。尽管它感染的人数超过许多备受关注的疾病,研究资金却少得可怜。两种治疗药物都已使用半个世纪,新药研发进展缓慢,疫苗遥遥无期。
在21世纪的今天,恰加斯病提醒我们,即使在现代医学取得巨大进步的时代,古老的敌人仍然潜伏在我们周围。那些在深夜爬上睡脸的昆虫,那些在血液中静静游弋的寄生虫,那些在心肌中悄悄积累的伤痕——它们都在提醒我们,人类与病原体的战争远未结束。而在拉丁美洲那些泥砖房的缝隙中,锥蝽仍在等待,准备开始下一个百年的循环。
参考资料
-
Coura JR. Ecoepidemiology, short history and control of Chagas disease in the endemic countries and the new challenge for non-endemic countries. Mem Inst Oswaldo Cruz. 2013;108(7):852-865.
-
Bonney KM, Luthringer DJ, Wargnier AM, et al. Pathology and Pathogenesis of Chagas Heart Disease. Annu Rev Pathol. 2019;14:413-438.
-
Pérez-Molina JA, Molina I. Chagas disease. Lancet. 2018;391(10115):82-94.
-
World Health Organization. Chagas disease (American trypanosomiasis). Fact sheet. 2025.
-
Lidani KCF, Andrade FA, Bavia L, et al. Chagas Disease: From Discovery to a Worldwide Health Problem. Front Public Health. 2019;7:166.
-
Centers for Disease Control and Prevention. DPDx - American Trypanosomiasis.
-
Nardy AF, Freire-de-Lima CG, Morrot A. Immune Evasion Strategies of Trypanosoma cruzi. J Immunol Res. 2015;2015:178947.
-
Schofield CJ, Dias JC. The Southern Cone Initiative against Chagas disease. Adv Parasitol. 1999;42:1-27.
-
Bern C, Montgomery SP, Herwaldt BL, et al. Evaluation and Treatment of Chagas Disease in the United States: A Systematic Review. JAMA. 2007;298(18):2171-2181.
-
Botto-Mahan C, Cattan PE, Medel R. Was Chagas disease responsible for Darwin’s illness? The overlooked eco-epidemiological context in Chile. Parasitol Int. 2021;80:102225.