1779年的某个清晨,开罗的街道上弥漫着一种诡异的氛围。原本熙熙攘攘的集市变得冷清,不是因为战争或饥荒,而是因为一种奇怪的疾病正在城市中蔓延。患者们描述的症状令人毛骨悚然:高烧不退、剧烈的头痛、眼球后方仿佛有人在用烧红的针穿刺、全身的骨头像是被一寸寸敲碎。当时的医生们从未见过如此剧烈的疼痛,他们给这种疾病起了一个形象而恐怖的名字——“断骨热”。
几乎在同一时间,遥远的雅加达和费城也报告了类似的疫情。这是人类历史上首次有明确记录的登革热大流行。然而,当时没有人知道,这种疾病将在接下来的两个半世纪里,成为人类与蚊子之间最漫长、最残酷的战争之一。今天,登革热已成为全球最常见的虫媒病毒疾病,每年感染约四亿人,导致约两万人死亡。它最令人胆寒的特征,不是它传播的广泛性,而是它独特的"背叛"机制——它能够利用人体免疫系统产生的抗体,作为入侵细胞的钥匙,让曾经保护你的盾牌变成刺向自己的利刃。
四张面孔的幽灵:登革热病毒的分子解剖
登革热病毒属于黄病毒科黄病毒属,与黄热病病毒、西尼罗河病毒和寨卡病毒是近亲。但登革热病毒有一个独特之处:它以四种截然不同的血清型存在于自然界中,分别被命名为DENV-1、DENV-2、DENV-3和DENV-4。这四种血清型在核苷酸序列上有约30%的差异,就像四张长相相似但性格迥异的面孔。
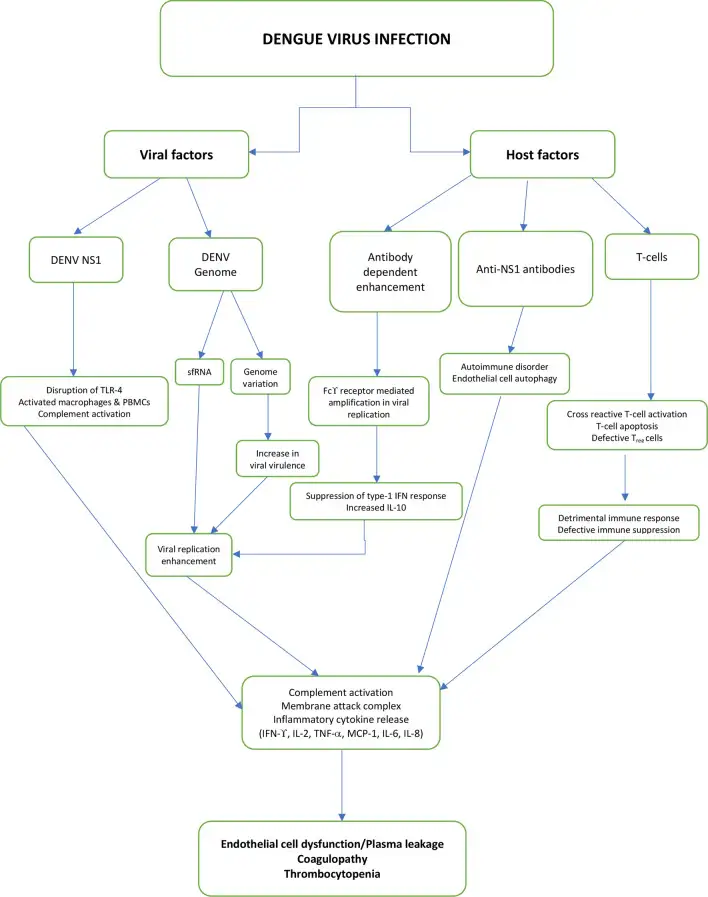
在电子显微镜下,登革热病毒颗粒呈现出完美的球形,直径约50纳米。它的表面覆盖着180个E蛋白(包膜蛋白)二聚体,排列成光滑的二十面体对称结构。这些E蛋白就像病毒的外衣,既是它入侵细胞的钥匙,也是宿主免疫系统识别它的靶标。每个E蛋白单体可以分为三个结构域:EDI位于中央,EDII包含融合环,是病毒与细胞膜融合的关键部位,而EDIII则位于病毒颗粒的最外侧,负责与细胞受体的结合。
病毒的核心是一条约11千碱基的单股正链RNA,编码一个巨大的多聚蛋白。这个多聚蛋白会被切割成三种结构蛋白(C、prM、E)和七种非结构蛋白(NS1、NS2A、NS2B、NS3、NS4A、NS4B、NS5)。其中,NS1蛋白在登革热的致病过程中扮演着关键角色,它不仅参与病毒的复制,还能直接破坏血管内皮细胞,导致致命的血浆渗漏。
1943年,日本科学家Susumu Hotta和Ren Kimura在神户首次成功分离出登革热病毒。他们将患者的血清接种到乳鼠的脑内,观察到病毒在鼠脑中繁殖。这一里程碑式的发现,开启了现代登革热研究的时代。此后,科学家们逐渐揭开了这种病毒的神秘面纱,但每一次发现都伴随着新的谜团。
血管里的背叛:抗体依赖性增强的黑暗机制
登革热最令人费解的特征,是二次感染往往比初次感染更加严重。这在传染病史上几乎是独一无二的——通常情况下,初次感染后产生的抗体会为人体提供持久的保护。但登革热不同,它发明了一种邪恶的"借力打力"策略。
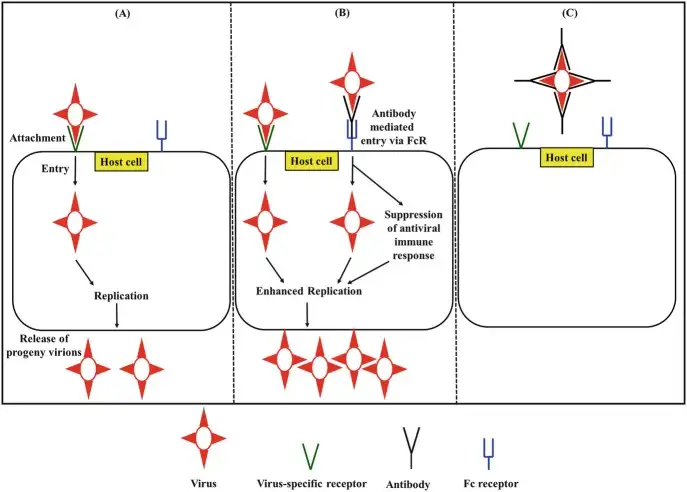
当一个人首次感染某种血清型的登革热病毒时,免疫系统会产生针对该血清型的特异性抗体。这些抗体能够有效地中和病毒,防止其感染细胞。然而,当同一个人后来感染另一种血清型的登革热病毒时,情况就会发生戏剧性的变化。原先产生的抗体虽然也能结合新的病毒,但无法有效地中和它。更糟糕的是,这些"非中和性抗体"会形成病毒-抗体复合物,然后通过抗体的Fc段结合到单核细胞和巨噬细胞表面的Fcγ受体上。
这种现象被称为"抗体依赖性增强"(Antibody-Dependent Enhancement,ADE)。通过这条通路,病毒获得了进入原本不易感染的免疫细胞的"后门"。研究表明,ADE可以使病毒在感染细胞中的复制效率提高100倍以上。更令人震惊的是,最近的研究还发现,当病毒通过ADE途径进入细胞后,它会主动抑制细胞的抗病毒反应,这一过程被称为"内在性ADE"。
1960年代至1970年代,美国科学家Scott Halstead在泰国进行了一系列开创性的研究,首次提出了ADE的概念。他观察到,在曼谷的登革热患者中,出现严重出血热的病例大多是在二次感染的患者中。这一发现彻底改变了人们对登革热发病机制的理解。2017年,一项在尼加拉瓜进行的长达多年的儿童队列研究终于为ADE在人类中的作用提供了确凿的证据。研究发现,体内存在特定浓度抗体的儿童,患重症登革热的风险最高;而抗体浓度极低或极高的儿童,风险反而较低。这意味着,抗体对登革热的影响呈现出一个"倒U型"曲线——太少无法保护,太多能够中和,而处于中间浓度时则会增强感染。
2017年,菲律宾爆发的Dengvaxia疫苗争议,就是ADE最惨痛的现实案例。这款由赛诺菲公司研发的登革热疫苗,在接种前已经感染过登革热的个体中效果良好,但在从未感染过的个体中,却可能增加患重症登革热的风险。当这一风险被揭露时,菲律宾已经有超过80万名学童接种了疫苗,引发了大规模的恐慌和公共卫生危机。这一事件深刻地揭示了登革热疫苗研发的困境:如何设计一种能够同时保护四种血清型的疫苗,而不触发ADE?
血管的哭泣:从发热到休克的死亡之路
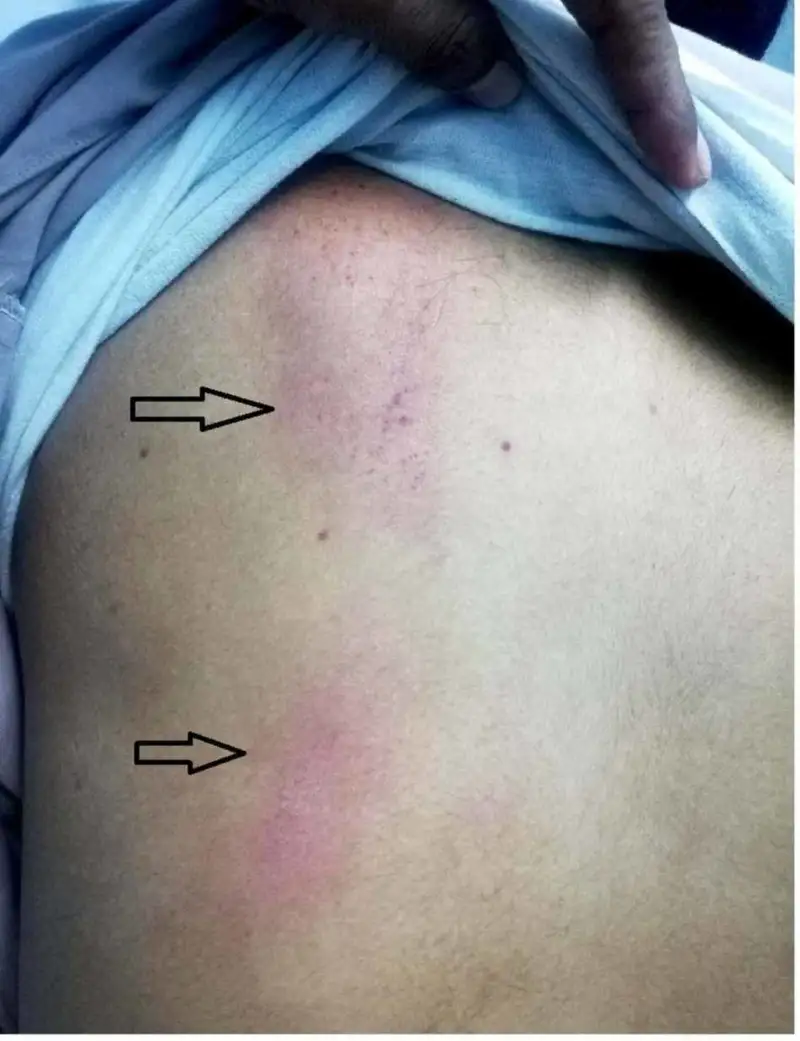
典型的登革热感染分为三个阶段。发热期持续2至7天,患者会出现高热、剧烈头痛、眼球后方疼痛、肌肉和关节酸痛、恶心呕吐等症状。约一半的患者会出现特征性的皮疹——先是从手背和脚背开始,逐渐蔓延到手臂、腿部和躯干,呈现出"红海中的白色岛屿"的独特图案。这是因为皮疹区域血管扩张充血,而某些区域的小血管收缩,形成白色的"岛屿"。
当发热开始消退时,疾病进入关键的"危险期",通常持续24至48小时。这是最危险的时刻。在少数患者中,血管内皮细胞开始渗漏,血浆从血管中渗出到周围组织。患者可能出现严重的腹痛、持续呕吐、牙龈出血、皮肤出现瘀点或瘀斑。如果血管渗漏严重,大量体液在胸腔和腹腔积聚,有效循环血量急剧下降,患者就会进入休克状态。
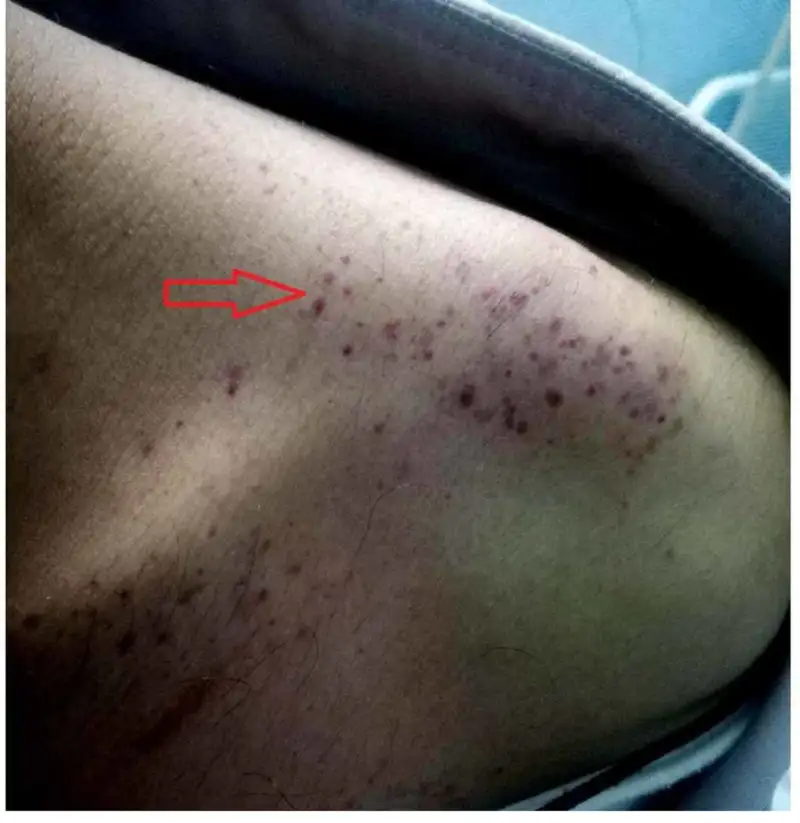
登革热休克综合征(Dengue Shock Syndrome,DSS)是登革热最致命的并发症。患者的血压急剧下降,脉搏微弱,皮肤湿冷,意识模糊。如果不能及时补液,多器官衰竭将在数小时内夺走患者的生命。在未经治疗的情况下,DSS的死亡率可高达20%以上;而及时的正确治疗可以将死亡率降低到1%以下。
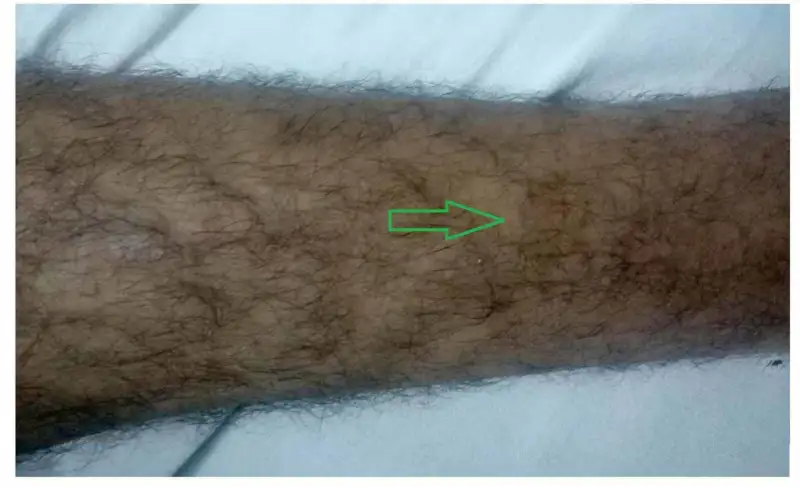
血管渗漏的机制至今仍是活跃的研究领域。目前认为,登革热病毒的NS1蛋白起着核心作用。NS1可以激活补体系统,产生炎症介质;它可以诱导巨噬细胞释放大量促炎细胞因子,如白细胞介素-6(IL-6)和白细胞介素-8(IL-8);它还可以直接破坏血管内皮细胞之间的连接,增加血管通透性。此外,抗NS1抗体还可能与血管内皮细胞发生交叉反应,导致自身免疫损伤。
血小板减少是登革热的另一个标志性特征。正常人的血小板计数在每微升15万至45万之间,而重症登革热患者的血小板可以降至每微升2万以下。血小板减少的机制是多方面的:病毒可以直接抑制骨髓中血小板的产生;抗血小板抗体可以加速血小板的破坏;脾脏对血小球的扣押增加。血小板减少会导致出血倾向,从轻微的牙龈出血、鼻衄,到严重的消化道出血、颅内出血。
从非洲丛林到全球蔓延:伊蚊的殖民史诗
登革热病毒的传播媒介主要是埃及伊蚊(Aedes aegypti),这种小型蚊子有着独特的黑白条纹,胸部背面有一个类似七弦琴形状的白色图案。埃及伊蚊原本生活在非洲的丛林中,以吸食野生动物的血液为生。但随着大航海时代的到来,这种蚊子开始了它的全球殖民之旅。
15世纪至19世纪,跨大西洋奴隶贸易将数百万非洲人运送到美洲。与此同时,埃及伊蚊的卵也随着奴隶船上的水桶漂洋过海,在新大陆安家落户。到17世纪,埃及伊蚊已经遍布加勒比海、中美洲和南美洲的沿海城市。这种蚊子完美地适应了人类的生活环境:它喜欢在人工容器中繁殖——花盆、水桶、废弃轮胎、甚至一个小小的瓶盖中的积水都足以让它繁衍后代。
与许多其他蚊子不同,埃及伊蚊主要在白天活动,尤其是清晨和傍晚。它是人类的专性寄生虫,几乎只吸食人血。一只雌蚊在产卵前需要吸食多次血液,这使得它成为极其高效的疾病传播者。研究表明,一只感染登革热病毒的埃及伊蚊可以保持终身感染能力,病毒在其唾液腺中持续复制。
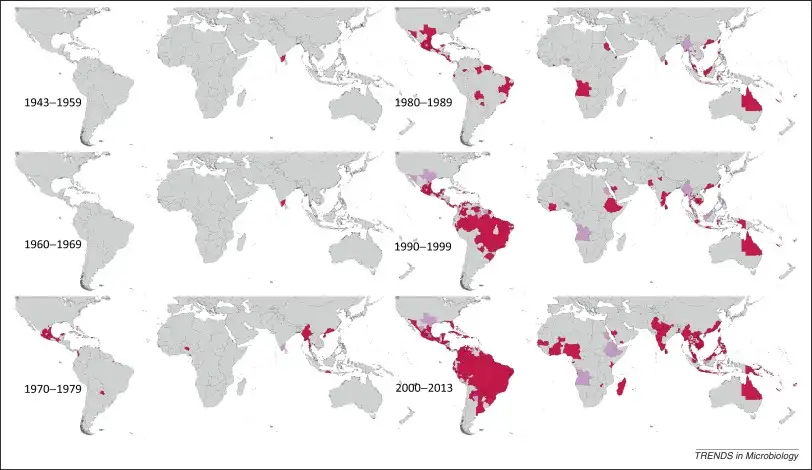
20世纪中期,人类曾有一次消灭埃及伊蚊的机会。1947年,泛美卫生组织启动了大陆性的埃及伊蚊根除计划,目标是消灭传播黄热病的蚊子。在DDT等杀虫剂的助力下,到1962年,18个大陆国家和多个加勒比岛屿成功消灭了埃及伊蚊。然而,随着黄热病威胁的降低和政治意愿的消退,这项计划逐渐瓦解。蚊子迅速卷土重来,而这一次,它带来了登革热。
1981年,古巴经历了美洲历史上首次严重的登革热出血热疫情。超过34万人感染,10312例出血热,158人死亡。这场疫情的罪魁祸首是来自东南亚的DENV-2毒株,它比美洲本土的DENV-2毒株具有更强的致病性。此后,登革热在美洲持续蔓延,病例数呈指数级增长。2024年,美洲地区报告了超过1400万例登革热病例,创历史新高。
亚洲一直是登革热最沉重的负担地区。1953年至1954年,马尼拉首次报告了登革热出血热的流行。在接下来的二十年里,这种疾病蔓延到整个东南亚。印度、印度尼西亚、缅甸、斯里兰卡和泰国位列全球登革热负担最重的30个国家之中。在东南亚的一些城市,儿童在成年前感染登革热几乎是必然的宿命。
气候变化的礼物:登革热的新版图
全球变暖正在为登革热开辟新的疆域。温度是影响登革热传播的关键因素:它决定了蚊子的生存范围、繁殖速度、叮咬频率,以及病毒在蚊子体内的复制速度。研究表明,当气温从28℃上升到32℃时,登革热病毒的传播潜力可以提高一倍以上。
2024年发表的一项研究估计,历史上的气候变化已经使登革热的发病率平均增加了18%。如果全球气温继续上升,到本世纪末,可能有额外10亿人暴露在登革热的威胁之下。登革热正在向温带地区推进:欧洲南部、美国南部、日本和韩国都出现了本地传播的病例。2023年,意大利、法国和西班牙都报告了登革热的本地传播,这在几十年前是不可想象的。
城市化为登革热提供了理想的温床。快速的城市化产生了大量的贫民窟和非正式定居点,这些地区缺乏可靠的自来水供应,居民不得不储存水在容器中——这恰恰是埃及伊蚊最喜欢的繁殖场所。垃圾收集不当产生的废弃容器,也为蚊子提供了无数的家园。登革热已经成为一种典型的"城市病"。
国际旅行和贸易是登革热全球化的催化剂。一个感染登革热的旅行者可以在24小时内飞越半个地球,将病毒带到新的地区。如果当地存在埃及伊蚊,就可能引发本地传播。2013年至2016年期间,一项研究发现,在登革热流行的国家之间旅行的乘客数量增加了约25%,这与全球登革热病例的增加密切相关。
疫苗的困境与希望
登革热疫苗的研发之路充满荆棘。最大的挑战是如何克服ADE:一种理想的登革热疫苗必须能够同时诱导针对所有四种血清型的平衡免疫反应。如果对某种血清型的免疫反应过弱,疫苗本身可能反而增加患重症登革热的风险。
Dengvaxia(CYD-TDV)是全球首个获批的登革热疫苗,由赛诺菲公司开发。它是一种四价减毒活疫苗,使用黄热病病毒作为载体,表达四种登革热病毒的prM和E蛋白。2015年底,Dengvaxia在墨西哥首次获批,随后在多个登革热流行国家上市。然而,2017年,赛诺菲公布了新的分析数据,显示在接种前从未感染过登革热的个体中,疫苗增加了患重症登革热的风险。世界卫生组织随后建议,Dengvaxia只应接种给已经证明曾经感染过登革热的个体。这一限制大大降低了疫苗的实用性,因为在登革热流行地区,很多人并不知道自己的感染史。
2022年,欧洲药品管理局批准了第二种登革热疫苗Qdenga(TAK-003),由武田制药公司开发。Qdenga同样是一种四价减毒活疫苗,但它使用的是DENV-2毒株作为骨架,嵌合了其他三种血清型的prM和E蛋白。临床试验显示,Qdenga在预防登革热住院方面具有良好的效果,且未观察到明显的ADE风险。截至目前,Qdenga已在多个国家获批,并被纳入巴西、印度尼西亚等国家的免疫规划。
另一种有前景的防控策略是利用Wolbachia细菌。Wolbachia是一种常见于昆虫体内的共生细菌,它可以阻止登革热病毒在埃及伊蚊体内复制。世界蚊子计划(World Mosquito Program)在印度尼西亚日惹市进行的大规模试验显示,释放携带Wolbachia的蚊子可以使登革热的发病率降低77%。目前,这种方法已经在十多个国家推广,覆盖超过1000万人。
诊断与治疗的艰难征程
登革热的诊断依赖于实验室检测。NS1抗原检测是最常用的早期诊断方法,它可以在发病后第1至5天检测到病毒的非结构蛋白NS1。IgM/IgG抗体检测则适用于发病后期,但需要注意,二次感染时IgM可能延迟出现或不出现。分子检测(RT-PCR)可以直接检测病毒RNA,具有较高的敏感性和特异性,但需要专业的实验室设备。
登革热目前没有特效的抗病毒药物,治疗主要依靠支持性护理。及时补充体液是预防休克的关键。对于重症患者,可能需要输注血小板和血浆。近年来,科学家们在抗登革热药物研发方面取得了一些进展。2025年,一种名为Mosnodenvir的新型抗病毒药物在临床试验中显示出希望,它能够阻断登革热病毒蛋白之间的相互作用,从而抑制病毒复制。
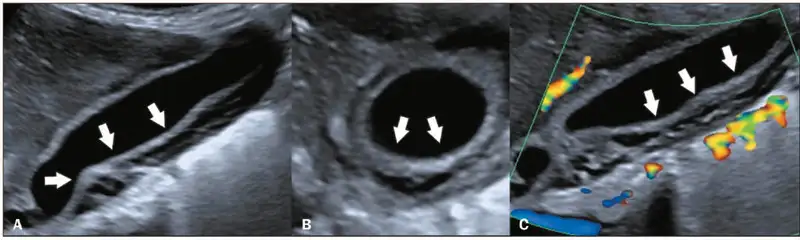
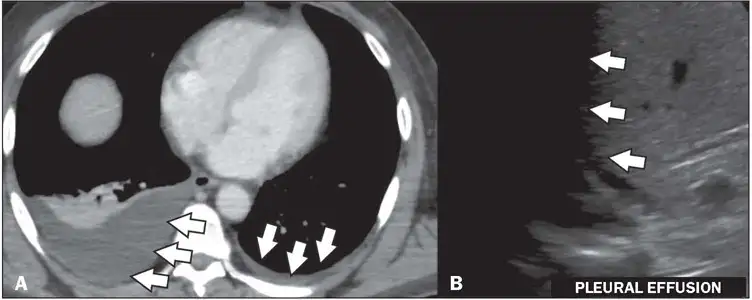
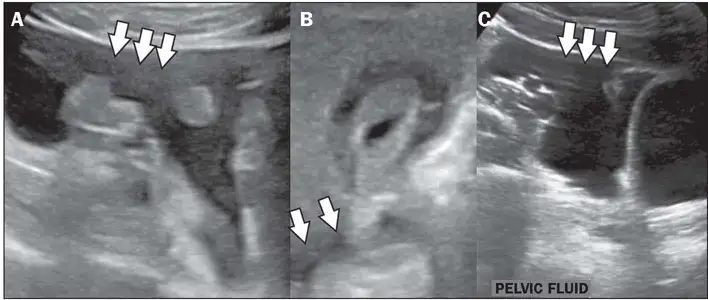
重症登革热的识别至关重要。世界卫生组织定义的预警信号包括:严重腹痛、持续呕吐、体液蓄积(腹水、胸腔积液)、黏膜出血、嗜睡或烦躁不安、肝脏肿大、红细胞压积升高伴血小板下降。任何出现这些预警信号的患者都应立即住院治疗。影像学检查在重症登革热的诊断和监测中发挥着重要作用。超声检查可以快速发现胆囊壁增厚、腹水、胸腔积液等典型的登革热表现,这些发现对于判断疾病严重程度和指导治疗具有重要价值。
未解之谜与未来展望
尽管科学家们对登革热的研究已经持续了80多年,但仍有许多谜团有待解开。为什么有些人感染后会发展为重症,而另一些人只是轻微发热?遗传因素、病毒株的差异、宿主的免疫状态都可能起着作用,但其具体机制尚不清楚。
登革热病毒的起源也是一个有趣的问题。分子钟分析表明,现代四种血清型的分化大约发生在1000至2000年前。这意味着登革热病毒可能是在人类文明较为成熟的时期才开始从猴类病毒演化而来的。然而,这个时间点也存在争议,一些研究认为分化时间可能更早。
气候变化、城市化和全球化正在重新塑造登革热的流行病学版图。新的人群将首次面对这种疾病,新的地区将成为传播的温床。与此同时,科学也在奋起直追:更安全的疫苗、更有效的药物、更智能的蚊虫控制策略正在研发中。人类与登革热的博弈,远未结束。
登革热是一种提醒。它提醒我们,在人与病原体的战争中,敌人的武器也在不断进化。它利用我们的免疫系统攻击我们自己,它利用我们的旅行和贸易网络传播,它利用我们创造的城市环境繁殖。要战胜它,我们需要更深入的科学研究、更有效的公共卫生干预,以及更坚定的全球合作。在21世纪的今天,登革热依然是全球公共卫生面临的重大挑战之一。从18世纪开罗的"断骨热",到今天遍布全球的疫情,这场跨越三百年的战争,还在继续。
参考资料
- World Health Organization. Dengue and severe dengue. Fact Sheet. 2025.
- Bhatt S, et al. The global distribution and burden of dengue. Nature. 2013;496(7446):504-507.
- Halstead SB. Dengue. Lancet. 2007;370(9599):1644-1652.
- Katzelnick LC, et al. Antibody-dependent enhancement of severe dengue disease in humans. Science. 2017;358(6365):929-932.
- Dick OB, et al. The History of Dengue Outbreaks in the Americas. Am J Trop Med Hyg. 2012;87(4):584-593.
- Wilder-Smith A, et al. Dengue. Lancet. 2019;393(10169):350-363.
- Guzman MG, et al. Dengue: a continuing global threat. Nat Rev Microbiol. 2010;8(12 Suppl):S7-S16.
- Anderson KB, et al. Preexisting Antibodies to Dengue Virus and the Risk of Severe Disease. Science. 2024;384(6692):eadj3254.
- Tsegaye AT, et al. Current Understanding of the Pathogenesis of Dengue Virus Infection. J Trop Med. 2021;2021:8898159.
- Rathore APA, et al. Dengue virus-induced autophagy modulates plasma leakage. Nat Commun. 2019;10(1):2848.
- World Mosquito Program. Wolbachia method for dengue control. 2024.
- Takeda Pharmaceutical Company. Qdenga clinical trial data. 2025.
- Simmons CP, et al. Dengue. N Engl J Med. 2012;366(15):1423-1432.
- Murray NE, et al. Epidemiology of dengue: past, present and future prospects. Clin Microbiol Rev. 2013;26(4):664-688.
- Kliks SC, et al. Antibody-dependent enhancement of dengue virus infection in children. J Infect Dis. 1988;158(5):1080-1083.
- Guilarde AO, et al. Dengue and dengue hemorrhagic fever. Lancet Infect Dis. 2008;8(4):225-226.
- Gubler DJ. Dengue and dengue hemorrhagic fever. Clin Microbiol Rev. 1998;11(3):480-496.
- Rigau-Perez JG, et al. Dengue and dengue haemorrhagic fever. Lancet. 1998;352(9132):971-977.
- Malavige GN, et al. Dengue viral infections. Postgrad Med J. 2004;80(948):588-601.
- Whitehead SS, et al. Prospects for a dengue virus vaccine. Nat Rev Microbiol. 2007;5(7):518-528.