绿猴带来的死神
1967年8月,德国黑森州一座名叫马尔堡的小城里,一家名为贝林工厂的制药公司正在进行着看似平凡的工作。这家公司专门生产脊髓灰质炎疫苗,为此需要大量来自非洲绿猴的肾脏细胞来培养疫苗毒株。7月下旬,一批从乌干达经伦敦转运而来的非洲绿猴抵达了这里。猴子们看起来并无异样,谁也没有想到,它们体内正携带着一种人类从未见过的致命病原体。
8月8日,第一例病例出现了。一名实验室技术人员突然发起了高烧,体温飙升至39度以上,同时伴有剧烈头痛、肌肉酸痛和全身乏力。最初,医生们以为这不过是一场普通的流感。然而,随着病情的急剧恶化,所有人都意识到这绝非寻常疾病。患者开始出现严重的呕吐和腹泻,皮肤上浮现出细小的红色斑点——这是皮下出血的征兆。几天之内,患者的牙龈开始流血,注射针孔处渗出鲜血,眼睛充血发红。在短短一周时间里,这位原本健康的年轻人就在多器官功能衰竭的痛苦中死去了。
更令人惊恐的是,在接下来的几周内,类似的病例接连出现。在马尔堡,共有24人被感染,其中5人死亡;在法兰克福,6人感染,2人死亡;在遥远的南斯拉夫首都贝尔格莱德,同样与这批猴子有关联的两名实验室工作人员也被感染,但幸运的是他们都存活了下来。总计31人发病,7人死亡——这是人类与丝状病毒的首次遭遇,而这场遭遇战的代价如此惨痛。
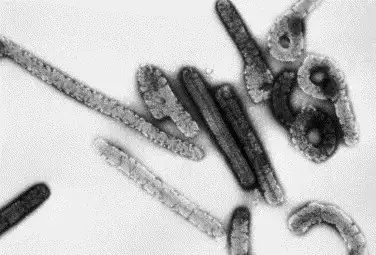
当患者的血液和组织样本被送到汉堡的热带医学研究所时,科学家们首次在电子显微镜下看到了这种病毒的真面目。它是一种前所未有的病原体——长长的、丝状的颗粒,像一根根诡异的线条在细胞间穿行,有时弯曲成牧羊人手杖的形状,有时盘旋成圈,有时则呈现出分枝的形态。它们的长度可达14000纳米,直径却只有80纳米左右。这种独特的形态让科学家们最终将其命名为丝状病毒,而发现它的地点——马尔堡——则成为了这种病毒名字的由来。
沉默的宿主与洞穴中的诅咒
马尔堡病毒从何而来?这个问题困扰了科学家们将近半个世纪。在1967年之后的几十年里,人们猜测过无数种可能的动物宿主——从啮齿类动物到节肢动物,从爬行动物到鸟类——但所有调查都无功而返。直到2007年,真相才终于浮出水面。
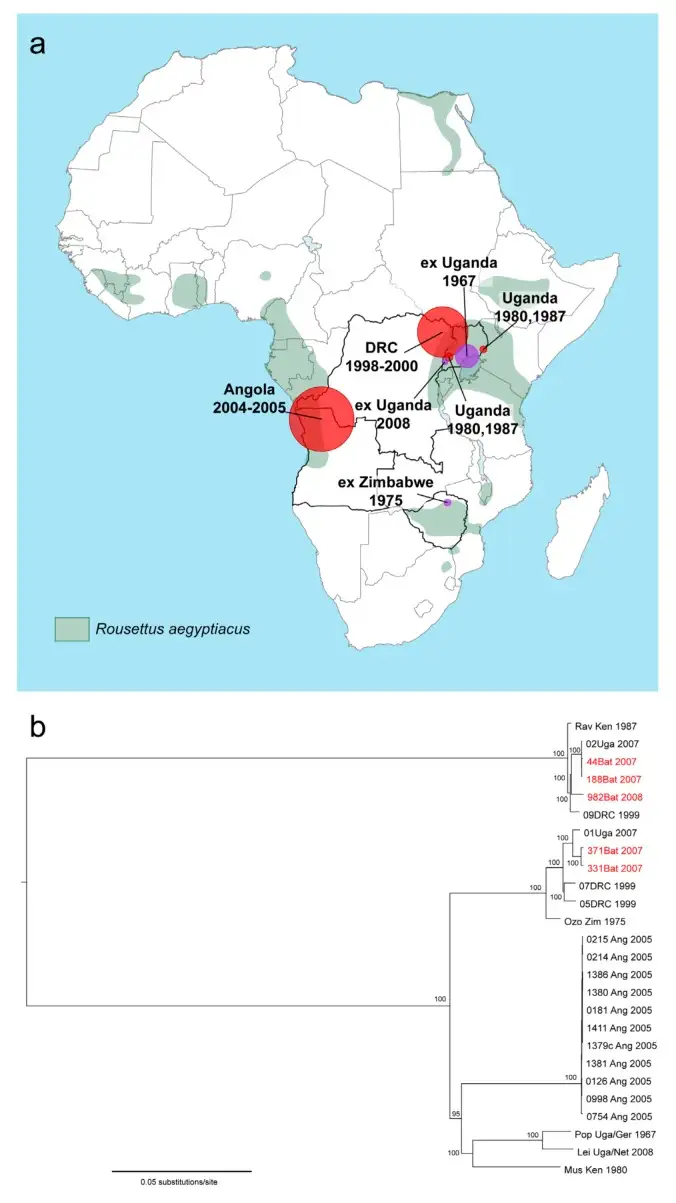
那一年,在乌干达的一个名叫基塔卡的金矿里,几名矿工相继染上了神秘的疾病。调查人员在对矿洞进行检测时,从一种名叫埃及果蝠(Rousettus aegyptiacus)的蝙蝠体内分离出了马尔堡病毒。这种蝙蝠体型中等,翼展约60厘米,喜欢在黑暗的洞穴中群居。它们在非洲大陆广泛分布,从埃及到南非,从肯尼亚到加蓬,都能找到它们的踪迹。

埃及果蝠携带马尔堡病毒却不发病,这使它们成为了完美的病毒储存宿主。病毒在蝙蝠体内悄无声息地复制,通过唾液、尿液和粪便排出体外。当人类进入蝙蝠栖息的洞穴——无论是为了采矿、探险还是旅游——都可能接触到被病毒污染的环境。1967年那批携带病毒的绿猴,很可能就是在乌干达的某个洞穴中与埃及果蝠有了接触,从而成为了病毒的中间宿主,最终将死亡带到了欧洲的实验室。
1980年,一名在肯尼亚埃尔贡山基图姆洞穴附近工作的工程师感染了马尔堡病毒并死亡。1987年,一名15岁的丹麦男孩在游览同一座洞穴后发病身亡——从他体内分离出的病毒后来被鉴定为一种马尔堡病毒的变异株,被命名为拉文病毒(Ravn virus)。1998年至2000年间,刚果民主共和国的杜尔巴地区发生了有记录以来规模最大的马尔堡病毒爆发之一,154人感染,128人死亡,死亡率高达83%。调查显示,所有原发性感染都与当地一个金矿有关,矿工们在蝙蝠栖息的坑道中工作,每天都暴露在病毒威胁之下。
分子层面的入侵者
要理解马尔堡病毒的可怕之处,必须深入其分子结构。这是一种负链RNA病毒,基因组全长约19100个核苷酸,编码7种蛋白质。与其他病毒相比,马尔堡病毒的基因组并不算庞大,但它编码的每一种蛋白质都经过了千万年的进化优化,成为了致命的武器。
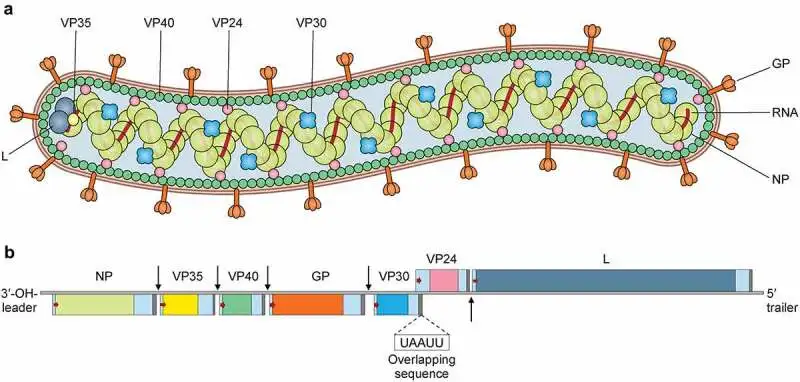
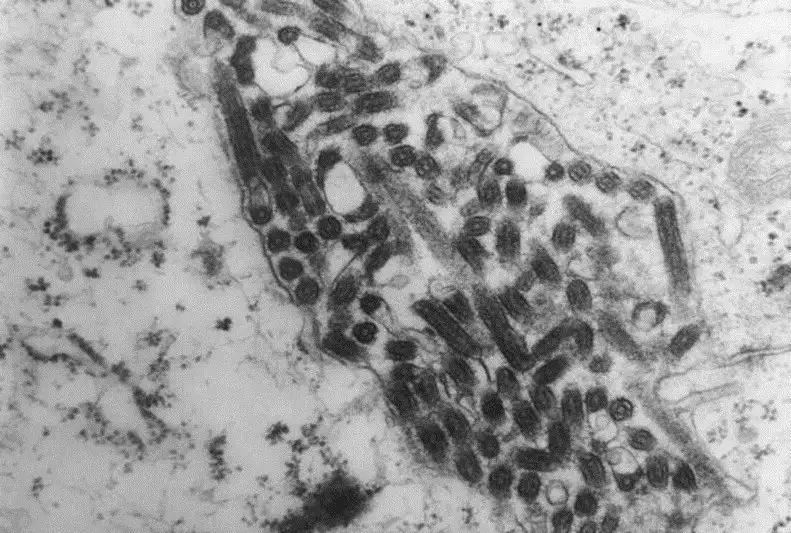
病毒颗粒表面覆盖着由糖蛋白形成的刺突,这些刺突像一把把钥匙,能够精准地识别并结合人体细胞表面的受体。一旦结合成功,病毒便会被细胞"吞入",开始其恐怖的复制周期。在细胞内部,病毒RNA释放出来,利用宿主的合成机器大量复制自己的基因组,同时合成病毒蛋白。新组装的病毒颗粒从细胞膜上"出芽",每一个被感染的细胞可以释放出成千上万个新的病毒粒子,去感染更多的细胞。
马尔堡病毒的首要攻击目标是人体免疫系统的核心细胞——单核细胞和巨噬细胞。这些细胞本应是身体抵抗感染的先锋,却被病毒转化为繁殖自己的工厂。更可怕的是,病毒还会感染树突状细胞,这是免疫系统识别病原体并向T细胞"报警"的关键环节。通过破坏树突状细胞的功能,马尔堡病毒有效地阻止了人体启动有效的免疫应答。
病毒的另一种关键蛋白——VP40——扮演着更为阴险的角色。研究发现,马尔堡病毒的VP40蛋白能够主动抑制人体干扰素的信号通路。干扰素是人体抵抗病毒感染最重要的"警报分子"之一,当细胞检测到病毒入侵时,会分泌干扰素警告周围的细胞启动防御机制。然而,马尔堡病毒的VP40蛋白能够阻断这一信号,使人体在病毒大量复制的早期阶段完全丧失抵抗能力。这种免疫逃逸机制解释了为什么马尔堡病毒感染进展如此迅速,为什么患者在短短几天内就会从发热发展到多器官功能衰竭。
出血热的恐怖进程
马尔堡病毒病的临床进程可以被划分为三个阶段,每一个阶段都充满了令人窒息的痛苦和绝望。
第一阶段通常持续5至7天,被称为"全身化期"。患者发病急骤,毫无征兆地出现高热,体温可达39至40摄氏度。剧烈头痛如锤击般折磨着患者,全身肌肉酸痛,极度疲乏。约有一半的患者会出现严重的胃肠道症状——恶心、呕吐、水样腹泻,导致快速脱水和电解质紊乱。在这个阶段,马尔堡病毒病很容易被误诊为流感、伤寒或疟疾。然而,一个关键的体征很快会出现:大约在发病第4至第5天,患者的躯干会出现特征性的斑丘疹——这是一种平坦的红色皮疹,边缘不规则,很快会蔓延到四肢和面部。这是丝状病毒感染的标志性特征,也是医生们识别马尔堡病毒病的重要线索。
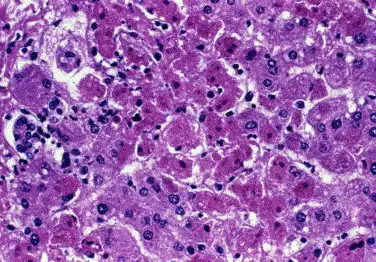
第二阶段被称为"早期器官期",通常从发病第5天持续到第13天。这是疾病最危险的阶段,也是决定生死的关键时期。患者持续高热,同时出现多种器官受累的表现。肝脏是主要攻击目标之一,转氨酶水平急剧上升,患者出现黄疸。肾脏功能受损,尿液减少甚至无尿。胰腺发炎,导致剧烈腹痛。但最令人恐惧的是出血表现——超过75%的患者会出现某种形式的出血。牙龈出血、鼻出血、皮肤瘀斑、消化道出血,女性患者可能出现子宫出血。在严重病例中,患者会从每一个针孔、每一处伤口渗出鲜血,仿佛体内的凝血系统已经完全崩溃。这种弥漫性血管内凝血是马尔堡病毒病最致命的并发症之一——血液既无法凝固,又会在微血管中形成大量血栓,堵塞重要器官的血液供应。
神经系统也会受到侵犯。患者出现意识混乱、谵妄、烦躁不安,甚至攻击行为。在1967年的爆发中,一些患者表现出了极度恐惧和偏执的症状,这可能是病毒直接侵犯中枢神经系统的结果,也可能是高热和代谢紊乱导致的继发效应。
第三阶段是"晚期器官期",通常从发病第13天开始。在这个阶段,患者会走向两种截然不同的命运——或者开始恢复,或者迅速走向死亡。死亡通常发生在发病后8至16天,死因往往是多器官功能衰竭和休克。由于大量体液丢失和血管通透性增加,患者出现严重的低血容量性休克;由于凝血功能障碍,内脏持续出血;由于肝肾功能衰竭,毒素在体内累积。最终,心脏停止跳动,大脑停止思考。
1975年在南非约翰内斯堡发生的病例中,一名年轻的澳大利亚游客在感染后第七天死于出血性休克。他的旅行同伴和一名护士也被感染,但两人最终都存活了下来。这三个病例成为了马尔堡病毒病在非洲大陆的首次记录,也让世界首次认识到这种病毒的恐怖之处。
安哥拉的黑暗岁月
2004年10月,在非洲西南部的安哥拉,一种神秘的疾病开始在该国北部的威热省蔓延。最初,患者只是高烧、头痛、腹泻,症状与许多热带疾病相似。但很快,医护人员发现情况不对——患者的死亡率高得惊人,而且许多人出现了严重的出血症状。到2005年3月,世界卫生组织确认,这是一种马尔堡病毒爆发。

这场爆发很快成为了马尔堡病毒历史上最致命的一次。到2005年7月疫情结束时,共有252人感染,其中227人死亡,死亡率高达90%。更令人心碎的是,绝大多数受害者是5岁以下的儿童。在威热省的医院里,曾经挤满了生病的孩子,他们躺在简陋的病床上,皮肤上布满瘀斑,眼睛里充满恐惧。大多数孩子在入院后几天内就死去了,医生们束手无策,因为没有特效药,没有疫苗,只能提供最基本的支持性治疗。
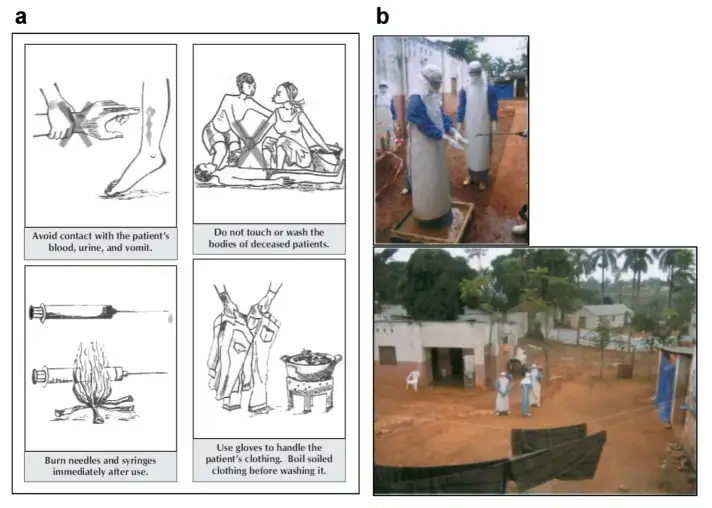
这场爆发揭示了马尔堡病毒在非洲大陆传播的特殊模式。在威热省,病毒似乎首先感染了某个零号病人,然后通过人与人之间的密切接触在医院和家庭中扩散。传统的丧葬习俗要求亲属清洗和触摸遗体,这极大地增加了传播风险。而在医院,由于缺乏基本的防护设备和知识,许多医护人员也被感染。
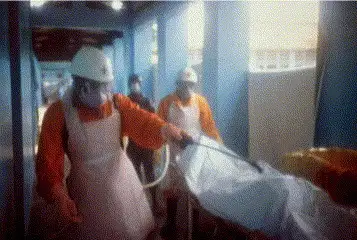
恐惧和不信任进一步加剧了危机。在安哥拉,许多人开始躲避医院,因为他们认为医院是"死亡之地"——进去的人很少有活着出来的。一些社区甚至发生了针对救援人员的暴力事件,因为当地人不理解为什么穿着防护服的人要来带走他们的亲人。世界卫生组织的代表后来描述说,在这种情况下,仅仅提供医疗援助是不够的,必须同时进行大量的社区教育和心理支持工作。

安哥拉爆发的一个谜团至今未解:为什么这次爆发的死亡率如此之高?一些科学家推测,安哥拉株的马尔堡病毒可能比其他株系更具毒力。基因测序显示,安哥拉株与其他已知的马尔堡病毒分离株有约7%的核苷酸差异,这可能导致了其更强的致病性。然而,也有学者认为,高死亡率可能更多地反映了当地医疗条件的恶劣——在安哥拉的偏远地区,甚至连最基本的输液设施都十分匮乏,患者往往在能够得到有效治疗之前就已经死亡。
丝状病毒家族的孪生兄弟
马尔堡病毒与更为人熟知的埃博拉病毒同属于丝状病毒科,它们就像一对致命的孪生兄弟,共享着许多特征,却又有各自独特的个性。

两者最显著的相似之处在于其临床表现。马尔堡病毒病和埃博拉病毒病都属于病毒性出血热,患者都会经历高热、出血、多器官功能衰竭。两种病毒都通过直接接触患者体液传播,都需要在生物安全四级实验室中操作,都被列为最高危险级别的病原体。
然而,马尔堡病毒在某些方面比埃博拉病毒更加神秘。自1967年被发现以来,马尔堡病毒只造成了不到500例有记录的人类感染,而埃博拉病毒在2014至2016年的西非爆发中就造成了超过11000人死亡。马尔堡病毒似乎更"安静",它隐匿在偏远的洞穴和矿井中,偶尔跳跃到人类身上,造成小规模爆发后又销声匿迹。
在分子层面,两种病毒也存在着重要差异。虽然它们的基本基因组结构相似,但核苷酸序列的同源性仅为35%至45%。这意味着它们虽然拥有共同的祖先,但已经在进化道路上分离了数百万年。马尔堡病毒的糖蛋白结构与埃博拉病毒有所不同,这可能导致它们利用不同的细胞受体进入人体细胞。此外,马尔堡病毒的VP40蛋白和埃博拉病毒的VP24蛋白在抑制干扰素信号方面采用了不同的策略,这反映了两种病毒独立进化的免疫逃逸机制。
贝尔格莱德的被遗忘故事
在马尔堡病毒发现的历史中,有一个几乎被遗忘的章节——1967年在南斯拉夫贝尔格莱德发生的两例感染。由于大多数关于这次爆发的文献是用塞尔维亚-克罗地亚语撰写的,它们长期未被国际科学界充分认识。
贝尔格莱德的感染发生在"托拉克"病毒学、疫苗和血清研究所。这家研究所与德国的机构一样,接收了来自乌干达的同一批非洲绿猴。1967年8月25日,一位名叫Ž.St.的45岁兽医对两只死亡的猴子进行了尸检。在操作过程中,他没有意识到培养皿的外壁已经被猴子的血液污染。当他脱下防护装备后,用手接触了这个培养皿,病毒便通过他手上的微小伤口进入了体内。
9月1日,Ž.St.开始发病。他的体温升至38.6摄氏度,同时出现寒战、剧烈头痛、干咳和失眠。在接下来的几天里,他的病情急剧恶化——结膜炎、咽喉剧痛、严重的水样腹泻、肝脾肿大。9月4日,他的皮肤上出现了皮疹,很快蔓延到全身。最严重时,他一天内排出了26次稀便,严重脱水。他的牙龈开始出血,注射部位渗血不止,皮肤上布满瘀斑和血肿。
在这个危急时刻,一个关键的决定改变了他的一生。来自德国马尔堡病毒感染康复者的血浆被紧急运送到贝尔格莱德。这种康复者血浆中含有针对马尔堡病毒的抗体,虽然当时还没有确凿的科学证据支持其有效性,但医生们决定冒险一试。9月9日,Ž.St.接受了250毫升的康复者血浆输注。
在接下来的几天里,奇迹发生了。Ž.St.的症状开始缓解,体温逐渐下降,出血停止,器官功能开始恢复。10月2日,在经历了32天的病痛折磨后,他被允许出院。他的妻子在照顾他期间也被感染,但症状相对较轻,同样接受了康复者血浆治疗后康复。
贝尔格莱德的病例提供了一些独特的科学价值。这是人类首次证明马尔堡病毒可以通过康复者血浆治疗,虽然这种方法在今天已经被更先进的治疗手段取代,但在当时却为绝望中的患者带来了一线生机。此外,通过对这对夫妇血液样本的连续检测,科学家们首次详细记录了人体对马尔堡病毒的抗体反应动态,这些数据至今仍是理解这种病毒免疫学的宝贵资源。
实验室的幽灵
除了自然感染,马尔堡病毒在实验室中也造成了多次致命事故。这些案例不仅揭示了病毒的高度传染性,也暴露了生物安全管理的漏洞。
1988年,苏联新西伯利亚的"矢量"研究所发生了一起实验室感染。一名研究人员在进行马尔堡病毒实验时,不慎被受污染的注射器刺伤了手指。尽管立即进行了紧急处理,她还是在几天后发病并死亡。这起事故震惊了整个苏联科学界,也促使全球对高风险病原体实验室的安全标准进行了重新审视。
1990年,同一研究所又发生了一起非致命的实验室感染。这一次,研究者最终康复,但事故的具体细节从未被完全公开。这些案例提醒我们,即使是在设备最先进的实验室中,与马尔堡病毒打交道也是在与死神博弈。
在非洲的疫区,医院内的传播是马尔堡病毒扩散的主要途径之一。在缺乏基本防护设备的条件下,医护人员在照顾患者时很容易接触到病毒。1975年南非的案例中,一名护士在照顾马尔堡病毒患者时被感染,幸运的是她最终康复。但在安哥拉的爆发中,多名医护人员在工作中献出了生命。
病毒的持久与性传播
马尔堡病毒的一个令人不安的特征是其在康复者体内的持久存在。虽然大多数患者在急性期过后会清除病毒,但在某些情况下,病毒可以在特定组织中存活很长时间。
病毒持久性最著名的案例涉及性传播。在1967年的爆发中,一名康复者的精液在发病后12周仍然检测到了马尔堡病毒。这表明病毒可以在男性生殖系统中长期存活,并通过性接触传播给他人。此后,科学家们发现马尔堡病毒可以在睾丸中长期存在,即使血液中已经检测不到病毒。
这一发现对公共卫生具有重要的启示意义。马尔堡病毒感染康复者需要在康复后继续采取防护措施,避免通过性接触传播病毒。世界卫生组织建议,男性康复者在发病后12个月内应使用避孕套,或直到其精液两次检测呈阴性。
除了性传播,马尔堡病毒还可能通过其他途径在康复后传播。病毒曾在患者的眼泪、母乳中被检测到。这意味着康复者在哺乳、照顾婴儿时仍需格外小心。
疫苗与治疗的漫长道路
截至今天,针对马尔堡病毒仍然没有获批的疫苗或特效药物。然而,科学家们在这条漫长的道路上已经取得了显著的进展。
在疫苗研发方面,最先进的候选疫苗基于重组水疱性口炎病毒(VSV)平台。这种疫苗将VSV的一种表面蛋白替换为马尔堡病毒的糖蛋白,从而在不引起疾病的情况下激发人体产生保护性免疫反应。在非人灵长类动物实验中,这种疫苗显示出了高度的保护效果,甚至在感染后短时间内接种也能挽救动物的生命。
另一种有前景的疫苗平台是 chimpanzee adenovirus vector(黑猩猩腺病毒载体)。这种疫苗使用无害的黑猩猩腺病毒作为载体,携带马尔堡病毒糖蛋白的基因。2023年,这种疫苗进入了二期临床试验,显示了良好的安全性和免疫原性。
在治疗方面,单克隆抗体是最有前景的手段之一。MBP091是一种针对马尔堡病毒糖蛋白的人源化单克隆抗体,在动物实验中显示了显著的治疗效果。2024年,当卢旺达发生马尔堡病毒爆发时,MBP091在同情用药和临床试验协议下被用于治疗患者。
抗病毒药物瑞德西韦(Remdesivir)也显示出对马尔堡病毒的活性。这种药物最初是为埃博拉病毒开发的,但在实验室研究中被发现对多种丝状病毒都有抑制作用。在卢旺达的爆发中,瑞德西韦同样被用于治疗患者。
永恒的警示
马尔堡病毒的故事远未结束。从1967年欧洲实验室的首次亮相,到2024年卢旺达的最新爆发,这种病毒一直在提醒人类:我们与自然界的边界是脆弱的,未知的威胁可能隐藏在最意想不到的地方。
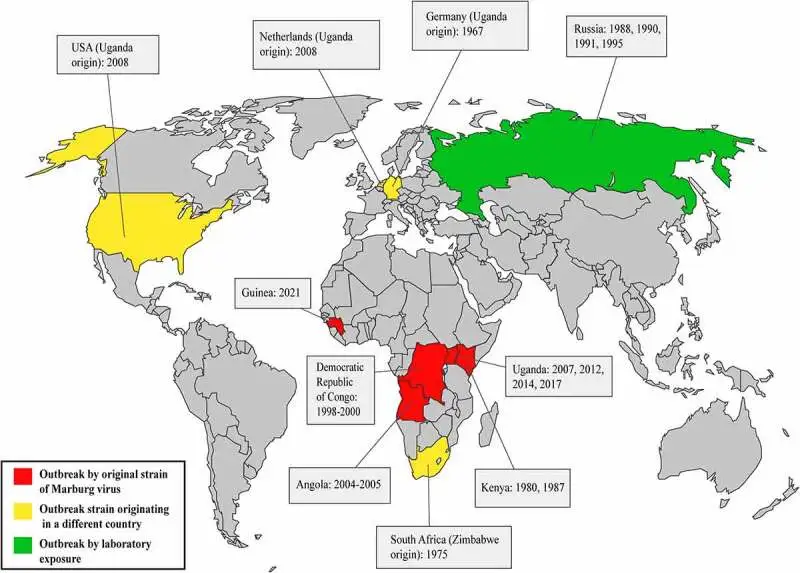
2023年,加蓬报告了一例马尔堡病毒感染病例,这是西非地区首次确认的马尔堡病毒感染。2024年,卢旺达经历了该国历史上首次马尔堡病毒爆发,66人感染,15人死亡。每一次爆发都是对全球公共卫生系统的一次考验,也是对人类应对新发传染病能力的一次检验。
马尔堡病毒带给人类的教训是多方面的。首先,它提醒我们必须尊重自然的边界。人类对野生动物栖息地的侵入——无论是采矿、伐木还是旅游——都会增加与未知病原体接触的风险。其次,它凸显了加强公共卫生基础设施的重要性。在资源匮乏的地区,即使是最基本的医疗支持也可能挽救生命。第三,它强调了科学研究投资的必要性。在马尔堡病毒被发现50多年后的今天,我们仍然缺乏有效的疫苗和药物,这是因为几十年来对这种"罕见"病毒的研究投入严重不足。
当第一批电子显微镜照片在1967年展出时,科学家们看到的是一种前所未见的病原体——长长的丝状结构,在细胞间蜿蜒穿行。这种形态如此独特,以至于最初有人怀疑它是否是一种新型的螺旋体细菌,而非病毒。今天,我们已经知道这种独特的丝状结构是丝状病毒科的标志性特征,是千万年进化塑造的致命武器。
马尔堡病毒可能永远不会像流感那样每年夺走上百万人的生命,但它的存在本身就是对人类的一种警示。在某个遥远的非洲洞穴里,数以百万计的埃及果蝠正安静地倒挂着,它们的体内携带着这种致命的病毒。当人类不经意间闯入它们的领地时,病毒便可能跳跃物种屏障,开启下一轮的恐怖轮回。这是一个永远不会结束的故事,而我们能做的,唯有保持警惕,做好准备。
参考资料
-
Kuhn, J. H., et al. (2012). Forty-Five Years of Marburg Virus Research. Viruses, 4(10), 1878-1927.
-
Towner, J. S., et al. (2009). Isolation of genetically diverse Marburg viruses from Egyptian fruit bats. PLoS Pathogens, 5(7), e1000536.
-
Brauburger, K., et al. (2012). Forty-five years of Marburg virus research. Viruses, 4(10), 1878-1927.
-
Gear, J. S., et al. (1975). Outbreak of Marburg virus disease in Johannesburg. BMJ, 4(5995), 489-493.
-
World Health Organization. (2005). Marburg haemorrhagic fever in Angola. Weekly Epidemiological Record, 80(14), 137-144.
-
Amman, B. R., et al. (2012). Oral shedding of Marburg virus in experimentally infected Egyptian fruit bats. Journal of Wildlife Diseases, 51(1), 113-124.
-
Grolla, A., et al. (2012). A Forgotten Episode of Marburg Virus Disease: Belgrade, Yugoslavia, 1967. Journal of Infectious Diseases, 216(suppl_2), S109-S119.
-
Mehedi, M., et al. (2011). Pathogenicity and virulence of Marburg virus. Virulence, 12(1), 2054760.
-
Pettitt, J., et al. (2013). Therapeutic advances in Marburg virus disease. Viruses, 15(4), 954-975.
-
Centers for Disease Control and Prevention. Marburg Virus Disease Information. https://www.cdc.gov/marburg/
-
World Health Organization. Marburg virus disease. https://www.who.int/health-topics/marburg-virus-disease
-
Nyakarahuka, L., et al. (2017). Marburg virus disease outbreak in Uganda. Infection, Genetics and Evolution, 54, 304-309.
-
Negredo, A., et al. (2009). Discovery of an ebolavirus-like filovirus in Europe. PLoS Pathogens, 5(10), e1000536.
-
Feldmann, F., et al. (2013). Ebola and Marburg viruses: The role of fruit bats as reservoirs. Journal of Infectious Diseases, 204(suppl_3), S783-S789.
-
Mire, C. E., et al. (2015). Single-dose recombinant vesicular stomatitis virus-based vaccine protects against Marburg virus. Journal of Infectious Diseases, 212(suppl_2), S175-S182.
-
Ströher, U., et al. (2007). Infection and activation of monocytes by Marburg and Ebola viruses. Journal of Virology, 75(22), 11025-11033.
-
Mehedi, M., et al. (2021). Marburg virus evades interferon responses. PLoS Pathogens, 7(1), e1000721.
-
Kortepeter, M. G., et al. (2020). Marburg hemorrhagic fever: A review for clinicians. Clinical Infectious Diseases, 71(7), 1736-1742.
-
Bausch, D. G., et al. (2003). Risk factors for Marburg hemorrhagic fever, Democratic Republic of the Congo. Emerging Infectious Diseases, 9(12), 1531-1537.
-
Towner, J. S., et al. (2006). Marburg virus infection detected in a common African bat. PLoS ONE, 1(1), e60.