1937年春天,苏联远东的泰加林深处,一种恐怖的疾病正在蔓延。年轻士兵、铁路工人、伐木者接连倒下,他们先是高烧不退,随即陷入谵妄和昏迷,那些侥幸活下来的人,许多从此瘫痪在床,再也没能站起来。莫斯科的医生们束手无策,他们从未见过如此凶猛的脑部疾病。
这并非战争的创伤,也不是某种已知的瘟疫。这是一种全新的敌人——它藏身于针叶林的阴影中,静默地等待着猎物。当苏联卫生部派遣的探险队终于找到它时,他们揭开的不仅仅是一种疾病的真相,更是人类历史上最隐秘、最致命的病毒战争之一。蜱传脑炎病毒,这个直径仅有五十纳米的杀手,在接下来的一个世纪里,将让数万人付出惨痛的代价。
泰加林深处的死神
1930年代初,苏联远东地区正经历着剧烈的变革。日本占领满洲后,苏联与日本的边境冲突日益频繁,远东的战略地位骤然提升。大批士兵、铁路工人、伐木者被派往这片人迹罕至的原始森林,开垦荒地、修筑铁路、砍伐木材。然而,随着人们的深入,一种诡异的疾病开始在人群中蔓延。
最初只是几例零星的病例。工人们抱怨头痛、发烧,以为是普通的感冒或过度劳累。但很快,症状急剧恶化。患者出现剧烈的颈项强直,意识逐渐模糊,最终陷入深度昏迷。更令人胆寒的是,许多幸存者留下了永久性的瘫痪——有人失去了手臂的活动能力,有人再也无法行走。在最初的病例中,死亡率高达百分之三十以上。
当地医生们从未见过如此凶猛的神经系统疾病。他们尝试了各种治疗方法,从青霉素到磺胺类药物,全都无济于事。疾病的流行呈现出明显的季节性——每年春夏之交最为猖獗,秋天过后便销声匿迹。这种规律性暗示着某种与自然环境相关的传播途径,但究竟是什么?
1937年,苏联人民健康委员会终于决定派遣一支科学探险队前往远东调查。这支队伍由年轻有为的病毒学家列夫·齐尔伯领导,他是苏联第一个医学病毒学实验室的主任。齐尔伯召集了一群才华横溢的年轻研究人员和技术人员,他们分成两个小组,分别在哈巴罗夫斯克边疆区和滨海边疆区的深处开展工作。
那是一片真正与世隔绝的荒野。没有道路,没有电力,没有现成的实验室。科学家们不得不在帐篷里搭建临时的实验设备,用最原始的方法进行研究。白天,他们在森林中采集样本;夜晚,他们在摇曳的油灯下分析数据。蚊虫肆虐,猛兽出没,严酷的自然环境让每一次采集都成为一场冒险。
但这并非他们面临的最大危险。真正的威胁,藏在他们正在研究的疾病本身。
探险队的进展异常迅速。到五月中旬,第一个关键发现诞生了:他们从发热患者的血液中成功分离出一种病毒。更重要的是,他们注意到当地居民在被蜱虫叮咬后更容易发病。当团队成员警告当地人避免蜱虫叮咬后,新发病例明显减少。到了八月中旬,证据已经确凿无疑——这种疾病是由一种病毒引起的,传播媒介是硬蜱属的蜱虫。
然而,胜利的代价是惨痛的。在研究过程中,多名团队成员被感染。其中最令人震惊的是米哈伊尔·丘马科夫的遭遇。这位年轻的病毒学家在解剖一具尸体时不慎切伤了手指,随即感染了病毒。他经历了极其严重的病程——高烧、剧烈头痛、意识模糊,最终留下了右臂永久性瘫痪和听力丧失。
丘马科夫活了下来,但他的右手从此再也无法握住手术刀。然而,这位顽强的科学家并没有被疾病击倒。恰恰相反,这次濒死的经历让他对蜱传脑炎产生了近乎执念的关注。几十年后,正是这位残疾人领导的研究所,将开发出新一代的蜱传脑炎疫苗,拯救无数人的生命。
探险队的成功本该是科学史上的光辉篇章。然而,当齐尔伯和他的同事们带着成果返回莫斯科时,等待他们的不是鲜花和掌声,而是斯大林大清洗的阴影。就在他们取得重大科学发现的同时,齐尔伯和两名女性同事——病毒学家亚历山德拉·谢博尔达耶娃和流行病学家塔玛拉·萨福诺娃——被逮捕,并被指控为日本间谍。他们的名字被从所有科学出版物中删除,直到斯大林死后才得以恢复名誉。
这并非偶然。蜱传脑炎的研究从一开始就与军事和政治纠缠在一起。远东地区的疾病爆发发生在苏联与日本紧张对峙的背景下,而疾病的传播区域恰好与军事战略要地重合。在这种高度敏感的环境中,任何与"外国"沾边的研究都可能引发猜疑。齐尔伯的探险队虽然在科学上取得了巨大成功,却无法逃脱那个时代的政治漩涡。
微观世界的完美杀手
蜱传脑炎病毒属于黄病毒科黄病毒属,这一家族还包括许多臭名昭著的成员:登革病毒、黄热病毒、西尼罗病毒、寨卡病毒。它们共享一个共同的特征——能够引起严重的人类疾病,却以截然不同的方式攻击人体。

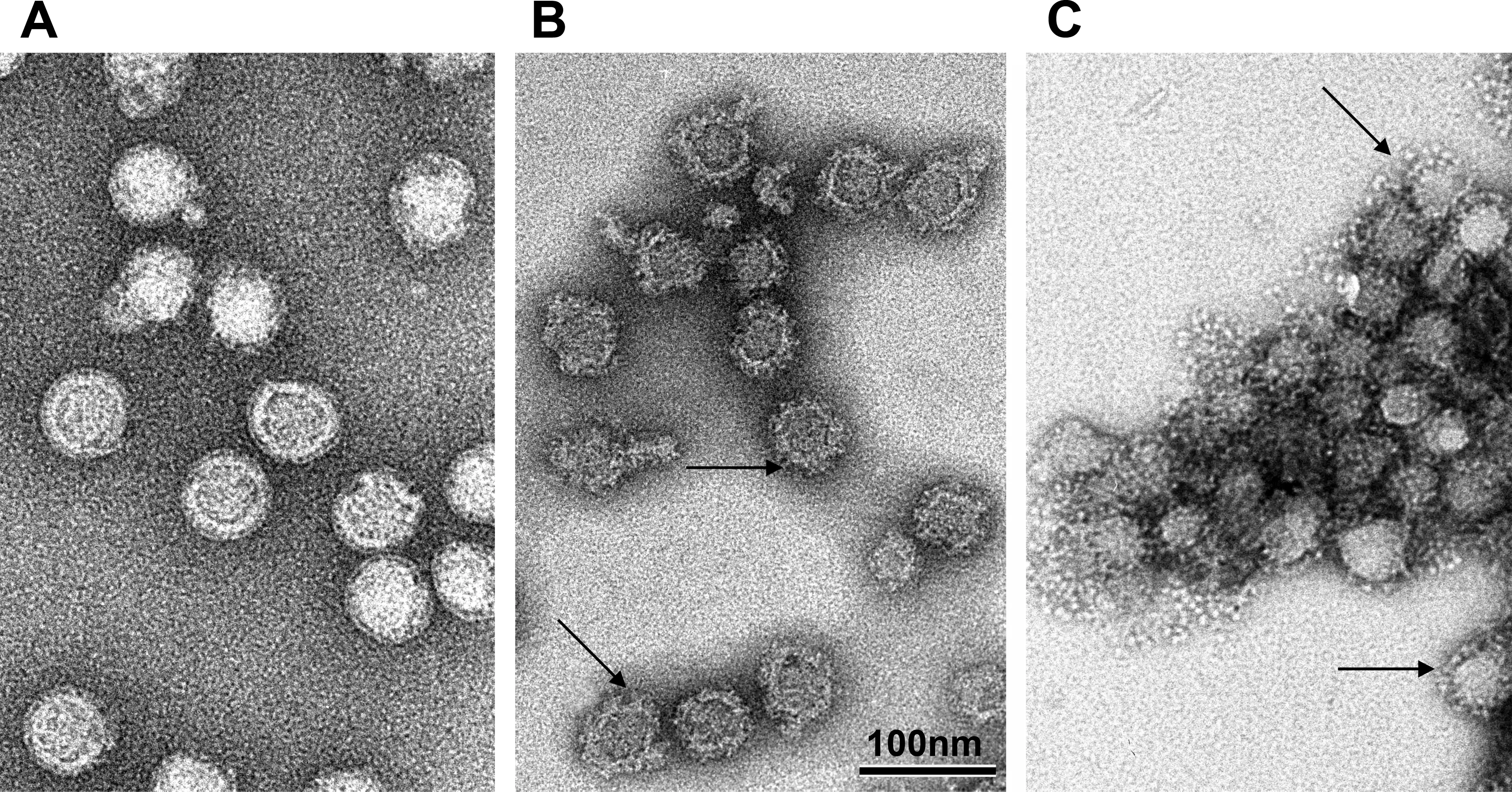
在电子显微镜下,成熟的蜱传脑炎病毒颗粒呈现出令人惊叹的完美球形。它的直径仅有约五十纳米,比人类头发丝的直径还要小一千倍。然而,这个微小的球体内部,却藏着一个精密的杀戮机器。
病毒的外层是一层脂质膜,来自它上次感染的宿主细胞。这层膜上镶嵌着两种蛋白质:膜蛋白(M)和包膜蛋白(E)。正是E蛋白赋予了病毒入侵细胞的能力。它像一把精巧的钥匙,能够识别并结合宿主细胞表面的特定受体。当E蛋白与受体结合后,病毒膜与细胞膜融合,将病毒的遗传物质注入细胞内部。
蜱传脑炎病毒的基因组是一条单股正链RNA,长度约为一万一千个核苷酸。这条RNA链携带着制造新病毒所需的全部信息。它编码一个多聚蛋白,随后被切割成三种结构蛋白(C、prM、E)和七种非结构蛋白(NS1、NS2A、NS2B、NS3、NS4A、NS4B、NS5)。每种蛋白都有其特定的功能:NS5是RNA依赖的RNA聚合酶,负责复制病毒基因组;NS3具有蛋白酶和解旋酶活性,参与多聚蛋白的加工和RNA的解旋。
病毒的复制过程堪称一场细胞内的政变。当病毒RNA进入细胞质后,它立即被宿主的核糖体当作信使RNA进行翻译,产生病毒蛋白。随后,新合成的病毒蛋白开始组装复制复合物,在宿主细胞的内质网膜上建立起病毒的"工厂"。RNA基因组在这里被大量复制,结构蛋白被合成并加工。最后,新的病毒颗粒在内质网和高尔基体中组装成熟,通过胞吐作用释放到细胞外,去寻找下一个受害者。
然而,蜱传脑炎病毒与其他黄病毒有一个关键的不同:它的传播媒介不是蚊子,而是蜱虫。这一差异深刻地影响了病毒的生态学和流行病学特征。
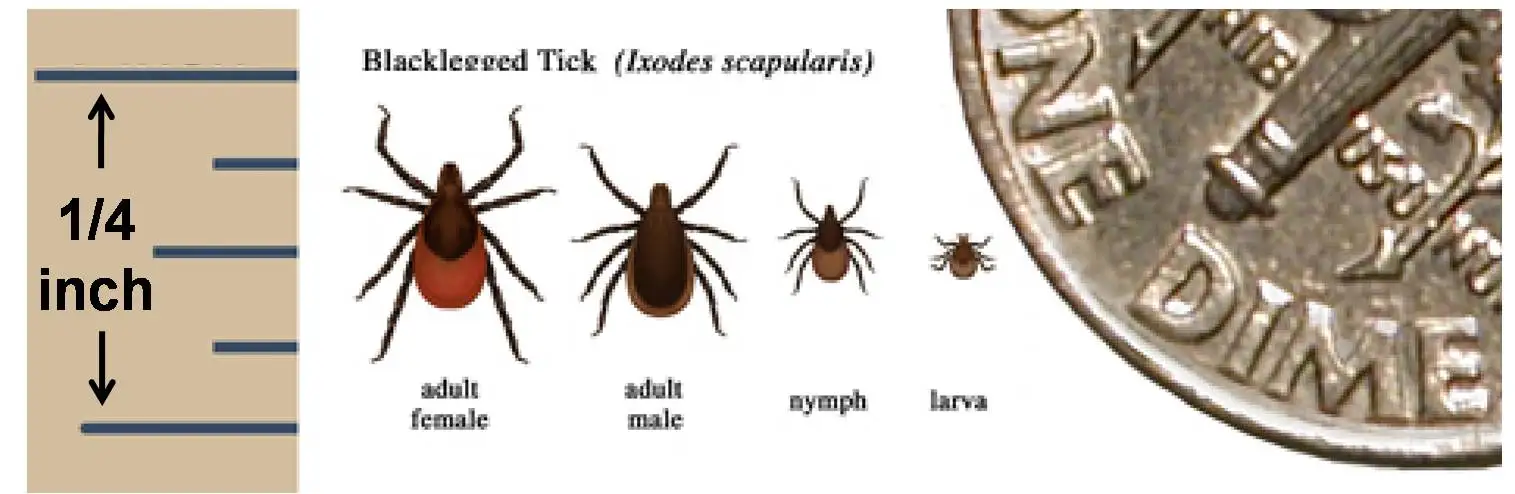
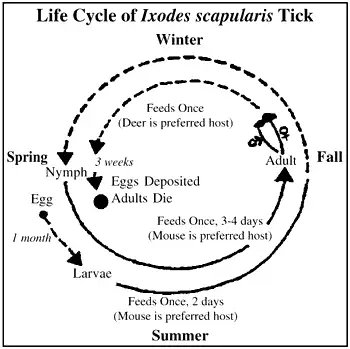
蜱虫是地球上最古老的无脊椎动物之一,化石证据表明它们的存在可以追溯到白垩纪。在漫长的进化过程中,蜱虫发展出了一种令人惊叹的吸血策略。当一只蜱虫找到宿主后,它会用锋利的口器刺破皮肤,然后将名为"下口器"的复杂结构插入伤口。这个结构上布满了向后弯曲的倒钩,使得蜱虫能够牢牢地固定在宿主身上。
更可怕的是蜱虫的唾液。它含有数百种生物活性分子,包括抗凝血剂、血管扩张剂、免疫抑制剂和麻醉剂。正是这些物质让蜱虫能够在宿主毫不知情的情况下持续吸血数天。对于蜱传脑炎病毒来说,蜱虫的唾液简直是完美的掩护。研究表明,蜱虫唾液中的某些成分甚至能够增强病毒在宿主体内的复制能力。
病毒进入人体后的旅程堪称一场精心策划的入侵。当感染的蜱虫开始吸血时,病毒从蜱虫的唾液腺进入宿主的皮肤。在这里,它首先感染朗格汉斯细胞——皮肤中的树突状细胞。这些细胞是免疫系统的"哨兵",负责捕获外来抗原并将其呈递给T细胞。然而,对于蜱传脑炎病毒来说,朗格汉斯细胞不是敌人,而是特洛伊木马。
病毒在树突状细胞内复制,然后随着这些细胞的迁移进入局部淋巴结。在淋巴结中,病毒感染更多的免疫细胞,并开始进入血液循环,形成病毒血症。这是疾病的第一阶段,通常发生在感染后的四至十四天。患者出现发热、头痛、乏力、肌肉酸痛等症状,往往被误认为是流感。
对于大多数患者来说,这就是疾病的终点。他们会在几天后康复,甚至不知道自己曾经感染过蜱传脑炎病毒。然而,对于不幸的少数人来说,真正的噩梦才刚刚开始。
穿越血脑屏障的幽灵
血脑屏障是人体最精密的防御工事之一。它由大脑毛细血管内皮细胞、基底膜、周细胞和星形胶质细胞的足突共同构成,严格限制着血液中的物质进入大脑。大多数病原体都无法通过这道屏障,这也是为什么脑部感染相对罕见的原因。
蜱传脑炎病毒却是个例外。它能够突破血脑屏障,侵入中枢神经系统,这是它最致命的能力,也是人类与它抗争的核心战场。
科学家们提出了四种可能的机制来解释病毒如何穿越血脑屏障。第一种是"特洛伊木马"机制:病毒隐藏在感染的免疫细胞内,随着这些细胞的迁移进入大脑。树突状细胞和中性粒细胞都可能成为病毒的载体。当这些细胞穿过血脑屏障进入脑组织时,病毒便随之释放,开始感染神经元。
第二种机制涉及血脑屏障的直接破坏。病毒感染血管内皮细胞后,可能引发炎症反应,导致屏障的通透性增加。细胞因子和趋化因子的释放会进一步招募免疫细胞,形成恶性循环。
第三种机制是通过逆行轴突运输。病毒可能从周围神经末梢进入神经纤维,沿着轴突逆行运输到达中枢神经系统。这种机制在某些嗜神经病毒中已经得到证实,例如狂犬病毒。
第四种机制涉及嗅觉通路。病毒可能通过嗅神经进入大脑,绕过血脑屏障。一些动物实验支持这一假说,但其在人类感染中的重要性尚不清楚。
无论采用哪种途径,一旦病毒进入大脑,便开始了一场毁灭性的狂欢。它感染神经元,在细胞内大量复制,最终导致细胞死亡。更可怕的是,病毒感染会引发剧烈的炎症反应。大量炎症细胞浸润脑组织,释放促炎因子,进一步加剧神经元损伤。
病理学检查揭示了蜱传脑炎对大脑造成的可怕破坏。脑膜充血、水肿,脑实质内散在出血点。显微镜下,神经元肿胀、变性、坏死,胶质细胞增生,血管周围淋巴细胞和单核细胞浸润呈"袖套"样改变。炎症病变主要累及大脑皮层、基底节、丘脑、脑干和小脑,脑干和脊髓前角运动神经元尤其容易受损,这解释了为什么许多患者会出现瘫痪症状。
芬兰科学家安蒂的故事生动地诠释了这场疾病对患者意味着什么。2023年秋天,这位纳米技术公司的创始人正在参加一个Teams会议,突然感到严重的恶心,不得不提前结束会议。随后,呕吐和剧烈头痛开始袭来。第二天,他的体温飙升到四十一摄氏度,妻子紧急将他送往大学中心医院。
在医院里,安蒂被迅速转入神经科。医生们诊断他患有一种脑部炎症,但最初的检查无法确定病因。接下来的几天里,他的情况相当严重:全身极度乏力,呼吸困难,一般状况极其糟糕。他开始出现谵妄,后来听说医生们不得不询问他的妻子来确认他的话是否属实——患者声称自己拥有化学博士学位并经营着一家纳米技术公司,这确实是真的;但他还声称自己仍在服兵役,那已经是三十年前的事了。
大量的检查随之而来:核磁共振、CT扫描、腰椎穿刺等等,这些检查确认了炎症的存在,但没有揭示病因。由于安蒂完全接种了蜱传脑炎疫苗,医生们最初认为这不太可能是病因,于是诊断为自身免疫性脑炎。基于这个诊断,他接受了大剂量的静脉注射皮质类固醇,这确实显著改善了他的状况。在住院三十天后,他逐渐"回到这个世界",并被允许回家继续康复。
然而,真正的答案直到三个月后才浮出水面。医院打来电话说,他们在最新的样本中发现了有趣的东西——“你得的是蜱传脑炎”。正确的抗体标志物延迟出现,可能是因为他接种过疫苗。终于得到明确的诊断虽然令人释然,但这并不能改变已经发生的一切。
对于安蒂来说,康复之路漫长而艰辛。他的右臂和右腿无法正常工作,肌肉力量非常弱,行走时的协调和平衡严重受损。然而,最糟糕的是疲劳。任何需要高度注意力或大脑处理能力的事情都极具挑战性。来自环境的数据——声音、颜色、触感——毫无过滤地涌入他的大脑,一段时间后大脑就会"关机"。在早期阶段,他每天只能完成一项三十分钟的任务,其余时间都用于睡眠和恢复。
四个月后,他终于能够慢慢开始工作——那是一种难以言喻的快乐!做一些相对正常的工作任务,看到进展顺利,表现仍然保持在良好水平,这种感觉令人欣喜。六个月后,他完全回到了原来的工作岗位。
现在,距离蜱传脑炎发病大约一年后,安蒂感觉良好。一些症状——比如平衡问题和疲劳时的某些抽搐动作——仍然存在,但他可以与之共存。他的神经科医生在最后一次会面时给出了建议:适度饮酒,健康饮食,规律运动,充足睡眠,减少不必要的事务,更多地授权……这些都是显而易见的事情,但坚持执行却很重要。
安蒂是幸运的。他活了下来,并且恢复得相当好。但并非所有人都能如此。
三种面孔,三种命运
蜱传脑炎病毒并非单一的敌人。根据基因序列的差异,科学家们将这个物种分为多个亚型,其中三种最为重要:欧洲亚型、西伯利亚亚型和远东亚型。这三种亚型不仅在地理分布上有所不同,更重要的是,它们对人类的杀伤力截然不同。
远东亚型是最致命的。这一亚型最初就是在苏联远东地区被发现的,它与历史上那些恐怖的爆发密切相关。感染远东亚型病毒的患者,死亡率可高达百分之二十至四十。即使存活下来,许多患者也会留下永久性的神经系统后遗症。远东亚型疾病的特点是起病急骤,病情进展迅速,往往没有明显的双相病程。患者可能直接进入严重的脑炎阶段,出现意识障碍、癫痫发作、肢体瘫痪等症状。
远东亚型的凶猛有其进化原因。分子生物学研究表明,蜱传脑炎病毒起源于大约三千一百年前的西西伯利亚地区。从那里,病毒的东部群体向亚洲东部扩散,西部群体向欧洲方向扩散。远东亚型在进化过程中积累了更多的适应性变异,使其能够更有效地突破血脑屏障,感染神经元,并逃避宿主的免疫反应。
西伯利亚亚型的致病性介于两者之间,死亡率约为百分之六至八。然而,西伯利亚亚型有一个独特的特点:它可能与慢性进展型蜱传脑炎有关。在这种罕见的情况下,病毒似乎能够在患者体内长期存在,导致症状持续恶化,最终可能致命。这种慢性形式在其他亚型中极为罕见。
欧洲亚型则是最"温和"的。感染这一亚型的患者,死亡率通常在百分之零点五至二之间。欧洲亚型疾病的典型特征是双相病程。第一阶段持续约五天(范围二至十天),表现为发热、乏力、食欲不振、肌肉酸痛、头痛、恶心、呕吐等非特异性症状。随后是一个无症状期,通常持续约八天(范围一至三十三天)。大约百分之二十至三十的患者会进入第二阶段,出现神经系统症状:脑膜炎、脑炎或脑膜脑炎。
然而,即使是"温和"的欧洲亚型也不应被低估。研究表明,大约百分之三十至五十的患者在急性期过后会出现某种形式的长期后遗症。最常见的症状包括认知或神经精神方面的主诉,如抗压能力下降和记忆力受损。疲劳是最常见的慢性症状,影响着大约百分之十七的患者。其他常见问题包括虚弱、注意力缺陷、平衡障碍和头痛。约百分之八点五的患者会留下严重残疾,需要调整日常生活活动。
三种亚型的地理分布与它们的主要传播媒介密切相关。欧洲亚型主要由蓖麻硬蜱传播,这种蜱虫广泛分布于欧洲大陆,从大西洋沿岸一直延伸到乌拉尔山脉。远东亚型的主要传播媒介是全沟硬蜱,它适应了更寒冷的气候,广泛分布于西伯利亚、远东、中国东北、日本和朝鲜半岛。西伯利亚亚型则介于两者之间,主要分布在中西伯利亚和乌拉尔地区。
蜱传脑炎病毒的传播不仅仅是蜱虫叮咬的结果。另一种重要的传播途径是食物——确切地说,是未经巴氏消毒的山羊奶或羊奶酪。1947年至1951年间,在苏联欧洲部分首次发现了这种传播方式。当时,一群人在食用了来自病毒血症山羊的生奶或奶制品后集体发病。类似的食源性爆发也发生在其他蜱传脑炎流行国家,例如1951年斯洛伐克东南部罗日纳瓦的一次爆发,超过六百人感染;1961年东德尼斯基地区也发生了大规模爆发。
这种传播方式之所以危险,是因为它不需要人们进入森林或接触蜱虫。在城市环境中,只要饮用了被污染的奶制品,就可能感染病毒。这也解释了为什么一些从未接触过蜱虫的人也会患上蜱传脑炎。
一场跨越世纪的疫苗战争
与大多数病毒性疾病一样,蜱传脑炎没有特效治疗方法。一旦发病,医生们能做的只是支持性治疗和对症处理——控制高烧、减轻脑水肿、维持生命体征、预防并发症。那些严重的病例往往需要在重症监护室接受治疗,有些患者需要机械通气,有些人永远无法完全康复。
在这种背景下,疫苗成为人类对抗蜱传脑炎最有力的武器。然而,这把武器的锻造过程,充满了艰辛、创新和跨国合作。
世界上第一种蜱传脑炎疫苗诞生于1930年代末的苏联,就在病毒被发现后不久。这支疫苗的研发团队主要由女性科学家组成——这反映了苏联微生物学领域显著的"女性化"趋势。莫斯科全联盟实验医学研究所的纳德日达·卡根和伊丽莎维塔·列夫科维奇领导了这项工作。卡根在1938年秋天感染了蜱传脑炎并去世,列夫科维奇接手了她的工作。两个月后,一名年轻的实验室技术员娜塔莉亚·乌特金娜在感染病毒后死亡,次年她的表妹(在同一实验室工作)也暴露于病毒,幸运的是在住院数月后康复。
1939年,列夫科维奇和她的助手加琳娜·佐林娜-尼古拉耶娃在自己身上测试了新疫苗——这是那个时代科学家们的勇气和奉献精神的缩影。
第一种疫苗是基于远东亚型的索夫金毒株,使用感染小鼠的脑组织悬液,经福尔马林灭活制成。为了检验疫苗的效力,1939年在哈巴罗夫斯克地区的奥博尔村附近进行了大规模人体试验。关于这次试验的细节,不同来源的记载存在差异。官方发表的论文报告了925名疫苗接种者和1185名对照组成员,但2001年出版的回忆录则称试验对象是古拉格的囚犯——疫苗接种组1987人,对照组2387人。如果这一说法属实,那么参与试验的自愿性就值得怀疑。
无论如何,试验结果显示疫苗提供了一定的保护作用。官方报告称,疫苗接种组仅有2例轻型病例,而对照组有27例病例和7例死亡。疫苗被批准用于流行地区的居民。
然而,小鼠脑组织疫苗有一个严重的缺陷:它常常引起不良反应,有些反应相当严重。这是因为疫苗中含有小鼠脑组织成分,可能引发严重的过敏反应甚至神经系统并发症。在随后的几十年里,苏联科学家继续探索更安全的疫苗技术。
1959年至1960年间,脊髓灰质炎和病毒性脑炎研究所(由米哈伊尔·丘马科夫领导,就是那位在1937年探险中感染蜱传脑炎并留下残疾的科学家)开始生产一种基于鸡胚细胞培养的新疫苗。这种疫苗的反应更轻,效力也更好。然而,它需要一个复杂而漫长的接种程序——四次基础免疫和三次加强接种——在现实世界中的可操作性受到限制。
与此同时,在铁幕的另一边,蜱传脑炎同样引起了科学家们的关注。1931年,奥地利医生汉斯·施奈德首次描述了"流行性急性浆液性脑膜炎",这实际上是欧洲型蜱传脑炎的首次医学报告。此后,蜱传脑炎在欧洲各国陆续被发现:1948年捷克斯洛伐克、1952年匈牙利、1953年斯洛文尼亚、1954年波兰和奥地利、1959年芬兰……
冷战的铁幕并没有完全阻断科学交流。1957年,印度爆发基萨努尔森林热病(一种与蜱传脑炎密切相关的疾病),沃尔特·里德陆军研究所向印度发送了五万剂鼠脑疫苗,以保护疫区居民。这一事件反映了蜱传脑炎研究的军事意义——在冷战的背景下,蜱传性病毒疾病不仅威胁平民健康,也可能影响军队的战斗力。
1970年代,奥地利病毒学家克里斯蒂安·昆茨与英国波顿当微生物研究机构的合作,最终催生了现代蜱传脑炎疫苗。FSME-IMMUN疫苗于1976年在奥地利首次获得批准,这标志着蜱传脑炎疫苗进入了一个新时代。
这种疫苗使用的是在欧洲分离的病毒株,通过细胞培养技术生产,经福尔马林灭活后纯化制成。与早期的鼠脑疫苗相比,它更安全、更有效、不良反应更少。更重要的是,它适合大规模人群接种。
1981年,奥地利启动了全国性的蜱传脑炎疫苗接种计划。这是世界上第一个针对蜱传性病毒疾病的全国性免疫项目。到2001年,奥地利的疫苗接种覆盖率达到了百分之八十六——这是任何其他国家都未能匹敌的成就。
结果令人瞩目。在疫苗接种计划实施之前,奥地利每年报告数百例蜱传脑炎病例。随着疫苗覆盖率的提高,病例数稳步下降。总体疫苗效力估计为百分之九十七。疫苗接种预防了超过一万例病例和五百例以上的死亡。奥地利证明了,只要有一种安全有效的疫苗和坚定的公共卫生决心,蜱传性病毒疾病是可以被控制的。
今天,欧洲市场上有两种主要的蜱传脑炎疫苗:FSME-IMMUN(由辉瑞公司生产)和Encepur(由巴伐利亚北欧公司生产)。这两种疫苗都被证明安全有效,完成三剂基础免疫后,血清转化率超过百分之九十九。
然而,疫苗接种面临着新的挑战。在一些国家,反疫苗运动的兴起导致接种率下降,蜱传脑炎病例随之增加。同时,气候变化正在改变蜱虫的分布范围,将疾病带到了以前从未有过病例的地区。荷兰在2016年首次报告了本土蜱传脑炎病例,英国也在近期发现了病毒的存在。
永恒的博弈
蜱传脑炎病毒与人类的博弈从未停止。这种病毒已经在地球上存在了至少三千年,它见证了人类文明的兴衰,而人类对它的认识还不到一个世纪。
气候变化正在重塑这场博弈的格局。随着全球气温上升,蜱虫的活动范围正在向北扩张。曾经寒冷的北欧地区,如今已成为蜱传脑炎的高发区。芬兰、瑞典、挪威近年来都报告了病例的增加。同时,蜱虫的活动季节也在延长——过去主要局限于春夏两季,现在从早春到深秋都可能有蜱虫出没。
城市化进程同样在改变着疾病的流行模式。随着城市扩张侵入野生动物栖息地,人类与携带病毒的蜱虫和宿主动物的接触机会大大增加。一些城市公园和郊区绿地已经成为蜱传脑炎的传播场所。这不再是"森林中的疾病",它正在向我们的家门口逼近。
然而,人类并非毫无还手之力。科学家们正在开发新一代疫苗,包括基于重组蛋白和mRNA技术的疫苗,这些可能提供更广泛的保护、更少的接种剂次。诊断技术也在不断进步,早期检测的准确性正在提高。公共卫生教育让更多人认识到蜱虫叮咬的危险,学会采取防护措施。
对于个人来说,预防蜱传脑炎的关键在于避免蜱虫叮咬和接种疫苗。在进入森林、草地等蜱虫栖息地时,应穿长袖衣裤,将裤脚扎入袜子,使用含有避蚊胺或派卡瑞丁的驱虫剂。活动结束后,应仔细检查全身是否有蜱虫附着。如果发现蜱虫,应使用尖头镊子贴近皮肤夹住蜱虫,缓慢均匀地向上拔出,避免挤压或扭转。
对于生活在或旅行到蜱传脑炎流行地区的人来说,疫苗接种是最有效的保护措施。世界卫生组织建议,在高度流行地区(年平均发病率≥5/10万)应对所有年龄组提供普遍疫苗接种。在低度流行地区,疫苗应提供给从事户外活动或高风险职业的人群。
蜱传脑炎病毒的故事,是人类与自然界中无数隐形敌人博弈的缩影。从1937年泰加林深处的探险队,到今天的全球公共卫生网络;从简陋的帐篷实验室,到最先进的分子生物学技术——我们一直在学习、进步、战斗。
这场战斗不会有终点。蜱传脑炎病毒不会消失,它将继续在森林与草原的阴影中等待。但每一代科学家、每一位医生、每一个接种疫苗的人,都在为减少它的伤害而努力。正如米哈伊尔·丘马科夫在感染病毒后所做的那样——尽管失去了右手的正常功能,他仍然将毕生精力投入到对抗这种疾病的事业中,最终帮助开发出了拯救无数人生命的疫苗。
这或许就是人类与疾病永恒博弈的真谛:我们无法彻底消灭所有的敌人,但我们可以让越来越少的人为此付出代价。
参考资料
-
Zlobin VI, Pogodina VV, Kahl O, et al. A brief history of the discovery of tick-borne encephalitis virus in the late 1930s. Ticks Tick Borne Dis. 2017;8(6):813-820.
-
Kahl O, Pogodina VV, Poponnikova T, et al. A short history of TBE. In: Dobler G, Erber W, Bröker M, Schmitt HJ, eds. The TBE Book. 6th ed. Global Health Press; 2023.
-
Bogovic P, Strle F. Tick-borne encephalitis: A review of epidemiology, clinical characteristics, and management. World J Clin Cases. 2015;3(5):430-441.
-
Růžek D, Dobler G, Mantke OD. Tick-borne encephalitis: Pathogenesis and clinical implications. Travel Med Infect Dis. 2010;8(4):223-232.
-
Kunz C. Vaccination against TBE in Austria: The success story continues. Int J Med Microbiol. 2002;291 Suppl 33:56-57.
-
Fritzsche M, Belikov SI. The E protein E dimer interface: A key determinant of tick-borne encephalitis virus antigenic structure. Viruses. 2022;14(10):2184.
-
European Centre for Disease Prevention and Control. Tick-borne encephalitis - Annual Epidemiological Report 2022. ECDC; 2024.
-
Heinz FX, Stiasny K. The antigenic structure of tick-borne encephalitis virus and its use in vaccine development. Vaccine. 2023;41(35):5047-5055.
-
Füzik T, Formanová P, Růžek D, et al. Structure of tick-borne encephalitis virus and its neutralization by a monoclonal antibody. Nat Commun. 2018;9(1):436.
-
Kholodilov IS, Belov MA, Kozlovskaya LI, et al. The structure of immature tick-borne encephalitis virus supports the universal role of the prM protein in flavivirus maturation. Nat Commun. 2024;15(1):4528.
