
1975年深秋,康涅狄格州的一个宁静小镇上,两位母亲开始了她们生命中最重要的战斗。Polly Murray和Judith Mensch并不是医生,也不是科学家,她们只是普通的家庭主妇,但她们敏锐地注意到了一个令人不安的现象:她们的孩子们,以及邻居家的孩子们,正在以一种奇怪的方式生病。
这些孩子出现了关节肿胀、疼痛、发烧和奇怪的皮疹。当她们带着孩子去看医生时,得到的诊断往往是"青少年类风湿性关节炎"或"生长痛"。但两位母亲无法接受这个解释——类风湿性关节炎是一种慢性疾病,通常不会在同一时间、同一个小镇上如此集中地爆发。
她们的坚持最终引发了医学史上最重要的发现之一。这两位母亲的担忧,揭开了一个被称为"伟大的模仿者二世"的疾病——莱姆病的面纱。而在这场发现之旅的背后,是科学家们跨越十年的追踪、一位瑞士裔美国微生物学家的偶然发现,以及一个比人类文明还要古老的细菌与蜱虫之间精妙而可怕的合作关系。
瑞士钟表匠后裔的显微镜

1981年秋天,在蒙大拿州汉密尔顿市的落基山实验室里,56岁的Wilhelm"Willy"Burgdorfer正准备迎接一个改变医学史的下午。这位瑞士出生的微生物学家已经在蜱传疾病领域工作了三十多年,他的博士论文研究的就是非洲回归热螺旋体与其蜱虫媒介的关系。
Jorge Benach,一位来自纽约州立大学石溪分校的寄生虫学家,向Willy寄送了一批来自长岛谢尔特岛的鹿蜱。这些蜱虫是在调查当地巴贝虫病和莱姆病患者家庭周围收集的。Willy的任务是在这些蜱虫中寻找立克次体——一种可能引起疾病的细菌。
当Willy在暗视野显微镜下观察这些蜱虫的血淋巴和肠道内容物时,他没有找到立克次体。但他看到了一些让他心脏骤停的东西:在蜱虫肠道中游动的螺旋形细菌——螺旋体。
这是一种令人震惊的发现。螺旋体是一种独特的细菌类型,它们的身体呈螺旋状,能够在粘稠的液体中像开瓶器一样钻动前进。最著名的螺旋体是引起梅毒的苍白密螺旋体,而Willy在蜱虫肠道中发现的,是一种全新的、从未被描述过的螺旋体。
Willy立刻意识到这可能就是困扰康涅狄格州居民多年的神秘疾病的病原体。他迅速联系了同事Alan Barbour,一位刚加入落基山实验室的年轻传染病专家。两人合作,在1981年11月成功分离并培养了这种螺旋体。
当Willy用莱姆病患者的血清与这些螺旋体进行间接免疫荧光测试时,结果令人振奋:患者血清中含有针对这种螺旋体的抗体,而健康对照组的血清则没有。1982年6月,他们的发现发表在《Science》杂志上,论文标题是"Lyme Disease—a Tick-Borne Spirochetosis?“注意那个问号——当时的证据仍然是间接的。
一年后,这个问号被移除了。1983年,研究人员成功从莱姆病患者的血液和其他标本中分离出了这种螺旋体,完成了科赫法则的验证。这种细菌被命名为伯氏疏螺旋体(Borrelia burgdorferi),以纪念Willy Burgdorfer的发现。
五千年的沉默
Willy Burgdorfer的发现让医学界为之振奋,但莱姆病的故事远比1975年的康涅狄格州更为古老。
1991年9月,两名德国登山者在阿尔卑斯山脉的Ötztal阿尔卑斯山发现了一具被冻结在冰川中的古代尸体。这具后来被称为"Ötzi冰人"的遗体,经过碳14测年,被证实死于约5300年前。DNA分析揭示了一个惊人的事实:Ötzi体内携带着伯氏疏螺旋体的DNA。
这意味着,莱姆病的病原体至少在五千年前就已经在北半球传播。事实上,有证据表明这种疾病可能比人类本身还要古老。俄勒冈州立大学的研究发现,伯氏疏螺旋体已经存在了数百万年,在北美大陆上的历史可以追溯到远古时期。
在欧洲,对游走性红斑(莱姆病的标志性皮疹)的描述可以追溯到20世纪初。1909年,瑞典皮肤科医生Arvid Afzelius在斯德哥尔摩的瑞典皮肤科学会会议上首次描述了这种扩张性的环状皮疹。他注意到这种皮疹与蜱虫叮咬有关,但并不知道是什么引起了它。
在随后的几十年里,欧洲医生观察到了与游走性红斑相关的神经系统症状,包括神经痛、瘫痪和脑膜炎。他们推测这可能是由某种感染引起的,青霉素和其他抗生素治疗显示了一定效果。但直到1975年康涅狄格州的爆发,人们才意识到这是一种全新的、多系统疾病。
康涅狄格河畔的侦探故事
当Polly Murray和Judith Mensch向康涅狄格州卫生部门和耶鲁大学医学院求助时,她们启动了一场跨越多年的医学侦探行动。
耶鲁大学风湿病学部门的Allen Steere医生当时只是一名第一年的风湿病学研究员。他和部门主管Stephen Malawista医生一起,设计了一项详细的监测研究来调查这起神秘的关节炎爆发。
他们的研究聚焦于Lyme、Old Lyme和East Haddam三个相邻的城镇。在这些总共约12000人的社区中,他们发现了51名被诊断为青少年关节炎或不明原因关节炎的患者——39名儿童和12名成人。
体格检查和血液检测没有发现任何异常。但病史采集揭示了一个关键的线索:大约25%的患者报告在关节炎症状出现前四周或更长时间,曾经出现过一种扩张性的"牛眼样"皮疹。
这个描述让Steere和Malawista想起了欧洲文献中描述的游走性红斑。在欧洲,这种皮疹被认为是由某种感染引起的,但从未与关节炎联系起来。更重要的是,在欧洲的病例中,游走性红斑从未导致关节症状。
地理和时间分布模式也提供了重要线索。患者们大多居住在小镇的农村林区,城镇中心没有病例。一些孩子住在同一条街上,几个家庭成员同时发病。而最引人注目的是症状出现的时间:大多数患者在6月至9月之间发病。类风湿性关节炎是一种自身免疫性疾病,绝不会以这种方式在地理和时间上聚集出现。
这些发现让Steere和Malawista提出了一个大胆的假设:这种"莱姆关节炎"是由某种虫媒传播的感染引起的。
1976年夏天,研究团队迎来了下一个"高发季节”。他们发现了30名新患者,并通过详细调查确认了游走性红斑与关节炎发展之间的联系。游走性红斑被正式确定为感染的初始标志和莱姆病的诊断特征。
1978年,研究团队扩展了他们的监测范围,跨越康涅狄格河。他们发现,河东侧(Lyme所在)的莱姆关节炎发病率是西侧的30倍。这种分布与当地鹿和鹿蜱的分布惊人地吻合,提供了蜱虫作为传播媒介的流行病学证据。
螺旋体的完美伪装
伯氏疏螺旋体是一种生物学上的奇迹,也是人类免疫系统最狡猾的对手之一。
在暗视野显微镜下,这些细菌呈现出优雅的螺旋形态,长度约10-30微米,直径仅0.2-0.3微米。它们拥有独特的鞭毛结构——不是像其他细菌那样从细胞表面伸出,而是位于外膜和原生质柱之间的周质空间内。这些周质鞭毛从细菌两端向中间延伸,像捆绑在一起的丝带一样缠绕着细胞体。
这种结构赋予了螺旋体非凡的运动能力。它们可以在粘稠的液体中像开瓶器一样钻动前进,速度可达每分钟数个细胞长度。这种能力使它们能够穿透人体组织,穿越血管壁,到达几乎身体的任何部位。
伯氏疏螺旋体的基因组是所有已知细菌中最小的之一,仅约150万个碱基对。这个精简的基因组反映了它作为专性寄生者的生活方式——它依赖宿主提供许多必需的营养物质,包括大多数氨基酸和脂肪酸。
但基因组小并不意味着简单。伯氏疏螺旋体拥有一套复杂的表面蛋白系统,使它能够在蜱虫和哺乳动物两种截然不同的宿主之间生存和传播。
当细菌在蜱虫肠道中时,它们表达一种叫做OspA(外表面蛋白A)的表面蛋白。这种蛋白与蜱虫肠道上皮细胞表面的受体结合,使细菌能够附着在肠道壁上。当蜱虫开始吸血时,血液中的营养物质和环境变化触发了一系列基因表达的变化。
在吸血过程中,细菌下调OspA的表达,同时上调另一种表面蛋白OspC。OspC帮助细菌从蜱虫肠道迁移到唾液腺,最终通过唾液进入哺乳动物宿主。
但这还不是伯氏疏螺旋体最令人惊叹的逃避免疫的策略。
蜱虫的化学战
蜱虫叮咬不是一个简单的机械过程。当一只鹿蜱附着在人体皮肤上开始吸血时,它会释放一种复杂的唾液混合物,其中包含数百种具有生物活性的蛋白质。
这些唾液蛋白是蜱虫进化数百万年获得的武器库。它们包括抗凝血剂(防止血液凝固)、血管扩张剂(增加血流量)、麻醉剂(使叮咬几乎无痛)和免疫抑制剂。
对于伯氏疏螺旋体来说,蜱虫的唾液是一个完美的掩护。研究显示,蜱虫唾液蛋白Salp15能够与细菌表面的OspC结合,形成一层保护性的外衣。当细菌进入哺乳动物宿主时,这层外衣使细菌能够逃避免疫系统的识别。
更令人惊叹的是,蜱虫唾液还含有能够抑制补体系统——人体先天免疫的重要组成部分——的蛋白质。补体系统是一组在血液中循环的蛋白质,它们能够识别并破坏入侵的病原体。但蜱虫唾液中的某些蛋白质能够阻断补体级联反应的关键步骤,为细菌创造一个安全的入侵通道。
蜱虫唾液中还含有抗炎化合物,能够抑制巨噬细胞和树突状细胞——免疫系统的"哨兵"——的功能。这些细胞通常负责识别病原体并启动适应性免疫反应。通过抑制它们的功能,蜱虫唾液实际上为细菌创造了一个"免疫盲区"。
这种蜱虫与细菌之间的协同进化关系,是自然界最精妙的合作之一。蜱虫需要细菌的帮助吗?不一定。但对于细菌来说,蜱虫唾液提供的免疫抑制环境是无价的优势。
牛眼下的秘密
游走性红斑是莱姆病最特征性的临床表现,也是最可靠的诊断线索。这种皮疹通常在蜱虫叮咬后3-30天出现,开始时是一个小的红色斑点或丘疹,然后以每天约2-3厘米的速度向外扩展。
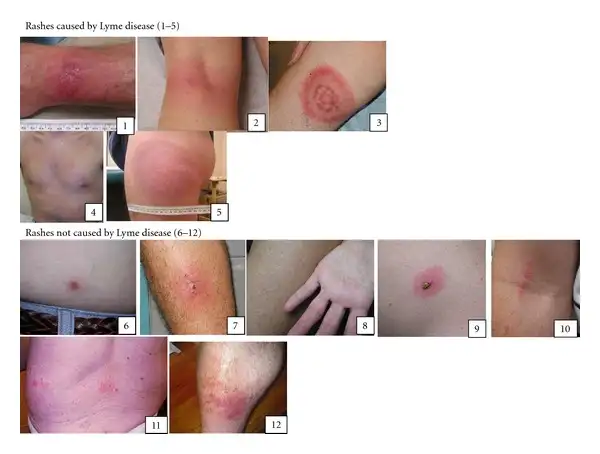
典型的游走性红斑呈现出"牛眼样"外观:中央是一个清晰的区域(通常是原叮咬部位),周围是红色的环状边界。皮疹可以变得非常大,直径可达数十厘米,但通常不会超过70厘米。患者可能会感到皮疹部位温暖,但通常不痒也不痛。
然而,“牛眼样"皮疹只是游走性红斑的一种表现形式。研究表明,只有约20-30%的游走性红斑呈现经典的牛眼样外观。更常见的是均匀的红斑,或者呈现不规则形状。这种多样性使得游走性红斑有时被误认为是蜘蛛叮咬、蜜蜂蜇伤或接触性皮炎。
重要的是,游走性红斑在深色皮肤上的表现可能与在浅色皮肤上不同。在深色皮肤上,红斑可能呈现紫色、棕色或深色,而不是典型的红色。这种差异可能导致莱姆病在某些人群中被低估或误诊。
游走性红斑的出现是莱姆病诊断的"金标准”。根据美国疾病控制与预防中心的定义,在流行地区,出现典型的游走性红斑即可临床诊断莱姆病,无需实验室检测确认。这是因为游走性红斑的特异性极高——几乎没有其他疾病会产生这种独特的皮疹。
然而,问题是并非所有莱姆病患者都会出现游走性红斑。估计有20-30%的患者从不发展出这种皮疹。对于这些患者,诊断变得更加困难,他们可能在疾病进展到后期阶段才被正确识别。
从皮肤到心脏的旅程
如果不治疗,伯氏疏螺旋体可以从最初的感染部位扩散到身体的几乎任何器官系统。这种传播通常是血源性的,细菌通过血液循环到达远处部位。
疾病的第二阶段,称为早期播散性莱姆病,通常发生在感染后数天到数周。在这个阶段,患者可能出现多发性游走性红斑——这些是次发性皮疹,出现在远离原叮咬部位的皮肤上。它们表明细菌已经进入血液并扩散到全身。
神经系统的受累是早期播散性莱姆病的另一个重要表现。神经莱姆病可以表现为多种形式,包括脑膜炎(脑膜的炎症)、颅神经炎(尤其是面神经,导致面瘫)和神经根神经炎(脊神经根的炎症,引起剧烈的神经痛)。
一个典型的神经莱姆病综合征是Bannwarth综合征,最初在欧洲被描述。这种综合征的特征是严重的神经根疼痛、淋巴细胞性脑膜炎和颅神经麻痹。疼痛通常在夜间加重,可能被误认为是椎间盘突出或其他脊柱疾病。
心脏也可能受到攻击。莱姆心肌炎是早期播散性莱姆病的一种罕见但重要的表现,估计发生在约1-5%的未治疗患者中。伯氏疏螺旋体可以侵入心脏传导系统,导致各种程度的心脏传导阻滞。
最令人担忧的是三度(完全性)房室传导阻滞,即心脏的电信号完全无法从心房传导到心室。患者可能出现晕厥、头晕或严重的心动过缓。一项研究发现,在一系列莱姆心肌炎患者中,超过40%出现了某种程度的房室传导阻滞。
好消息是,莱姆心肌炎通常对抗生素治疗反应良好,大多数患者的心脏传导功能可以完全恢复。但关键是要及时识别——一个年轻健康的患者突然出现不明原因的心脏传导阻滞,尤其是在莱姆病流行地区,应该高度怀疑这种可能性。
关节的慢性战争
莱姆关节炎是晚期莱姆病最常见的表现,通常在感染后数月甚至数年才出现。
这种关节炎有其独特的特征。它通常是不对称的,主要影响大关节,尤其是膝关节。受累关节可能出现大量积液,膝盖可能肿胀到令人难以置信的程度。与类风湿性关节炎不同,莱姆关节炎通常一次只影响少数关节(寡关节炎),而不是多个小关节。
关节炎发作可能持续数周,然后自发缓解,但可能在数月后复发。这种复发-缓解的模式可能持续数年。
有趣的是,研究发现莱姆关节炎的发病机制与其他表现有所不同。在疾病的早期阶段,症状主要是由活细菌的存在引起的。但在关节炎中,即使细菌已经被抗生素清除,炎症仍可能持续。
这被称为"抗生素难治性莱姆关节炎",估计发生在约10%的莱姆关节炎患者中。研究表明,这种情况可能是由免疫系统的异常反应引起的——患者的免疫系统对细菌残留的某些成分产生了持续的炎症反应。
关节滑液中可以检测到高水平的促炎细胞因子和趋化因子,即使细菌已经不存在。这解释了为什么一些患者需要额外的抗炎治疗,甚至免疫调节剂,来控制关节炎症状。
诊断的灰色地带
莱姆病的诊断是医学实践中最具争议的领域之一。
问题的核心在于:莱姆病的血清学检测并不完美。目前的标准检测方法是两步法:首先进行酶联免疫吸附测定(ELISA)或免疫荧光测定(IFA)作为筛查,如果结果为阳性或可疑,再进行免疫印迹(Western blot)确认。
但这种检测策略有几个重要的局限性。首先,人体产生针对伯氏疏螺旋体的抗体需要时间——通常至少2-4周。在感染早期(尤其是游走性红斑出现时),患者可能还没有产生可检测的抗体,导致假阴性结果。研究显示,早期莱姆病的假阴性率可能高达30-50%。
其次,伯氏疏螺旋体的抗原与其他细菌存在交叉反应。特别是其他螺旋体(如梅毒螺旋体)以及某些其他感染,可能导致假阳性结果。自身免疫性疾病患者也可能出现假阳性。
第三,即使感染已经清除,抗体也可能在血液中持续存在数年甚至终身。这使得检测无法区分活动性感染和既往感染。
第四,不同实验室之间的检测标准化程度有限。同样的标本在不同实验室可能得到不同的结果。
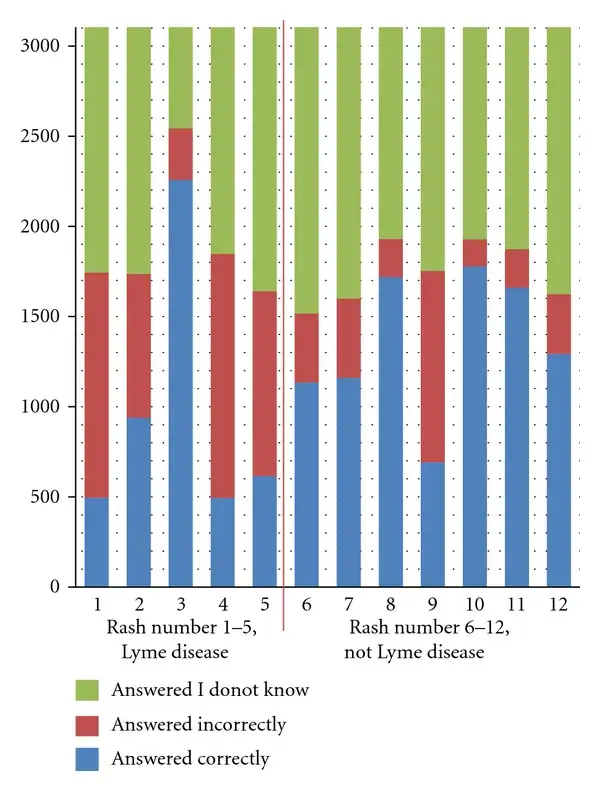
这些局限性在临床实践中造成了困境。当患者出现典型症状和游走性红斑时,诊断相对简单。但当患者只有非特异性症状,或者检测结果是临界值时,医生必须做出困难的判断。
慢性莱姆病的争议
没有任何一个话题比"慢性莱姆病"更让医学界分裂。
争议的核心问题是:在标准抗生素治疗后,莱姆病是否可以持续存在?
根据美国感染病学会(IDSA)的指南,莱姆病可以用10-28天的抗生素疗程有效治疗。大多数患者在这个治疗后会完全康复。然而,一小部分患者报告在治疗后持续存在症状,包括疲劳、关节痛、肌肉痛和认知障碍。
这种情况被正式命名为"治疗后莱姆病综合征"(PTLDS),估计发生在约10-20%的治疗患者中。IDSA认为,这些持续症状不是因为活动性感染,而是由于治疗前的组织损伤、残留的炎症反应或自身免疫机制。
然而,一些医生和患者权益组织持不同观点。他们认为,伯氏疏螺旋体可以在标准抗生素治疗后存活,持续存在于体内,导致"慢性莱姆病"。他们主张使用更长时间、更高剂量或多种抗生素的联合治疗。
这种分歧导致了激烈的医学争议,甚至引发了法律诉讼。2006-2008年间,康涅狄格州总检察长对IDSA进行了反垄断调查,指控其制定指南时存在利益冲突。调查最终没有发现违规行为,但IDSA同意召集一个新的小组重新审查指南,新指南在2010年发布,基本维持了原有建议。
科学证据如何?动物研究表明,在某些情况下,伯氏疏螺旋体确实可能在抗生素治疗后存活,但数量极少,且通常无法培养。这些"残余"细菌是否足以引起症状,目前尚不清楚。
关于长期抗生素治疗的研究结果也不一致。一些研究表明,延长抗生素治疗可能带来轻微益处,而其他研究则发现没有益处,甚至可能有害(抗生素副作用、静脉导管并发症等)。
这场争议已经超越了科学领域,涉及患者权益、医疗资源分配和医学权威等复杂问题。对于患者来说,持续的症状是真实的,而医学界提供的不确定答案往往令人沮丧。
蜱虫的帝国崛起
气候变化正在改变莱姆病的版图。
鹿蜱的生命周期跨越两年,包括幼虫、若虫和成虫三个阶段。每个阶段都需要一次血餐来完成发育。温度和湿度对蜱虫的存活和活动至关重要。
更温暖的冬季意味着更多的蜱虫能够存活到下一个季节。更早的春季和更晚的秋季延长了蜱虫的活动窗口。研究表明,气候变化已经导致蜱虫向北扩展到以前太冷不适合生存的地区。
在美国,莱姆病已经从东北部和中西部上游的传统流行区扩展到更广阔的区域。加拿大东部正在经历莱姆病病例的急剧增加,这与气候变暖导致的蜱虫栖息地北移相吻合。
在欧洲,类似的趋势也在发生。莱姆病(在欧洲称为莱姆疏螺旋体病)正在向北扩展到斯堪的纳维亚半岛,向东扩展到更广阔的地区。
气候变化还可能通过影响宿主动物的种群来间接影响莱姆病的传播。白脚鼠是伯氏疏螺旋体的主要储存宿主,它们能够在不生病的情况下携带细菌。橡树果实的丰度会影响鼠类的种群数量,而气候变化可能影响橡树的结实模式。
另一个重要因素是鹿群数量的变化。鹿是成虫蜱虫的主要血餐来源和交配场所。美国东北部鹿群数量的增加,被认为是莱姆病流行加剧的重要原因之一。人类活动导致的鹿的天敌(如狼和山狮)消失,以及郊区发展创造的理想鹿栖息地,都促成了这一趋势。
疫苗的梦想与挫折
莱姆病疫苗的故事是一个关于希望、挫折和重新开始的故事。
1998年12月,美国食品药品监督管理局(FDA)批准了一种名为LYMErix的莱姆病疫苗。这种疫苗基于伯氏疏螺旋体的OspA蛋白,采用了一种创新的策略:在蜱虫叮咬时,疫苗诱导的抗体会随血液进入蜱虫体内,在那里中和细菌,阻止它们从蜱虫肠道迁移到唾液腺。
临床试验显示,LYMErix在预防莱姆病方面约80%有效。这似乎是一个公共卫生的成功故事。
但问题很快出现了。一些接种疫苗的人报告出现了关节痛和其他症状,他们认为这是疫苗的副作用。虽然大型研究没有发现疫苗与这些症状之间的因果联系,但媒体报道和法律诉讼迅速引发了公众担忧。
更复杂的是,OspA蛋白与人类某些蛋白质存在结构相似性,这引发了关于分子模拟可能导致自身免疫反应的理论担忧。虽然这个理论从未被证实,但在公众心目中种下了疑虑的种子。
到2001年,LYMErix的销量急剧下降。2002年,制造商葛兰素史克(当时是SmithKline Beecham)决定停止销售该疫苗。到那时,已有超过100万人接种了LYMErix,但最终法律诉讼以和解结束,没有任何因果关系被证实。
LYMErix的失败对莱姆病疫苗领域产生了寒蝉效应。近20年来,美国没有可用的莱姆病疫苗。
然而,近年来,莱姆病疫苗的研发正在复兴。欧洲生物技术公司Valneva与美国制药巨头辉瑞合作开发了一种新的OspA疫苗VLA15。这种疫苗覆盖了北美和欧洲流行的多种伯氏疏螺旋体基因型,目前正在进行临床试验。
另一种创新策略是使用单克隆抗体进行被动免疫。这种方法不需要人体自身产生抗体,而是直接提供现成的抗体。一项研究发现,单剂量的抗OspA单克隆抗体可以在整个蜱虫季节提供保护。
经济的阴影
莱姆病不仅是一个健康问题,也是一个经济问题。
2022年,耶鲁大学公共卫生学院的研究人员发表了一项关于莱姆病经济负担的研究。他们估计,美国每年的莱姆病相关成本可能接近10亿美元。这包括直接的医疗费用(门诊就诊、实验室检测、抗生素治疗)和间接成本(误工、长期残疾)。
另一项研究发现,莱姆病患者平均每年比匹配对照组多花费约3000美元的医疗费用。对于发展为播散性疾病的患者,这个数字更高。
全球范围内,莱姆病的负担更难估计。欧洲每年报告的病例数估计在65,000至85,000之间,但实际数字可能更高,因为报告系统各国不一。亚洲的流行病学数据更加有限。
对于患者个人来说,莱姆病的经济影响可能是毁灭性的。误诊导致的延误治疗、反复就诊、替代治疗尝试、误工——这些都可能给家庭带来沉重的财务负担。一些患者报告花费数万甚至数十万美元在与莱姆病相关的医疗费用上。
小镇母亲的遗产
回到1975年的康涅狄格州,Polly Murray和Judith Mensch可能没有预料到她们的坚持会产生如此深远的影响。
Polly Murray后来写了一本关于她经历的书,题为《The Widening Circle: A Lyme Disease Pioneer Tells Her Story》。她在书中描述了她自己的健康挣扎,以及她如何注意到孩子们的症状与她自己的相似。她于2012年去世,享年81岁。
Judith Mensch至今仍在倡导莱姆病患者权益。她回忆说,当她第一次向卫生部门报告时,她被告知"不可能有那么多人同时患关节炎"。但她的坚持最终导致了耶鲁大学的调查。
今天,莱姆病是美国报告最多的虫媒传播疾病。每年约有30,000-40,000例确诊病例,但CDC估计实际感染人数可能高达476,000人。全球范围内,超过15%的人口可能曾经感染过伯氏疏螺旋体。
Willy Burgdorfer于2014年11月去世,享年89岁。他发现的细菌继续以他的名字命名,作为对他贡献的永恒纪念。在他生命的最后几年,他仍然关注着莱姆病研究的进展,并对慢性莱姆病的争议保持沉默,让科学自行判断。
Allen Steere继续在哈佛医学院和麻省总医院工作,领导着莱姆病研究的前沿。他现在被认为是莱姆病研究的权威之一,他的工作奠定了我们今天对这种疾病理解的基础。
尾声:未完成的战斗
莱姆病的故事远未结束。
随着气候变暖,蜱虫的栖息地将继续扩展。新的基因型、新的蜱虫物种可能带来新的挑战。研究人员正在探索新的诊断方法、新的治疗策略和新的疫苗。
但对于那些已经与莱姆病斗争多年的人来说,科学进步的速度可能太慢。慢性症状的患者继续寻找答案,医生继续在诊断的灰色地带摸索,而公共卫生官员继续在资源有限的情况下努力控制传播。
莱姆病教会我们的是:即使在现代医学时代,我们与微生物世界的斗争仍在继续。一个比芝麻还小的蜱虫,携带一种肉眼不可见的细菌,可以改变一个人一生的轨迹。而医学发现的历程——从两位母亲的警觉到科学家的显微镜——提醒我们,突破往往来自于最意想不到的地方。
在康涅狄格州的森林里,蜱虫仍在等待。它们携带着5300年前就存在于冰人体内的细菌,继续着一场比人类文明更古老的生存游戏。而我们,作为这场游戏的后来者,正在学习如何保护自己——尽管这个过程充满曲折、争议和未解之谜。
参考资料
-
Burgdorfer W, Barbour AG, Hayes SF, et al. Lyme disease—a tick-borne spirochetosis? Science. 1982;216(4552):1317-1319.
-
Steere AC, Malawista SE, Snydman DR, et al. Lyme arthritis: an epidemic of oligoarticular arthritis in children and adults in three Connecticut communities. Arthritis Rheum. 1977;20(1):7-17.
-
Benach JL, Bosler EM, Hanrahan JP, et al. Spirochetes isolated from the blood of two patients with Lyme disease. N Engl J Med. 1983;308(13):740-742.
-
Barbour AG, Benach JL. Discovery of the Lyme Disease Agent. mBio. 2019;10(5):e02166-19.
-
Steere AC, Strle F, Wormser GP, et al. Lyme borreliosis. Nat Rev Dis Primers. 2016;2:16090.
-
Radolf JD, Caimano MJ, Stevenson B, Hu LT. Of ticks, mice and men: understanding the dual-host lifestyle of Lyme disease spirochaetes. Nat Rev Microbiol. 2012;10(2):87-99.
-
Stanek G, Wormser GP, Gray J, Strle F. Lyme borreliosis. Lancet. 2012;379(9814):461-473.
-
Piesman J, Gern L. Lyme borreliosis in Europe and North America. Parasitology. 2004;129 Suppl:S191-220.
-
Nigrovic LE, Thompson AD. Lyme disease. In: Kliegman RM, St Geme JW, Blum NJ, et al, eds. Nelson Textbook of Pediatrics. 21st ed. Elsevier; 2020:1519-1523.
-
Centers for Disease Control and Prevention. Lyme Disease. https://www.cdc.gov/lyme/
-
Yale School of Public Health. Economic burden of Lyme disease could be nearly $1 billion annually. 2022.
-
Sanchez JL. Clinical manifestations and treatment of Lyme disease. Clin Lab Med. 2015;35(4):735-753.