1942年的波士顿:一个新疾病的诞生
1942年2月14日,波士顿儿科医生Stewart Clifford进行了一次例行的家访。躺在摇篮里的女婴看起来发育良好——她是一名早产儿,三个月前出生时体重不足三磅,如今已经长得白白胖胖。然而,当Clifford凑近观察婴儿的眼睛时,他的心脏几乎停止跳动。那双本该清澈明亮的眼睛此刻已经变得浑浊不透明,瞳孔后面似乎蒙着一层灰白色的膜。更令人不安的是,婴儿的眼球在不受控制地颤动——一种医学上称为眼球震颤的现象。这个孩子已经看不见了。
Clifford的病人不是孤例。在接下来的几个月里,类似的病例开始出现在波士顿的其他医院。这些婴儿有一个共同点:他们都是早产儿,出生时眼睛看起来完全正常,却在几周或几个月后莫名其妙地失明。在波士顿马萨诸塞眼耳医院的病理实验室里,一位名叫Theodore Terry的眼科医生开始收集这些病例。到1945年,他已经积累了117个病例。Terry将这种疾病命名为"晶状体后纤维增生症"(Retrolental Fibroplasia),因为他在检查这些婴儿的眼睛时发现,晶状体后方形成了异常的纤维组织。他不知道这种疾病的成因,也不知道如何治疗它。他只知道,这是一种全新的、以前从未记录过的疾病。

在1940年左右的纽约哈莱姆医院,早产儿被安置在恒温的保育室里。这些照片发表在Morris Gleich 1942年出版的《早产儿》一书中。此时,没有人意识到,在这个恒温环境中输送的氧气正在摧毁婴儿们的视网膜。
医学进步的代价:保育箱的普及与氧气的滥用
要理解这场灾难,必须先了解早产儿护理的历史。在19世纪末以前,早产儿几乎没有生存的机会。医生们对这一群体束手无策,只能将他们交给父母带回家等待奇迹。1880年,法国产科医生Stéphane Tarnier在巴黎圣母院产院发明了第一台真正意义上的保育箱。这个木制箱子底部装有一个热水容器,可以为婴儿提供稳定的温暖。Tarnier的发明将早产儿的死亡率从66%降低到了38%。
在接下来的几十年里,保育箱技术不断改进。到1930年代,美国各大城市的主要医院都已经建立了专门的早产儿护理中心。这些中心的一项关键创新是氧气治疗。早产儿常常因为肺部发育不完全而出现呼吸困难,医生们发现,向保育箱内输送高浓度的氧气可以显著改善婴儿的氧合状况,减少紫绀和呼吸窘迫。
在当时的医学界,氧气被视为一种"无害"的物质。毕竟,它是空气中天然存在的成分,人体每时每刻都在呼吸它。没有人想过要问:多少氧气是太多?也没有人想过要验证一个看似理所当然的假设:如果少量氧气对早产儿有益,那么大量氧气岂不是更好?
到1940年代后期,美国的早产儿保育室已经形成了常规做法:对所有早产儿进行高浓度氧气治疗,无论他们是否真正出现呼吸窘迫。氧气浓度常常被维持在50%到60%甚至更高,有时甚至接近100%。婴儿们在这种富氧环境中可能被放置数周甚至数月。
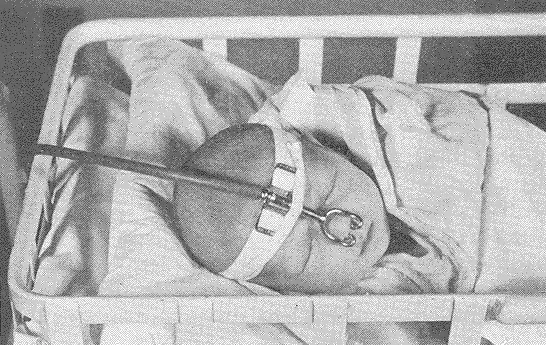
这张照片展示了1940年代向早产儿输送氧气的方法。一个叉形的金属鼻尖被固定在婴儿的鼻孔处,另一端连接着氧气罐。医生们相信氧气是"无害"的,因此慷慨地将其输送给每一个早产儿。
流行病的蔓延
到1940年代末,晶状体后纤维增生症已经演变成一场全面的流行病。病例不仅在波士顿报告,也开始出现在纽约、芝加哥、费城、伦敦、斯德哥尔摩、墨尔本——几乎所有拥有现代化早产儿护理中心的城市。一个令人困惑的现象是:这种疾病似乎更频繁地出现在富裕地区,而不是贫困地区。在设备简陋、无力负担高浓度氧气治疗的医院里,病例反而更少见。这个观察结果本应该成为一个重要线索,但当时没有人将其与氧气联系起来。
1948年,美国眼科学会的统计数据显示,晶状体后纤维增生症已经成为美国儿童失明的首要原因。在英格兰和威尔士,1947年至1949年间报告了710例病例,其中超过一半的婴儿完全失明。在澳大利亚墨尔本,1948年至1950年间报告了23例病例——而在此医院引入氧气治疗之前,从未有过类似病例的记录。
这场流行病的规模在不断扩大,但病因仍然是一个谜。研究者们提出了各种各样的理论:是维生素缺乏吗?是某种感染吗?是母亲在妊娠期间接触了某种毒素吗?还是早产儿自身的遗传缺陷?医学界的目光扫过每一个可能的因素,却唯独忽略了那个每天源源不断流入保育箱的气体。
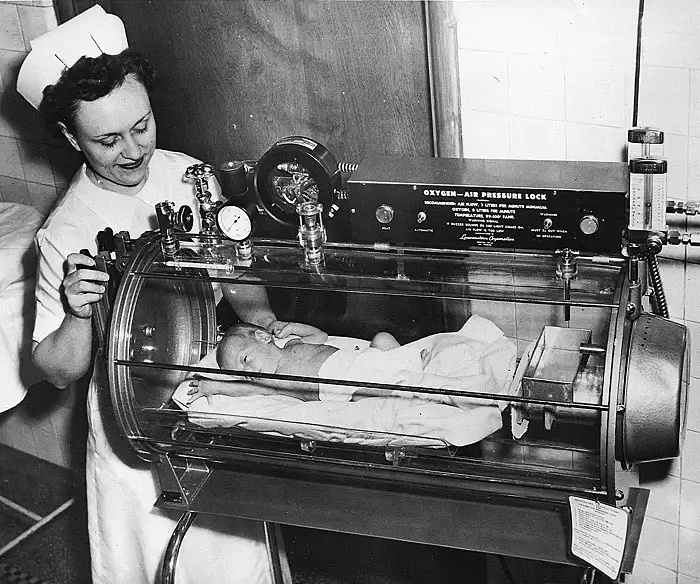
1950年,美国密苏里州圣路易斯的一家医院。这样的保育箱在当时被广泛使用,氧气通过管道持续输入箱内。医生们相信,高浓度氧气对早产儿有益无害。
巴尔的摩的年轻医生
1951年,华盛顿特区总医院的眼科住院医师Arnall Patz开始注意到一个现象。他观察到,那些患有严重晶状体后纤维增生症的早产儿,几乎都曾在保育箱中接受过长时间的高浓度氧气治疗。这个观察让他产生了怀疑:会不会正是这种被广泛认为有益无害的治疗,才是导致失明的罪魁祸首?
Patz是一个32岁的年轻人,刚从埃默里大学医学院毕业不久。他的想法在当时的医学界听起来近乎荒谬。氧气?那不是生命必需的物质吗?怎么可能导致失明?更不用说,减少氧气供应可能会危及这些脆弱婴儿的生命。任何一个提出这种假说的医生,都可能被同行视为不负责任甚至危险。
但Patz没有放弃。他与医院的儿科主任Leroy Hoeck合作,设计了一项简单的观察研究。他们发现,视网膜血管对氧气有非常敏感的反应——在高浓度氧气中,这些血管会剧烈收缩,变得细如发丝。当氧气浓度降低后,血管又会重新扩张。Patz意识到,这可能是解开谜团的关键。早产儿的视网膜血管尚未完全发育,对氧气的反应可能与成人完全不同。
Patz决定进行一项更大胆的实验。他想比较两组早产儿:一组接受常规的高浓度氧气治疗,另一组则接受较低浓度的氧气。但这需要资金支持。他向美国国立卫生研究院提交了申请,却被拒绝了——评审者们认为这个假设毫无根据,甚至可能危及婴儿的生命。
被官方拒绝后,Patz做出了一个令人难以置信的决定。他向自己的兄弟Louis借了钱,自费开展这项研究。在当时的医学界,这几乎是闻所未闻的。一个年轻的住院医师,用自己的钱去挑战整个医学界的共识,去验证一个被认为是"疯狂"的假说。

1950年,一位母亲和护士正在观察保育箱中的早产儿。没有人知道,这些被认为是在"拯救"婴儿生命的设备,正在摧毁他们的视力。
关键的临床试验
1952年,Patz和他的同事在巴尔的摩的几家医院开展了一项对照临床试验。他们将出生体重低于三磅的早产儿随机分配到两组:一组接受标准的50%至60%浓度氧气治疗,另一组则接受40%至50%的较低浓度氧气。研究的结果令人震惊。
在标准氧气治疗组中,28名婴儿里有7名发展为晶状体后纤维增生症,其中3名完全失明。在低浓度氧气组中,37名婴儿里没有一人失明,只有少数几人出现了轻微的视网膜病变。这个结果几乎以一种残酷的方式证明了Patz的假设:正是高浓度氧气导致了这些婴儿的失明。
但这个结果也引发了巨大的争议。许多医生拒绝相信,一个被广泛使用的、被认为是"救命"的治疗措施,竟然是导致失明的原因。批评者指出,Patz的研究样本量太小,方法可能存在偏倚。更重要的是,他们担心降低氧气供应会增加婴儿的死亡率。毕竟,氧气最初被引入早产儿护理,就是为了挽救那些因呼吸困难而濒死的婴儿。
Patz的研究需要一个更大规模的多中心试验来验证。这个任务落到了美国国立卫生研究院资助的一项全国性协作研究上。该研究由波士顿马萨诸塞眼耳医院的生物化学家Everett Kinsey协调,Leona Zacharias,这位在男性主导的医学界中默默工作的女科学家,是这项研究的重要参与者之一。
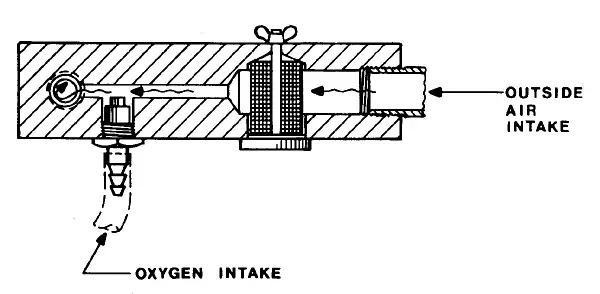
这是1954年之前使用的保育箱氧气进气装置示意图。一个双层浮阀会随着氧气流量上升,从而限制外部空气进入保育箱。这种设计使得高浓度氧气成为可能——但也正是这种"进步",夺走了数千名婴儿的视力。
国家协作研究:真相的确认
1953年至1954年间进行的全国协作研究,最终确认了Patz的发现。这项研究纳入了超过700名早产儿,采用了严格的随机对照设计。结果显示,高浓度氧气治疗组婴儿失明的风险是低浓度组的四倍以上。具体而言,在标准治疗组中,约23%的婴儿发展为晶状体后纤维增生症,而在限制氧气组中,这一比例仅为约7%。
这个结果震惊了整个儿科和眼科界。1954年9月,研究结果在美国眼科学会年会上公布。到场的医生们陷入了沉默——他们意识到,自己多年来奉行的治疗常规,实际上摧毁了无数儿童的视力。1956年,Arnall Patz和Everett Kinsey因这一发现共同获得了拉斯克奖——美国医学界的最高荣誉之一。
但Leona Zacharias的名字没有被提及。她从未获得过与她贡献相匹配的认可。在她的职业生涯中,尽管拥有博士学位并发表了多篇重要论文,她始终停留在副教授级别,从未晋升为正教授。当Patz晚年被问及Zacharias时,他承认自己从未听说过她的名字——尽管她曾与Kinsey密切合作多年。

William Silverman医生的著作《晶状体后纤维增生症:一个现代寓言》于1980年出版。Silverman是这场灾难的亲历者,他在这本书中对医学界如何犯下这一集体错误进行了深刻的反思。
氧气的毒性机制:一个生物学悖论
为什么氧气会损害视网膜?这个看似矛盾的现象背后,隐藏着一个精密的生物学机制。
人类胎儿的视网膜血管发育是一个渐进的过程。在妊娠早期,视网膜完全没有血管。血管从视神经乳头开始逐渐向外生长,最终覆盖整个视网膜表面。这个过程通常在妊娠36至40周时完成。如果一个婴儿提前出生,他的视网膜血管发育尚未完成,处于一种独特的"未成熟"状态。
在子宫内,胎儿生活在一个相对缺氧的环境中——胎儿的血氧分压大约为20至25毫米汞柱,远低于出生后的水平。在这种低氧环境中,视网膜通过产生血管内皮生长因子(VEGF)来刺激血管的持续生长。这是一种精密的适应机制:缺氧信号触发血管新生,血管新生改善氧供应,然后氧供应增加又会抑制进一步的血管新生。
当早产儿被置于高浓度氧气环境中时,这个精密的平衡被彻底打破。高浓度氧气导致视网膜血管剧烈收缩——这是一种保护性反应,旨在防止氧毒性。但血管收缩会导致血管闭塞和血管生长停止。更关键的是,高浓度氧气会强烈抑制VEGF的产生。
当这些婴儿最终被从高浓度氧气环境中移出,恢复到正常空气中时,问题才真正开始显现。此时,他们的视网膜大片区域仍然没有血管供应,处于极度缺氧状态。缺氧触发了一次爆发性的VEGF产生,刺激了大量异常新生血管的形成。这些新生血管不像正常血管那样在视网膜表面有序生长,而是杂乱无章地向玻璃体内生长。它们脆弱、易出血,最终会导致纤维组织形成、视网膜牵拉和视网膜脱离——这就是晶状体后纤维增生症的最终结局。
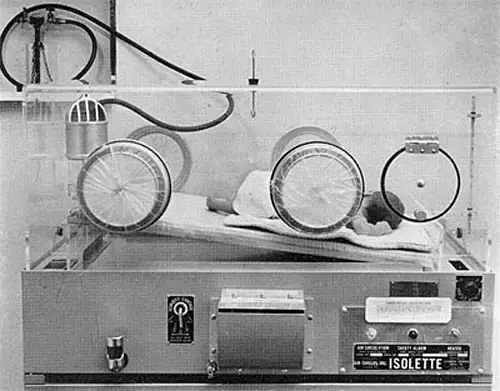
这种被称为"Isolette"的保育箱在1940年代被广泛使用。它们坚固但原始,在许多医院一直使用到1960年代和1970年代。这些保育箱能够精确控制温度和氧气浓度——但正是这种"精确",在没有充分理解氧气毒性的情况下,造成了无法挽回的伤害。
Stevie Wonder:最著名的受害者
1950年5月13日,在密歇根州萨吉诺市,一个名叫Stevland Hardaway Judkins的非裔美国婴儿提前六周来到了这个世界。他出生时只有三磅重,被立即放入了保育箱中,接受高浓度氧气治疗。几周后,医生告诉他的母亲Lula Hardaway一个毁灭性的消息:婴儿已经失明,患有晶状体后纤维增生症。
Lula Hardaway给儿子改名为Stevland Morris。后来,整个世界会以另一个名字认识他:Stevie Wonder。
Stevie Wonder的失明是这场医学灾难中最著名的案例,但他只是约一万名受害者中的一员。在那个年代,几乎每一个现代化医院的早产儿保育室都在生产着同样的悲剧。在富有的家庭中,这些失明的孩子可能会得到特殊教育和生活照顾。但在贫困的家庭中,失明往往意味着一生的边缘化和苦难。
许多受害者直到晚年才知道自己失明的真正原因。对于他们来说,那不是一场医疗事故,而是命运。他们不知道,正是医学界对"进步"的盲目追求,夺走了他们看到这个世界的权利。

1942年,摄影师Fritz Henle记录了一名护士照顾保育箱中早产儿的场景。这些照片在当时被用来展示医学进步的奇迹——没有人意识到,这些婴儿中有多少人将在未来失去视力。
错误的代价:医学界的反思
当真相被确认后,氧气治疗的标准迅速发生了改变。到1950年代中期,美国儿科学会建议将保育箱内的氧气浓度限制在40%以下,仅在婴儿出现明确的低氧血症时才使用更高浓度。晶状体后纤维增生症的发病率随之急剧下降。
但这种转变也带来了新的问题。一些医生担心,过度限制氧气可能会导致更多早产儿因缺氧而死亡或遭受脑损伤。后来的研究显示,这种担忧并非没有道理——极端低氧同样对早产儿有害。医学界花费了几十年时间,才逐渐找到了氧气治疗的"安全窗口"。
William Silverman医生是这场灾难的亲历者之一。他在哥伦比亚大学从事新生儿医学研究多年,参与了早期的协作研究。晚年,他将这段经历写成了一本书:《晶状体后纤维增生症:一个现代寓言》。在这本书中,Silverman对医学界如何犯下这一集体错误进行了深刻的反思。
他指出了几个关键问题。首先,医学界在引入一项新治疗之前,往往缺乏严格的科学验证。氧气治疗被广泛采用,不是因为有人证明了它的有效性,而是因为它"听起来有道理"。其次,当不良反应开始出现时,医学界花了太长时间才将它们与治疗本身联系起来。毕竟,承认自己可能正在伤害患者,是任何医生都难以接受的。第三,即使在证据已经相当充分的情况下,改变既有的医疗常规仍然需要很长时间——因为这意味着承认过去的错误。
Silverman写道:“在医学史上,没有多少章节像晶状体后纤维增生症这样,如此清晰地展示了医学进步与医学伤害之间的模糊边界。我们常常在追求治愈的过程中创造出新的疾病,在尝试拯救生命的过程中造成无法挽回的伤害。”
遗忘与记忆
今天,晶状体后纤维增生症已经被重新命名为"早产儿视网膜病变"(Retinopathy of Prematurity,ROP)。它仍然是早产儿面临的一个重要风险因素,尤其是在发展中国家和医疗资源有限的地区。随着新生儿重症监护技术的进步,越来越多的极低出生体重儿得以存活,其中一部分仍然会发展为不同程度的视网膜病变。
但1940年代和1950年代的那场大规模流行病,已经在公众记忆中逐渐淡去。大多数人对这段历史一无所知。即使是医学界内部,也很少有人真正反思过这一事件的深层教训。
Leona Zacharias于2006年去世,享年98岁。她的孙女、科学记者Katie Hafner在多年后才通过档案馆的资料发现了祖母在这场医学发现中的关键角色。在一篇为《科学美国人》撰写的文章中,Hafner写道:“在我的整个童年里,我只知道祖母是一个冷漠、严厉的女人。我不知道她曾参与解开一个困扰全世界医学界的谜团。我不知道她曾日夜追踪每一个可能的线索,在成堆的数据中寻找模式。我不知道她曾凝视过那些失明儿童的眼睛,试图理解为什么他们出生时健康的眼球会变成那样。”
Arnall Patz于2010年去世,享年89岁。他一生获得了无数荣誉,包括总统自由勋章。但即使在获得这些荣誉时,他仍然保持着谦逊的态度。“我可以列举出50个比我更值得这个奖项的医学科学家,“他在获得总统自由勋章时说。
而那一万名失明的儿童——他们中的大多数已经步入老年。他们从未看到过父母的面孔,从未看到过日落的颜色,从未看到过自己孩子的眼睛。他们是医学进步的沉默代价,被埋葬在教科书的一个脚注里,被遗忘在历史的一个角落中。
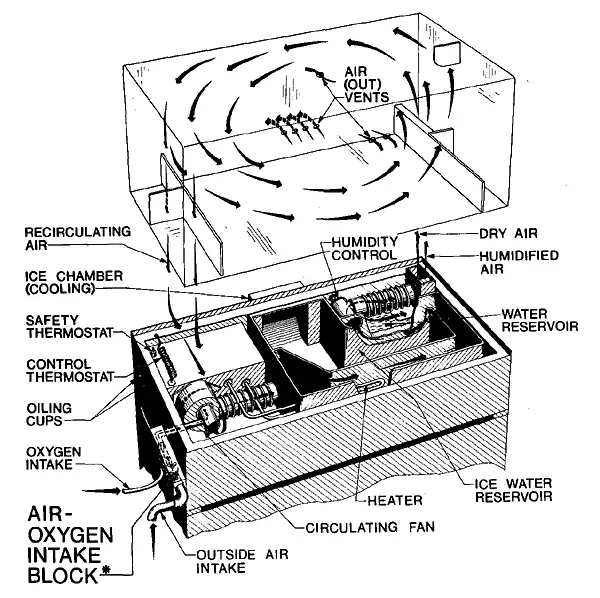
这是1954年之前使用的保育箱爆炸视图。空气以每分钟10升的速率被吸入保育箱,以防止婴儿产生的二氧化碳积累,并在打开护理通道时阻挡保育室空气进入。有机玻璃罩使护理人员可以清楚地观察到婴儿的呼吸运动。但所有这些"先进"设计,都没有考虑到一个问题:氧气本身可能是有毒的。
尾声:医学的永恒困境
早产儿视网膜病变的故事,不仅仅是一个关于氧气毒性的医学案例。它是一个关于人类如何在追求知识的过程中伤害自己的寓言。它告诉我们,医学从来不是一门纯粹的善意科学——它是一门充满了不确定性和风险的事业。每一次治疗决定,都可能在拯救与伤害之间摇摆。
那些在1940年代和1950年代失去视力的儿童,他们的失明不是因为医生的恶意,而是因为医学界集体的无知和傲慢。那些医生们真心相信自己在拯救生命,却不知道自己正在制造一场流行病。这正是这个故事最令人不安的地方:如果我们今天坚信正确的事情,实际上可能正在伤害我们的患者呢?
这个问题没有简单的答案。医学必须在尝试和错误中前进,患者必须在不确定中做出选择。但至少,我们可以记住那些沉默的受害者,记住他们的失明不是命运的安排,而是人类知识边界的一次悲剧性试探。我们可以记住Leona Zacharias这样默默无闻的科学家,记住那些在黑暗中寻找真相的孤独努力。我们可以记住,每当我们打开一个氧气阀门、开具一个处方、执行一项手术时,我们都在与未知打交道——而未知,永远是危险的。
参考资料
- Terry TL. Extreme prematurity and fibroblastic overgrowth of persistent vascular sheath behind each crystalline lens. American Journal of Ophthalmology. 1942;25:203-204.
- Patz A, Hoeck LE, De La Cruz E. Studies on the effect of high oxygen administration in retrolental fibroplasia. American Journal of Ophthalmology. 1952;35(9):1248-1253.
- Kinsey VE, Zacharias L. Retrolental fibroplasia: A cooperative study of retrolental fibroplasia and the use of oxygen. JAMA. 1956;139(9):572-578.
- Silverman WA. Retrolental Fibroplasia: A Modern Parable. New York: Grune & Stratton; 1980.
- Jacobson RM. Oxygen as a cause of blindness in premature infants: “Autopsy” of a decade of errors in clinical epidemiologic research. Journal of Clinical Epidemiology. 1992;45(11):1187-1193.
- Hellström A, Smith LE, Shen-Orr Z, et al. Retinopathy of prematurity. The Lancet. 2013;382(9902):1445-1457.
- Hafner K. Leona Zacharias Helped Solve a Blindness Epidemic among Premature Babies. She Received Little Credit. Scientific American. 2023.
- Reedy EA. The Discovery of Retrolental Fibroplasia and the Role of Oxygen: A Historical Review 1942-1956. Documenta Ophthalmologica. 2004;108(1):7-13.
- Campbell K. Intensive oxygen therapy as a possible cause of retrolental fibroplasia. Medical Journal of Australia. 1951;2(3):48-50.
- Ryan H. Retrolental fibroplasia: A clinicopathologic study. American Journal of Ophthalmology. 1952;35(11):1553-1558.
- National Cooperative Study. Cooperative study of retrolental fibroplasia. Pediatrics. 1956;18(4):583-688.
- Drack AV. Preventing Blindness in Premature Infants. New England Journal of Medicine. 1998;338(22):1624-1625.
- Hartnett ME. Retinopathy of Prematurity: Past, Present and Future. World Journal of Clinical Pediatrics. 2021;10(2):35-47.
- Shah PK, Prabhu V, Karandikar SS, et al. Retinopathy of Prematurity: Past, Present and Future. World Journal of Clinical Pediatrics. 2016;5(1):35-47.
- Carlo WA. Optimum oxygen therapy to prevent retinopathy of prematurity. Expert Opinion on Pharmacotherapy. 2010;11(12):2045-2053.
- Silverman WA. Personal reflections on lessons learned from randomized trials involving newborn infants, 1951 to 1967. James Lind Library. 2003.
- The Lesson of Retrolental Fibroplasia. Scientific American. 1977;236(6):76-85.
- Arnall Patz, MD: Physician, Scientist, and Humanitarian. JAMA Ophthalmology. 2005;123(11):1572-1574.
- Hong EH, Shin YU, Cho H. Retinopathy of prematurity: a review of epidemiology and current treatments. Clinical and Experimental Pediatrics. 2021;64(9):445-453.
- Circulating Now: Medically Manufactured: The Story of Retrolental Fibroplasia. National Library of Medicine. 2025.