1918年3月11日早晨,堪萨斯州的芬斯顿军营食堂里,一名叫阿尔伯特·吉切尔的年轻炊事兵向医务室报告自己患上了"重感冒"。他发着高烧,喉咙像被砂纸摩擦一样疼痛,全身肌肉酸痛得连站立都困难。军医 hastily 给他量了体温——39.4度——然后打发他回去休息。没有人知道,这个看似普通的决定,正在为人类历史上最致命的瘟疫拉开序幕。
吉切尔并非零号病人,但他成为第一个被正式记录的西班牙流感病例。在接下来的十八个月里,这个被称为"西班牙女士"的幽灵将席卷全球每一个角落,让五千万到一亿人在痛苦中死去——这个数字超过了第一次和第二次世界大战死亡人数的总和。更令人毛骨悚然的是,它的受害者不是通常流感偏好杀死的老人和幼儿,而是二十岁到四十岁的青壮年。一个健康年轻的小伙子早晨还在街上散步,傍晚可能就已经变成一具发黑的尸体。这些年轻人死于一种当时医生从未见过的恐怖症状:肺部充满血性液体,皮肤因缺氧变成深紫色,在清醒的状态下慢慢窒息而死。
一个世纪后的今天,科学家们终于通过逆向遗传学技术从埋葬在阿拉斯加永久冻土层的尸体中"复活"了1918年的流感病毒,揭开了这个杀手的部分面纱。他们发现,这个病毒拥有一种令人不寒而栗的能力:它能够引发一场失控的免疫风暴,让年轻强健的免疫系统反过来摧毁宿主自己的肺部。这正是为什么最健康的人反而死得最快的原因——他们的免疫系统太过强大,强大到足以杀死自己。
完美的伪装大师:一个只有八十纳米的分子艺术家
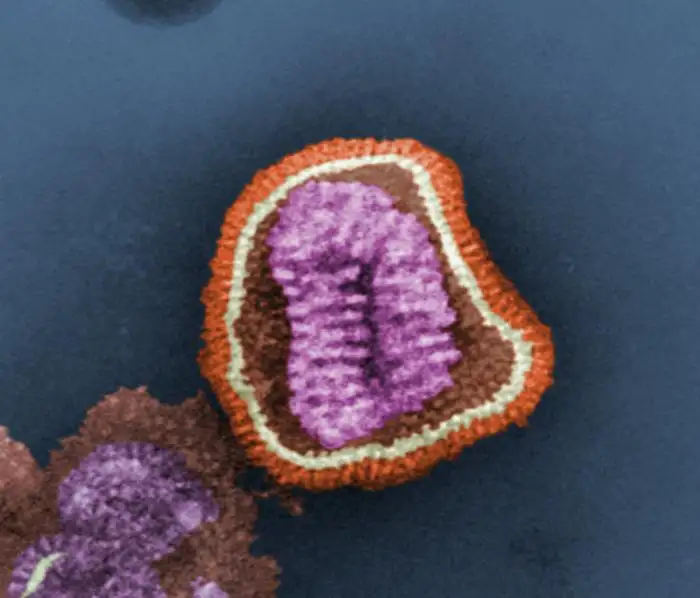
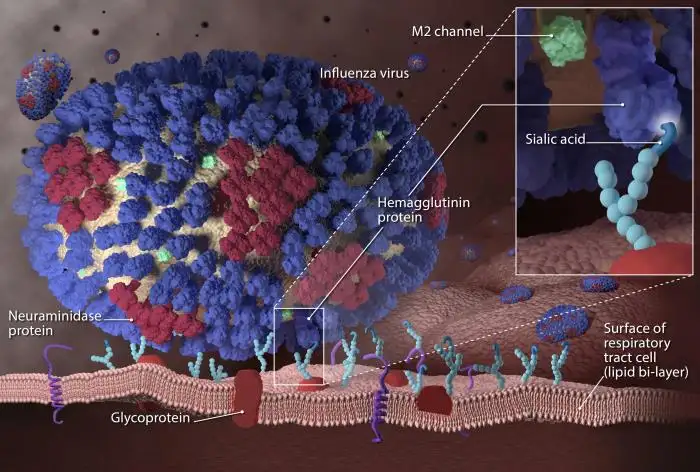
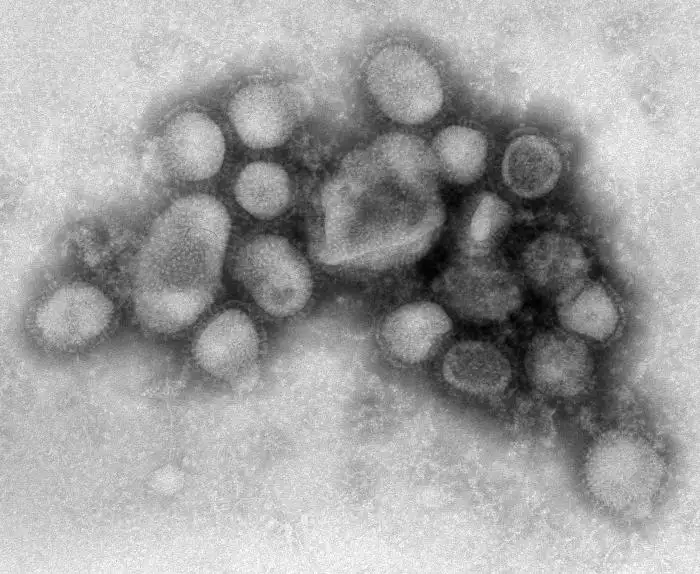
流感病毒是自然界最精巧的分子机器之一。在透射电子显微镜下,它呈现出一种诡异的美感:一个直径约八十到一百二十纳米的球形或丝状颗粒,表面覆盖着数百个像蘑菇一样的突起,整体看起来像一颗布满尖刺的微型海胆。这些突起正是流感病毒最致命的武器——血凝素和神经氨酸酶。
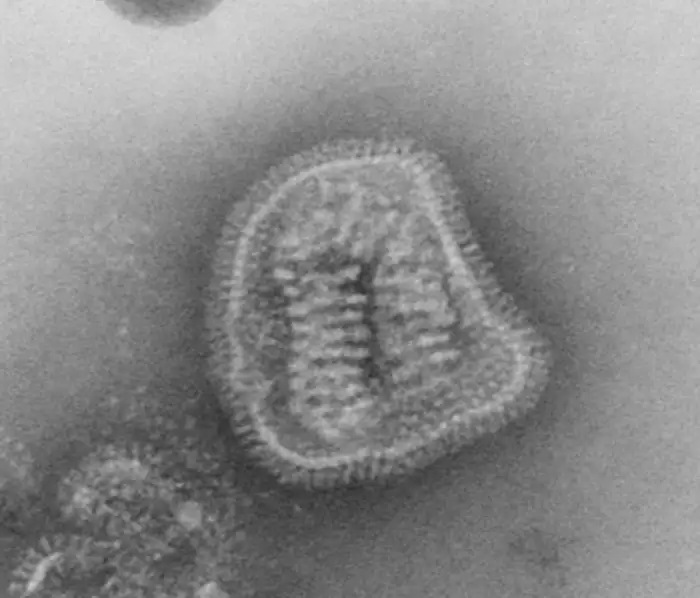
血凝素是流感病毒的"入侵钥匙"。每个血凝素分子像一根细长的钉子,顶端有一个能够精准识别并结合人类呼吸道细胞表面唾液酸受体的"锁孔"。当血凝素与受体结合后,它会触发一场分子级别的变形记:病毒的外膜与细胞膜融合,将病毒的遗传物质注入细胞内部。一个血凝素分子可以结合多个受体,这解释了为什么流感病毒如此高效——它不需要等待,一旦接触就开始入侵。
神经氨酸酶则是流感病毒的"越狱工具"。当病毒在细胞内完成复制,新产生的病毒颗粒需要离开这个已经被榨干的细胞去感染下一个受害者。但问题是,新生的病毒颗粒会被细胞表面的唾液酸受体牢牢粘住。神经氨酸酶的作用就是切断这些连接,像一把分子剪刀一样释放病毒颗粒,让它们自由地去寻找新的猎物。
这两种表面蛋白的完美配合,使流感病毒成为一台高效的感染机器。但真正让流感病毒成为人类噩梦的,是它那种近乎完美的变异能力。
流感病毒的基因组不像人类那样是一条完整的DNA链,而是被分割成八个独立的RNA片段,每个片段编码一两个蛋白质。这种分段结构听起来像是进化的意外,却成为流感病毒最狡猾的设计。当两种不同的流感病毒同时感染同一个细胞时,它们的基因组片段可以像扑克牌一样重新洗牌,产生一种全新的病毒。这种被称为"抗原转换"的过程,正是造成人类历史上所有流感大流行的罪魁祸首。
除了这种剧烈的基因重配,流感病毒还在进行着一种更隐蔽、更持续的变化——抗原漂移。流感病毒的RNA复制酶是一种"粗心"的酶,它在复制病毒基因组时平均每一万个碱基就会犯一个错误。这些随机产生的突变,绝大多数是无害甚至有害的,但偶尔会有一个突变恰好改变了血凝素或神经氨酸酶的结构,让它们不再被人体原有的抗体识别。这就是为什么流感疫苗需要每年更新的原因——病毒总是在进化,而我们的免疫系统总是在追赶。
1918年的黑色春天:当死神披上流感的伪装
1918年的春天,第一次世界大战已进入最后阶段。在欧洲的战壕里,年轻的士兵们不仅要躲避敌人的炮火,还要面对一种突如其来的怪病。这种疾病起初看起来和普通流感没什么区别:发烧、咳嗽、肌肉酸痛、疲劳。大多数患者在一周内就能康复。但仅仅几个月后,当秋天来临时,这个"温和"的访客突然露出獠牙。
1918年秋季爆发的第二波流感与春季的第一波截然不同。患者的症状变得极端恐怖:他们的脸部在几小时内变成紫黑色,肺部充满血性液体,呼吸变得像溺水者一样艰难。医生们从未见过这样的病例——患者的肺泡里充满了血细胞和纤维蛋白,肺组织被彻底破坏,就像被某种腐蚀性物质溶解了一样。尸检报告描述的肺部景象令人不寒而栗:“肺脏肿胀,重量增加,切面呈深紫色,有大量血性液体渗出。”

最令人困惑的是死亡曲线。普通流感的死亡曲线呈U形——幼儿和老人死亡率高,青壮年死亡率低。但1918年流感的死亡曲线呈W形——除了幼儿和老人,二十岁到四十岁的青壮年出现了额外的死亡高峰。这意味着病毒在以某种特殊的方式杀死最健康的人群。
现代研究终于揭开了这个谜团。2005年,美国疾病控制与预防中心的科学家们成功地从阿拉斯加永久冻土层中保存的1918年流感受害者遗体中提取并重建了病毒基因组。他们发现,1918年病毒的血凝素蛋白具有一种特殊的结构,使其能够高效地感染人类呼吸道深处的肺泡细胞——这是普通流感病毒难以到达的区域。更深层的秘密在于病毒引发的免疫反应。
当1918年流感病毒感染人体后,它会触发一场失控的细胞因子风暴。细胞因子是免疫系统的信号分子,它们在正常情况下帮助协调免疫反应。但在某些严重感染中,免疫系统会释放过量的细胞因子,导致大规模的炎症反应。年轻健康的成年人拥有更强大的免疫系统,因此当病毒触发细胞因子风暴时,他们的反应也更加剧烈——这正是他们死亡率更高的原因。换句话说,他们是被自己的免疫系统杀死的。

这场瘟疫的传播速度令人窒息。在1918年10月——死亡高峰月——仅美国就有约十九万五千人死亡。费城是受灾最严重的城市之一。10月初,城市还在举行大规模的战争债券游行,数万人拥挤在街头。几天后,医院开始爆满,停尸房堆满了尸体。城市不得不征用教堂和社区中心作为临时医院,甚至连停放尸体都成了问题——人们不得不在自家后院挖掘坟墓,因为公墓已经无处可埋。城市不得不禁止公众集会,关闭学校、剧院和教堂,但为时已晚。
在阿拉斯加的一些原住民村庄,死亡率高达百分之九十以上。整个社区在几周内被清空,只剩下一座座空荡荡的小屋和散落的白骨。在印度,死亡人数估计高达一千七百万。在整个次大陆,火葬柴堆日夜燃烧,河流中漂浮着无人认领的尸体。世界人口在那个时代总共只有约十八亿,这场瘟疫夺走了全球百分之三到百分之五的人口。
为什么这场瘟疫被称为"西班牙流感"?这是一个历史误会。当时正值战争期间,参战国对新闻实行严格审查,不允许报道任何可能影响士气的消息。西班牙是中立国,其媒体没有受到审查限制,因此最先详细报道了这场瘟疫。结果,全世界都以为这种疾病来自西班牙,而西班牙人则愤怒地称之为"法国流感"。

从鸟到人:跨越物种屏障的致命跳跃
流感病毒的天然宿主是野生水禽。在野鸭、大雁和海鸥的肠道里,流感病毒安静地生活着,通常不会引起任何症状。这些鸟类体内的流感病毒种类繁多——目前已发现十八种血凝素亚型和十一种神经氨酸酶亚型,理论上可以组合出一百九十八种不同的病毒亚型。这些病毒在鸟类体内不断演化,形成了一个巨大的基因库,随时准备着突破物种屏障。
病毒从鸟类跨越到人类,需要克服多重障碍。首先是受体特异性问题。人类呼吸道上皮细胞表面主要表达α-2,6连接的唾液酸受体,而禽类肠道上皮细胞表面主要表达α-2,3连接的唾液酸受体。禽流感病毒的血凝素经过进化,已经适应了与α-2,3受体结合,因此它们很难直接感染人类。但猪是一个例外——猪的呼吸道上皮细胞同时表达这两种受体,这使得猪成为流感病毒的"混合容器"。当禽流感病毒和人流感病毒同时感染猪时,它们可以在猪体内进行基因重配,产生一种能够感染人类的新病毒。
这就是1957年和1968年流感大流行的起源故事。1957年,一种携带禽源血凝素和神经氨酸酶基因的H2N2病毒出现在中国南部,随后迅速传播到全球。这场被称为"亚洲流感"的大流行估计造成了一百万到两百万人死亡。1968年,另一种禽源H3血凝素基因与原有人类病毒重配,产生了H3N2病毒,引发了"香港流感",估计造成了一百万到四百万人死亡。
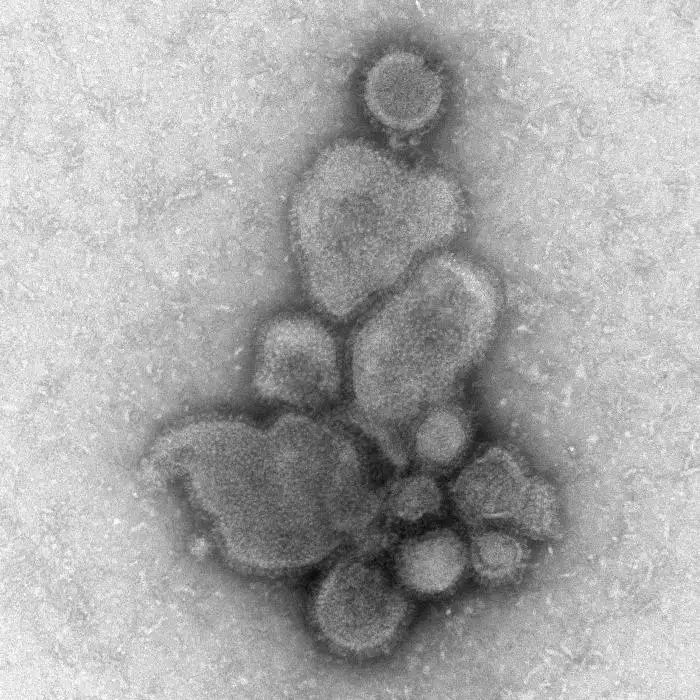
1997年,香港爆发的H5N1禽流感事件让世界看到了另一种可能性。十八人感染,六人死亡——百分之三十三的病死率远超普通流感。这是首次确认禽流感病毒直接感染人类的案例,打破了"禽流感病毒不能直接感染人类"的教条。此后,H5N1病毒在亚洲和非洲的家禽中广泛传播,多次跨物种感染人类,虽然没有人传人的能力,但每次感染都极其致命。
2013年,中国出现了H7N9禽流感病毒感染人类病例。这种病毒在禽类中几乎不引起症状,但在人类中却能造成严重疾病,病死率约为百分之三十。它像隐形的刺客一样潜伏在家禽市场中,随时准备给接触者致命一击。
然而,真正让流行病学家彻夜难眠的是H5N1病毒的进化潜力。截至2025年,H5N1病毒已经造成了近九百例人类感染,其中超过一半死亡。如果这种病毒获得了人传人的能力——哪怕只需要几个关键突变——后果将是灾难性的。世界卫生组织估计,即使是一种温和的大流行流感,也可能在全球造成两百万到七百四十万人死亡。而一种类似1918年毒力的病毒,死亡人数可能高达数千万。
季节的诅咒:为什么流感总在冬天
流感的季节性是人类观察了数千年的现象,但直到二十一世纪,科学家们才开始理解其背后的机制。为什么流感总是在冬季爆发?为什么南半球的流感季节与北半球截然相反?为什么热带地区全年都有流感传播?
2007年,俄勒冈州立大学的研究人员发表了一项突破性研究。他们分析了美国三十多年来的流感死亡数据,发现流感死亡率与绝对湿度——即空气中实际含有的水蒸气量——存在强烈的负相关。在冬季,冷空气能够容纳的水蒸气大大减少,导致绝对湿度急剧下降。这种干燥的环境对流感的传播极为有利。
其机制涉及病毒颗粒在空气中的行为。当感染者咳嗽或打喷嚏时,会释放出含有病毒的飞沫。在潮湿的环境中,这些飞沫会吸收空气中的水分,体积膨胀,更容易沉降到地面。但在干燥的冬季空气中,飞沫会迅速失去水分,收缩成轻小的干燥颗粒,能够长时间悬浮在空气中,被人吸入呼吸道。
更关键的是,流感病毒的外壳在干燥环境中变得更加稳定。2008年,美国国立卫生研究院的研究人员发现,在低湿度条件下,流感病毒能够在气溶胶中保持感染性更长时间。同时,干燥的空气会使人体呼吸道黏膜变干,削弱了第一道防线的功能,使病毒更容易入侵。
温度本身也发挥着作用。流感病毒在低温下更加稳定,这解释了为什么流感的传播高峰通常出现在最寒冷的月份。此外,冬季人们更多地在室内活动,通风减少,人群聚集增加,为病毒传播创造了理想条件。
但在热带地区,情况截然不同。这里没有明显的季节变化,流感传播呈现出更加复杂的模式。一些研究表明,热带地区的流感传播与雨季有关——降雨迫使人们更多地在室内聚集,增加了传播机会。
这种季节性规律对公共卫生策略具有重要意义。在温带地区,流感疫苗接种的最佳时机是秋季,以便在冬季流感季节开始前建立免疫保护。而在热带地区,全年接种可能更为合适。更重要的是,理解流感的季节性机制有助于预测新病毒的行为——如果一种新型流感病毒出现在南半球的冬季,北半球还有几个月的时间来准备。
疫苗的永恒追逐:一场不公平的竞赛
流感疫苗是人类对抗这种病毒的主要武器,但这场战争注定是一场不公平的竞赛。流感病毒的变异速度如此之快,以至于疫苗从设计到接种的过程中,病毒可能已经"换装"了。
目前的流感疫苗主要针对病毒表面的血凝素蛋白刺激产生的中和抗体。当人体接种疫苗后,免疫系统会产生针对特定血凝素亚型的抗体,当真正的病毒入侵时,这些抗体能够阻止病毒与细胞结合。问题在于,流感病毒通过抗原漂移不断改变血凝素的结构,使原有抗体逐渐失去效力。
世界卫生组织每年召开两次专家会议,分别决定北半球和南半球的流感疫苗毒株组成。这个过程需要提前六到八个月进行预测,因为疫苗生产需要这么长时间。专家们依靠全球流感监测网络收集的数据,分析正在传播的病毒株的抗原特性和基因序列,预测下一个流感季节最可能流行的病毒株。这种预测的准确性波动很大——有些年份预测准确,疫苗保护效果可达百分之六十以上;有些年份预测失误,保护率可能低至百分之十。

更根本的问题在于,目前的流感疫苗只能提供针对特定病毒株的保护,一旦病毒发生重大变异,疫苗就会失效。这就是为什么科学家们一直在追求"通用流感疫苗"——一种能够提供针对所有流感病毒株保护的疫苗。
通用流感疫苗的关键在于找到流感病毒中那些不变的区域。虽然血凝素的顶端——负责结合受体的部分——变异频繁,但其茎部区域相对保守。茎部在病毒入侵过程中扮演着关键角色:当血凝素与受体结合后,茎部会发生剧烈的构象变化,将病毒的遗传物质注入细胞。这个功能如此重要,以至于茎部的氨基酸序列在不同亚型之间保持着惊人的相似性。
多个研究团队正在开发针对血凝素茎部的疫苗。2024年,一些候选疫苗已经进入临床试验阶段,初步结果显示它们能够诱导广谱的免疫反应,对多种流感亚型提供保护。如果成功,这将彻底改变人类与流感的博弈——我们终于可以在这场永恒的追逐中占据上风。
另一种策略是利用信使核糖核酸技术。新冠疫情期间,信使核糖核酸疫苗的成功证明了这种平台的强大潜力。与传统疫苗需要培养病毒、纯化蛋白质不同,信使核糖核酸疫苗只需要合成编码目标蛋白质的核酸序列,大大缩短了生产时间。这意味着当新的流感病毒出现时,我们可能只需要几周而不是几个月就能生产出针对性的疫苗。
抗病毒药物:从莽草酸到达菲的化学战争
在疫苗之外,抗病毒药物是对抗流感的另一道防线。但与针对细菌的抗生素不同,抗病毒药物的开发更加困难——病毒利用宿主细胞的机制进行复制,要阻断这个过程而不伤害宿主细胞,需要极高的精准度。
第一种有效的抗流感药物是金刚烷胺,它于1966年被批准用于治疗甲型流感。金刚烷胺的作用机制是阻断病毒的离子通道蛋白,阻止病毒脱壳释放遗传物质。然而,流感病毒很快产生了耐药性——一个单点突变就能使病毒对金刚烷胺完全免疫。如今,大多数流行的流感病毒株已经对金刚烷胺耐药,这种药物实际上已经退出流感治疗的舞台。
真正的突破来自于对流感病毒神经氨酸酶的深入理解。既然神经氨酸酶帮助新生病毒颗粒从细胞表面释放,那么如果能够抑制神经氨酸酶的活性,是否就能阻止病毒传播?这个想法最终导致了神经氨酸酶抑制剂的诞生。
1999年,奥司他韦——商品名达菲——获得美国食品药品监督管理局批准上市。奥司他韦是一种神经氨酸酶抑制剂,它的分子结构与唾液酸相似,能够"欺骗"神经氨酸酶与之结合,从而阻止病毒颗粒的释放。研究表明,如果在症状出现后四十八小时内服用,奥司他韦可以将流感症状的持续时间缩短约一天,并降低并发症的风险。
然而,奥司他韦并非完美。首先,它的治疗窗口很窄——超过四十八小时再服用,效果大打折扣。其次,与金刚烷胺类似,流感病毒也可以通过突变产生对奥司他韦的耐药性。2008年,一种对奥司他韦耐药的H1N1病毒株在全球传播,引起了公共卫生界的担忧。
更新的抗流感药物正在开发中。巴洛沙韦是一种具有全新作用机制的药物,它抑制流感病毒的聚合酶——病毒复制遗传物质所必需的酶。临床试验显示,单次服用巴洛沙韦就能在二十四小时内显著降低病毒载量,比奥司他韦更快地阻断病毒传播。2018年,巴洛沙韦在日本和美国获批上市,为流感治疗提供了新的选择。
但抗病毒药物面临的最大挑战不是耐药性,而是诊断延迟。大多数流感患者在症状出现几天后才就医,此时病毒复制已经达到高峰,抗病毒药物难以发挥作用。快速诊断测试的发展可能是解决这个问题的关键——如果患者能在几分钟内确认流感诊断,就能及时开始治疗。
2009年的警告:当猪流感卷土重来
2009年春天,一种新型流感病毒在墨西哥悄然出现。起初,它被称为"猪流感",因为其基因组成与猪流感病毒相似。但这个名字引起了误解——人们以为只有接触猪才会感染,而实际上这种病毒能够在人与人之间高效传播。
世界卫生组织在2009年6月宣布这是四十一年来的首次流感大流行。病毒迅速传播到全球各地,到2010年8月大流行结束时,估计有十五万到五十七万五千人死亡。与1918年相比,这个数字似乎不大,但需要注意的是,2009年H1N1病毒的毒力相对温和,大多数死亡病例有基础疾病。
2009年大流行的真正教训在于全球应对能力。虽然各国在禽流感威胁后已经建立了大流行应对计划,但实际情况仍然混乱。疫苗生产延迟了数月,当疫苗终于到位时,最严重的疫情已经过去。抗病毒药物储备不足,分配不均。不同国家的应对策略差异巨大,缺乏协调。这场大流行是一次"实战演习",暴露了全球公共卫生体系的诸多弱点。
更重要的是,2009年大流行揭示了一个令人不安的事实:我们对流感病毒的了解仍然有限。这种病毒来自哪里?为什么它比预期更温和?为什么年轻人群的死亡率更高?这些问题至今没有完全解答。
对病毒基因组的分析显示,2009年H1N1病毒是一种复杂的重配病毒,其基因组片段来自四个不同的来源:北美猪流感病毒、北美禽流感病毒、人流感病毒和欧亚猪流感病毒。这种病毒在猪体内悄悄演化了多年,多次与其他病毒重配,最终产生了一种能够高效感染人类的全新病毒。这提醒我们,流感病毒的基因重配可以在任何时间、任何地点产生新的威胁,而我们往往在病毒已经开始传播后才意识到它的存在。
永恒的战争
流感病毒与人类的战争没有终点,只有暂时的停火。每一次大流行后,病毒都会潜伏下来,融入季节性流感的循环中,每年静静地夺走数十万生命。世界卫生组织估计,季节性流感每年导致全球约十亿人感染,其中三百万到五百万为重症病例,二十九万到六十五万人死亡。这些死亡大多发生在老年人和有基础疾病的人群中,常常被归因于其他原因,因此流感的真实负担可能被低估。
与此同时,下一次大流行的阴影始终笼罩着人类。下一次会是什么时候?会是哪种病毒?会有多致命?没有人知道答案。但我们知道的是,流感病毒将继续进化,继续寻找突破人类防线的方法。而我们能做的,是不断改进监测系统,加快疫苗研发速度,开发更有效的抗病毒药物,并建立一个能够快速响应的全球公共卫生网络。
1918年的幸存者正在逐渐离开我们,他们对那场瘟疫的记忆也随之消逝。但病毒不会忘记。它们在候鸟的肠道里、在家禽的呼吸道中、在猪的体内静静地演化,等待着下一次机会。当我们坐在温暖的房间里,抱怨又要打一针流感疫苗时,或许应该记住:我们正在与一个存在了数百万年的敌人进行着一场不公平的竞赛,而我们唯一的优势,就是知识和准备。
参考资料:
-
Taubenberger JK, Morens DM. 1918 Influenza: the Mother of All Pandemics. Emerging Infectious Diseases. 2006;12(1):15-22.
-
Morens DM, Taubenberger JK, Harvey HA, Memoli MJ. The 1918 Influenza Pandemic: Lessons for 2009 and the Future. Critical Care Medicine. 2010;38(4 Suppl):e10-e20.
-
Tumpey TM, Basler CF, Aguilar PV, et al. Characterization of the Reconstructed 1918 Spanish Influenza Pandemic Virus. Science. 2005;310(5745):77-80.
-
Webster RG, Bean WJ, Gorman OT, Chambers TM, Kawaoka Y. Evolution and Ecology of Influenza A Viruses. Microbiological Reviews. 1992;56(1):152-179.
-
Smith GJD, Vijaykrishna D, Bahl J, et al. Origins and Evolutionary Genomics of the 2009 Swine-Origin H1N1 Influenza A Epidemic. Nature. 2009;459(7250):1122-1125.
-
Shaman J, Pitzer VE, Viboud C, Grenfell BT, Lipsitch M. Absolute Humidity and the Seasonal Onset of Influenza in the Continental United States. PLoS Biology. 2010;8(2):e1000316.
-
Kuiken T, Taubenberger JK. Pathology of Human Influenza Revisited. Vaccine. 2008;26(Suppl 4):D59-D66.
-
Hilleman MR. Realities and Enigmas of Human Viral Influenza: Pathogenesis, Epidemiology and Control. Vaccine. 2002;20(25-26):3068-3087.
-
Centers for Disease Control and Prevention. 1918 Pandemic (H1N1 virus). CDC Website. 2019.
-
World Health Organization. Influenza (Seasonal). WHO Fact Sheet. 2023.
-
Nelson MI, Holmes EC. The Evolution of Epidemic Influenza. Nature Reviews Genetics. 2007;8(3):196-205.
-
Krammer F, Palese P. Advances in the Development of Influenza Virus Vaccines. Nature Reviews Drug Discovery. 2015;14(3):167-182.
-
Moscona A. Neuraminidase Inhibitors for Influenza. New England Journal of Medicine. 2005;353(13):1363-1373.
-
Pandemic Influenza Risk Management: WHO Interim Guidance. World Health Organization. 2017.
-
Viboud C, Simonsen L, Fuentes R, Flores J, Miller MA, Chowell G. Global Mortality Impact of the 1957-1959 Influenza Pandemic. Journal of Infectious Diseases. 2016;213(5):738-745.
-
Saunders-Hastings PR, Krewski D. Reviewing the History of Pandemic Influenza: Understanding Patterns of Emergence and Transmission. Pathogens. 2016;5(4):66.
-
Krammer F. The Human Antibody Response to Influenza Virus Infection and Vaccination. Nature Reviews Immunology. 2019;19(6):383-397.
-
Iuliano AD, Roguski KM, Chang HH, et al. Estimates of Global Seasonal Influenza-Associated Respiratory Mortality: A Modelling Study. The Lancet. 2018;391(10127):1285-1300.
-
Bui CM, Gardner L, MacIntyre CR. Highly Pathogenic Avian Influenza Virus, a Looming Threat. Future Virology. 2017;12(6):291-301.
-
Taubenberger JK, Kash JC. Influenza Virus Evolution, Host Adaptation, and Pandemic Formation. Cell Host & Microbe. 2010;7(6):440-451.