1901年的某个清晨,乌干达维多利亚湖畔的布索加地区,一个年轻的渔夫像往常一样划着独木舟出海。他的妻子在岸边挥手告别,孩子们在沙滩上追逐嬉戏。三个月后,这个渔夫开始感到莫名的疲倦。起初只是嗜睡,他会在划船时突然睡着,鱼从手中滑落。然后是淋巴结肿大,脖颈后面鼓起一个个拳头大小的包块。最后,他的眼神变得空洞,开始说一些没有逻辑的话语,在正午的阳光下蜷缩成一团,陷入一种永远无法醒来的睡眠。他的妻子守在床边,看着丈夫的呼吸一天天变得微弱,直到某个寂静的深夜,最后一声叹息消散在非洲的黑暗中。这不是一个孤立的故事。在接下来的二十年里,同样的命运降临在超过二十五万乌干达人身上——整个地区三分之一的人口,像被某种看不见的力量收割,悄无声息地消失在历史的尘埃里。
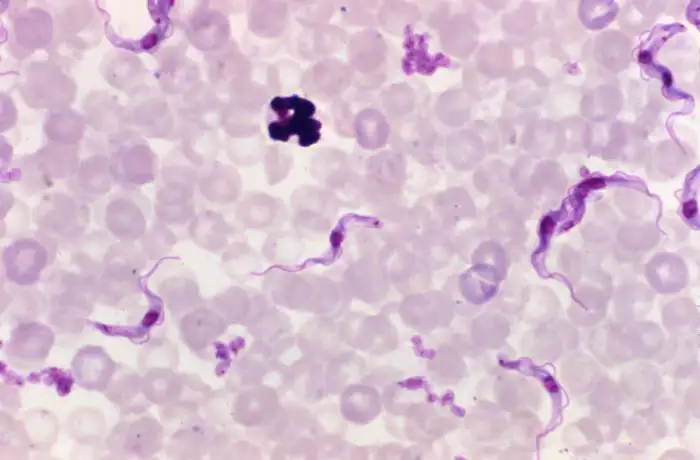
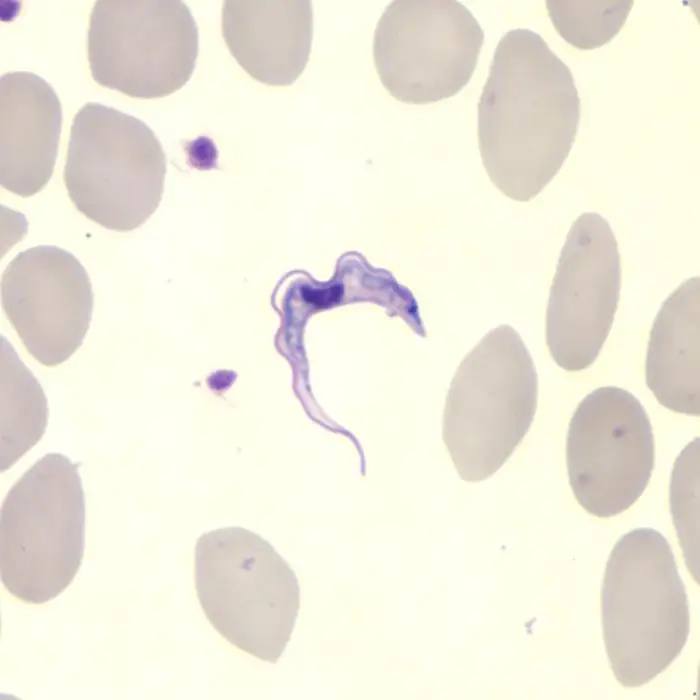
这个被称为"非洲昏睡病"或"人类非洲锥虫病"的疾病,是人类历史上最神秘、最致命的热带病之一。它的病原体是一种名为布氏锥虫的微小寄生虫,只有通过显微镜才能看见。这种单细胞生物呈细长的纺锤形,拖着一条波浪状的鞭毛,在血液中游动时如同一条迷你的鳗鱼。然而,就是这种肉眼几乎不可见的生物,在过去的一百多年里,夺走了数百万人的生命,摧毁了无数村庄,甚至改变了整个非洲大陆的历史进程。
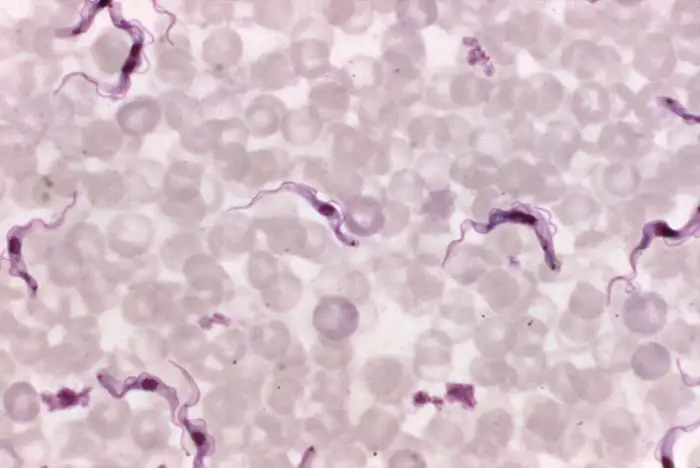
布氏锥虫的故事远不止是一场简单的疾病流行。它是人类进化史的见证者——科学家推测,这种寄生虫与它的传播媒介采采蝇已经共同存在了至少三千五百万年。在漫长的进化岁月中,非洲的野生动物发展出了对锥虫感染的耐受性,它们可以被感染却不会生病。然而,人类和他们的家畜却没有这么幸运。当第一批人类祖先从树上走下来,踏入采采蝇出没的草原时,他们遭遇了一个从未面对过的敌人。一些学者甚至认为,锥虫病可能对早期人科动物的进化产生了重要影响,促使我们的祖先发展出了某种程度的抵抗力——这解释了为什么人类对大多数锥虫种类具有天然的免疫,却唯独对布氏锥虫的两个亚种束手无策。
这两个亚种分别是布氏冈比亚锥虫和布氏罗德西亚锥虫,它们导致的疾病有着截然不同的面貌。前者主要流行于西非和中非,是一种慢性疾病,患者可以在感染后数月甚至数年才出现明显症状;后者则主要分布于东非和南非,是一种急性疾病,感染者可能在几个月内死亡。但无论是哪一种,最终的结果都是相同的——一旦寄生虫穿越血脑屏障进入中枢神经系统,患者将经历一段漫长而恐怖的死亡过程:先是睡眠周期被打乱,白天昏睡不醒,夜晚却彻夜难眠;然后是精神错乱、运动失调、感觉异常;最后是昏迷、恶病质,直至死亡。如果未经治疗,病死率几乎是百分之百。
这种疾病的传播媒介是采采蝇,一种仅分布于撒哈拉以南非洲的吸血昆虫。采采蝇的外形有些像苍蝇,但更大、更粗壮,休息时双翅会像剪刀一样交叉叠在背上。当一只携带锥虫的采采蝇叮咬人类时,它唾液中的寄生虫会被注入人体,开始一段复杂的生命旅程。锥虫首先在叮咬部位繁殖,形成一个疼痛的溃疡,称为"下疳"。然后,它们进入血液和淋巴系统,开始大规模复制。在这个阶段,患者会出现发热、头痛、关节痛和淋巴结肿大等症状——这些症状与疟疾、伤寒等常见热带病太过相似,使得早期诊断极其困难。

然而,布氏锥虫最令人震惊的特征,是它躲避人体免疫系统的狡诈本领。这种寄生虫的表面覆盖着一层致密的糖蛋白外壳,被称为"变异表面糖蛋白"。每个锥虫细胞表面约有1000万个这样的糖蛋白分子,形成一道密不透风的屏障。当人体的免疫系统产生针对这种糖蛋白的抗体,开始清除寄生虫时,一小部分锥虫会突然"换装"——它们通过基因重组,将表面的糖蛋白换成一种全新的类型。人体的抗体顿时失去了目标,而锥虫则趁机重新繁殖。这个过程会不断重复,患者体内的锥虫数量会呈现波浪式的起伏,每一次低谷都伴随着新的糖蛋白类型出现。科学家已经发现,布氏锥虫基因组中含有超过1000个不同的VSG基因,这意味着在理论上,这种寄生虫可以进行无数次"换装",永远领先人体的免疫系统一步。
这种抗原变异机制的发现,是二十世纪免疫学最激动人心的故事之一。它不仅揭示了病原体如何与宿主进行一场分子层面的军备竞赛,也为疫苗研发投下了长长的阴影——对于一种可以不断改变外表的寄生虫,传统的疫苗策略几乎毫无用武之地。更令人称奇的是,布氏锥虫的基因组本身就是一个进化的奇迹。它的线粒体DNA——被称为"动基体DNA"——以数千个小环和几十个大环相互锁扣的方式组织,形成一个篮球网般的复杂结构。这种独特的基因组结构,使锥虫能够在采采蝇体内经历一系列复杂的形态变化,最终发育成具有感染能力的形态。
当锥虫最终突破血脑屏障,进入中枢神经系统时,疾病进入了最可怕的阶段。血脑屏障是人体最坚固的防线之一,它由紧密连接的血管内皮细胞组成,阻挡大多数有害物质进入大脑。然而,布氏锥虫找到了绕过这道防线的方法。研究表明,锥虫可能通过多种途径进入大脑:它们可以诱导血管内皮细胞产生炎症反应,使血脑屏障变得渗漏;它们也可以通过主动穿越血管内皮细胞的方式进入脑组织。一旦进入中枢神经系统,锥虫会引发严重的脑膜脑炎,导致大脑实质的炎症和损伤。患者的脑脊液中会出现大量淋巴细胞和浆细胞,同时可以检测到锥虫的存在。在这个阶段,睡眠障碍成为最典型的症状——患者白天极度嗜睡,甚至在吃饭或交谈时突然睡着;夜晚却无法入睡,表现出明显的睡眠-觉醒周期颠倒。这种独特的症状,正是"昏睡病"名称的由来。
昏睡病的历史是一部交织着科学发现、殖民主义和人道主义灾难的复杂叙事。在欧洲殖民者到达非洲之前,这种疾病已经在当地流行了数百年。阿拉伯历史学家伊本·哈尔敦在十四世纪的著作中,就描述过马里帝国的一位苏丹死于一种令人昏睡不止的疾病。奴隶贸易时期,欧洲船医们注意到,许多非洲奴隶在海上航行期间出现奇怪的嗜睡症状,最终死亡。阿拉伯奴隶贩子们甚至已经知道,如果一个人颈后淋巴结肿大,就不应该购买他——这是早期昏睡病的重要体征之一,后来以英国医生托马斯·温特伯顿的名字命名为"温特伯腾征"。
然而,真正的大规模流行始于殖民时代。十九世纪末,随着欧洲列强瓜分非洲,大规模的人口迁移、贸易活动和生态破坏打破了原有的疾病平衡。1896年至1906年间,一场毁灭性的昏睡病流行席卷乌干达和刚果盆地。在乌干达的布索加地区,三十万人口中有二十万在短短五年内死于这种疾病。整个村庄被遗弃,农田荒芜,尸体无人埋葬。英国驻乌干达总督赫斯克斯·贝尔在日记中写道:“昏睡病问题笼罩着我在这里的一切工作。“一位英国外交部官员则称这场流行病"对热带非洲来说简直是一场灾难”。
这场流行病的爆发,与此前席卷非洲的牛瘟大流行有着密切的关系。1889年,随意大利入侵厄立特里亚传入的牛瘟病毒在短短几年内杀死了非洲90%以上的牛群,造成了大规模的饥荒和社会动荡。牧民们被迫放弃畜牧业,转而进入丛林狩猎和采集。当牛群消失后,灌木丛重新占领了牧场,野生动物种群恢复,采采蝇也随之卷土重来。人类与采采蝇栖息地的重叠增加,为疾病的传播创造了理想条件。

面对这场前所未有的人道主义危机,欧洲殖民政府派出了多支科学考察队前往非洲研究这种疾病。1902年,英国皇家学会派遣的一支考察队在乌干达的恩德培建立了研究基地。考察队成员、意大利医生阿尔多·卡斯特拉尼在患者的脑脊液中发现了锥虫的存在。次年,著名的苏格兰细菌学家大卫·布鲁斯带领第二支考察队抵达,他确认了卡斯特拉尼的发现,并证明了采采蝇是疾病的传播媒介。布鲁斯的发现建立在更早的研究基础上:1895年,他已经在南非发现了锥虫是牛锥虫病的病原体——这种被称为"纳加纳"的疾病,多年来一直是非洲畜牧业的噩梦。为了纪念他的贡献,锥虫属的学名最终被定为"布氏锥虫”。
然而,科学发现的荣耀背后,是一段更加黑暗的历史。1906年,德国著名科学家罗伯特·科赫——因发现结核杆菌和霍乱弧菌而闻名于世——带领一支考察队来到维多利亚湖的塞塞群岛,这里是当时昏睡病流行最严重的地区之一。科赫在这里建立了一个他称之为"集中营"的研究营地,对当地居民进行大规模的人体实验。他测试了各种砷剂药物的治疗效果,其中最主要的是一种名为"阿托西"的化合物。在1622名接受阿托西治疗的患者中,科赫观察到22人出现了视神经萎缩,导致完全失明。这种被宣传为"低毒"的药物,实际上治疗指数接近于1——意味着治愈寄生虫所需的最小剂量几乎与患者的最大耐受剂量相同。
科赫在非洲的所作所为,揭示了殖民医学最阴暗的一面。非洲人被当作实验材料,在没有知情同意的情况下接受危险的药物治疗。这些实验的伦理问题至今仍然引发争议。科赫本人似乎对这些伦理问题毫无意识,他在报告中详细记录了各种药物对非洲患者的副作用,却从未考虑过这些患者的命运。塞塞群岛的"集中营"成为了殖民医学的象征——一个科学进步与人权侵犯并存的空间。
与此同时,英国殖民政府采取了另一种策略。在总督赫斯克斯·贝尔的推动下,乌干达实施了大规模的强制迁移政策。所有居住在维多利亚湖沿岸和岛屿上的居民被命令搬迁到离湖岸两英里以上的地区,捕鱼和销售鱼类被严格禁止。贝尔写道:“我们必须从昆虫那里夺走感染的来源。整个国家必须被清空人口。“这项政策造成了巨大的社会苦难,渔民失去了生计来源,农民被迫离开肥沃的土地。然而,从流行病学的角度来看,它确实有效——1900年至1904年间,感染地区有20万人死于昏睡病;而1905年至1909年间,死亡人数下降到不足25000人。
然而,强制迁移和隔离政策并没有根治疾病。当第一次世界大战爆发,欧洲殖民者忙于相互厮杀,昏睡病的控制工作陷入停滞。战后,德国的殖民地被瓜分,昏睡病的流行再次加剧。1920年代,第二波大规模流行开始了。这一次,殖民政府有了更多的武器。法国医生欧仁·雅莫开创了一种新的控制方法:使用流动医疗队系统性地筛查和治疗患者,目的是消除寄生虫在人群中的储存库。在喀麦隆,雅莫的方法取得了显著效果——在11年内,昏睡病的患病率从1919年的60%下降到1930年的0.2%至4.1%。这种方法后来被其他殖民国家广泛采用。
药物治疗的发展历程同样充满了曲折和悲剧。早期的药物主要是各种砷剂化合物,它们有效但毒性极大。阿托西虽然能够杀死锥虫,却会导致失明。另一种名为"苏拉明"的药物由德国拜耳公司在1916年开发,至今仍是治疗早期罗德西亚锥虫病的首选药物。然而,对于已经进入中枢神经系统的晚期患者,苏拉明无能为力。第一种能够治疗晚期昏睡病的药物是"锥虫胂胺”,由美国洛克菲勒研究所的科学家在1919年开发。然而,这种药物同样具有严重的副作用,包括视神经损伤和肾脏损害。
1949年,瑞士科学家恩斯特·弗里德海姆开发了一种新的砷剂药物——美拉胂醇。这种药物成为治疗晚期昏睡病——特别是罗德西亚锥虫病——的主要药物,并且至今仍是唯一有效的选择。然而,美拉胂醇的毒性令人胆寒。它会导致5%至10%的患者出现"治疗后反应性脑病”,一种可能致命的脑部炎症反应。在这些患者中,有1%至5%最终死亡。更令人不安的是,这种药物本身的成分——有机砷——就是剧毒物质。医生们在给患者注射时必须格外小心,因为药物如果漏出血管,会导致周围组织的严重坏死。在某些治疗中心,接受美拉胂醇注射的患者会被绑在床上,以防止他们在剧烈的药物反应中伤害自己。
二十世纪后半叶,随着非洲国家的独立,昏睡病的控制工作面临新的挑战。许多新独立的国家缺乏足够的医疗资源和基础设施,控制项目被中断。1960年代,昏睡病的发病率降至历史最低点,人们一度认为这种疾病即将被消灭。然而,这种乐观很快被证明是过早的。1970年代开始,第三波大规模流行席卷了安哥拉、刚果民主共和国、苏丹南部和乌干达。到世纪之交,每年的新发病例估计达到五十万例,几乎回到了二十世纪初的水平。
在这个最黑暗的时刻,出现了一线曙光。一种名为"依氟鸟氨酸"的药物,原本是作为抗癌药物开发的,却意外地被发现对冈比亚锥虫病有效。与美拉胂醇不同,依氟鸟氨酸的毒性要低得多,成为治疗晚期冈比亚锥虫病的首选药物。然而,它需要复杂的给药方案——每六小时静脉注射一次,持续十四天——这在许多非洲农村地区难以实施。更糟糕的是,由于市场需求有限,制药公司一度停止了依氟鸟氨酸的生产,引发了全球药物短缺的危机。
转机出现在2001年。在世界卫生组织的协调下,赛诺菲和拜耳两家制药公司同意免费提供昏睡病治疗药物,由无国界医生组织负责分发。这一举措挽救了无数生命。同时,新的诊断和治疗技术也在不断发展。一种新的联合疗法——将依氟鸟氨酸与另一种名为"硝呋莫司"的药物联合使用——被证明同样有效,但给药方案大大简化。2009年,世界卫生组织将这种联合疗法列入基本药物清单。
近年来,昏睡病治疗领域迎来了革命性的进展。2018年,一种名为"非昔硝唑"的口服药物成为第一种可用于治疗昏睡病的口服疗法。患者只需每天服用一次,持续十天,无需住院治疗。这彻底改变了昏睡病的管理方式——过去需要腰椎穿刺来确定疾病阶段、需要在医院进行静脉注射治疗,现在可以在基层医疗机构甚至社区层面完成。更令人兴奋的是,一种名为"阿考齐硼醇"的新药正在进行临床试验,它可能实现单剂量口服治愈的目标。如果成功,这将是昏睡病治疗史上最大的突破之一。
这些进步反映在流行病学数据上。根据世界卫生组织的统计,昏睡病的新发病例已经从1998年的近四万例下降到2020年的不足一千例。2025年,肯尼亚成为最新一个宣布消除昏睡病作为公共卫生问题的国家。然而,科学家们警告说,根除这种疾病仍然面临重大挑战。采采蝇分布在撒哈拉以南非洲约一千万平方公里的区域内,涉及三十六个国家。锥虫的动物储存库——包括野生动物和家畜——使得完全消灭病原体几乎不可能。此外,疾病的流行与社会经济条件密切相关:贫困、战争和人口流动都会增加传播风险。2013年至2020年间,中非共和国和南苏丹的内战导致医疗服务中断,昏睡病的发病率再次上升。
回望昏睡病的历史,我们看到的不仅是一种疾病的故事,更是人类与自然、科学与伦理、殖民与独立之间复杂纠葛的缩影。从十四世纪马里帝国苏丹的神秘死亡,到二十一世纪口服药物的开发;从罗伯特·科赫在塞塞群岛的人体实验,到无国界医生在战区的紧急救治;从砷剂药物的残酷治疗,到单剂量口服药的曙光——这条漫长的道路见证了人类医学的进步,也留下了不可磨灭的伤痕。今天,当我们在显微镜下观察布氏锥虫那优雅的纺锤形身躯时,我们看到的不仅是一种病原体,更是一个与人类纠缠了千年的古老敌人。它的故事远未结束——在非洲大陆的某个角落,采采蝇仍在等待,锥虫仍在变异,而人类与这个隐形杀手的斗争,也将继续下去。
参考资料
- Steverding D. The history of African trypanosomiasis. Parasites & Vectors. 2008;1(1):3.
- Headrick DR. Sleeping sickness epidemics and colonial responses in East and Central Africa, 1900-1940. PLoS Neglected Tropical Diseases. 2014;8(4):e2772.
- Fèvre EM, et al. Reanalyzing the 1900-1920 sleeping sickness epidemic in Uganda. Emerging Infectious Diseases. 2004;10(4):567-573.
- Cox FEG. History of sleeping sickness (African trypanosomiasis). Infectious Disease Clinics of North America. 2004;18(2):231-245.
- Kennedy PGE. Human African trypanosomiasis of the CNS: current issues and challenges. Journal of Clinical Investigation. 2004;113(4):496-504.
- Pinger J, et al. Variant surface glycoprotein density defines an immune shield. Nature Communications. 2017;8(1):160.
- De Koning HP. The drugs of sleeping sickness: their mechanisms of action and resistance. Frontiers in Microbiology. 2020;11:1606.
- Fairlamb AH. Melarsoprol resistance in African trypanosomiasis. Trends in Parasitology. 2018;34(6):481-492.
- Nikolskaia OV, et al. Blood-brain barrier traversal by African trypanosomes requires calcium signaling. Journal of Clinical Investigation. 2006;116(10):2739-2747.
- World Health Organization. Trypanosomiasis, human African (sleeping sickness). WHO Fact Sheet. 2023.
- MacLean L, et al. Stage progression and neurological symptoms in Trypanosoma brucei rhodesiense sleeping sickness. PLoS Neglected Tropical Diseases. 2012;6(12):e1857.
- Lindner AK, et al. New WHO guidelines for treating rhodesiense human African trypanosomiasis. The Lancet Infectious Diseases. 2025;25(1):e3-e4.
- Bentivoglio M, et al. Cell trafficking in the brain: 100 years of research on the blood-brain barrier. Trends in Neurosciences. 2014;37(6):284-293.
- Masocha W, et al. Cerebral vessel laminins and IFN-γ define Trypanosoma brucei brucei penetration of the blood-brain barrier. Journal of Clinical Investigation. 2004;114(5):689-694.
- Mugnier MR, et al. Antigenic variation and the VSG coat in Trypanosoma brucei. Current Opinion in Microbiology. 2016;32:100-105.
- Aksoy S, et al. Trypanosome transmission dynamics in tsetse. Current Opinion in Insect Science. 2014;3:43-49.
- Bouteille B, et al. The detection and treatment of human African trypanosomiasis. Research and Reports in Tropical Medicine. 2012;3:35-45.
- Rotureau B. African trypanosome development in the tsetse fly. Frontiers in Cellular and Infection Microbiology. 2013;3:53.
- Lutumba P, et al. Human African trypanosomiasis in a rural community, Democratic Republic of Congo. PLoS Neglected Tropical Diseases. 2007;1(2):e128.
- Baker CH. The long wait for a new drug for human African trypanosomiasis. Trends in Parasitology. 2018;34(10):830-839.