沙漠新娘的第一个吻
公元十世纪的波斯,一位名叫伊本·西纳的年轻医生正在布哈拉的宫廷中行走。他刚刚完成了一部将改变医学史的著作,但此刻他的注意力被一位来自巴尔赫的病人吸引。这位病人的脸上长着一个奇特的溃疡,边缘隆起,中央凹陷,像一座微型的火山口。伊本·西纳在医书中记载了这种疾病,他将其称为"巴尔赫疮",这是人类历史上第一次对皮肤利什曼病进行准确的临床描述。
这个看似寻常的皮肤溃疡背后,隐藏着一个跨越千年的恐怖故事。在随后的岁月里,这种疾病将以各种名字出现在人类的医学文献中:东方疮、阿勒颇疖、德里疮、巴格达疮。每一个名字都代表着一片被它侵袭过的土地,每一片土地上都留下了无数受害者难以磨灭的伤疤。然而直到二十世纪初,人类才真正看清了这位隐形杀手的真面目——一种名为利什曼原虫的单细胞寄生虫,它通过一种几乎看不见的昆虫传播,在人体的免疫系统内部建立起自己的殖民地。
世界卫生组织将其列为最重要的被忽视热带病之一。每年,全球约有七十万到一百万人新感染利什曼病,约十亿人口生活在感染风险区域。它有三个主要类型:皮肤利什曼病是最常见的形式,每年导致六十万到一百万新病例,患者面部和四肢留下终身疤痕;黏膜皮肤利什曼病会侵蚀鼻腔、口腔和咽喉的黏膜组织,造成可怕的毁容;而内脏利什曼病,又称黑热病,是最致命的形式,如不接受治疗,死亡率高达百分之九十五。在人类的疾病谱系中,很少有疾病能像利什曼病这样,同时展现出如此多样的临床表现和如此高的致死率。
看不见的使者
白蛉是利什曼病的传播媒介,这些微小的昆虫在疾病传播中扮演着至关重要的角色。白蛉属于双翅目白蛉科,全球已知有超过九百种,其中约七十种被证实或怀疑能够传播利什曼原虫。它们只有两到三毫米长,足以穿过普通的蚊帐,毛茸茸的身体和尖细的翅膀让它们看起来像是缩小的飞蛾。当雌性白蛉叮咬感染者时,它们吸入含有无鞭毛体的血液。在白蛉的肠道内,无鞭毛体迅速转变为前鞭毛体并进行大量繁殖。当白蛉再次叮咬新的宿主时,前鞭毛体被注入皮肤,开始新一轮的感染。

在旧大陆,主要传播媒介属于白蛉属;在新大陆,主要传播媒介属于罗蛉属。白蛉的生命周期包括卵、幼虫、蛹和成虫四个阶段。雌性白蛉需要吸血才能产卵,它们主要在黄昏和黎明时分活动,叮咬各种哺乳动物包括人类。幼虫生活在潮湿、富含有机物的环境中,如啮齿动物洞穴、垃圾堆积处和建筑废墟。这种生态特点解释了为什么在人类居住环境恶化时,如战争和自然灾害期间,白蛉密度和利什曼病发病率往往会增加。
两个名字一个谜题
一九〇三年五月,一位名叫威廉·利什曼的英国军医在伦敦的皇家陆军医学院报告了一项重要发现。他在一名死于"黑热病"的印度士兵的脾脏中发现了大量微小的寄生生物。利什曼描述这些生物为"椭圆形小体",每个都包含两个深染的结构——一个是细胞核,另一个是一个特殊的细胞器,后来被称为动基体。他推测这是一种新的寄生虫,但当时无法确定它的分类地位。
同一年,在印度马德拉斯工作的爱尔兰医生查尔斯·多诺万也在黑热病患者的脾脏穿刺标本中观察到了同样的寄生虫。多诺万进一步证明,这些寄生虫可以通过脾脏穿刺从活体患者中获得,这为临床诊断开辟了新的途径。为了纪念这两位几乎同时发现的科学家,人们将黑热病脾脏中发现的寄生虫形态命名为"利什曼-多诺万小体"。
然而,一个关键的问题仍然悬而未决:这种寄生虫是如何从一个人传播到另一个人的?一九〇八年,巴西科学家加斯帕·维亚纳在研究皮肤利什曼病时发现了寄生虫的另一种形态——一种细长的、带有鞭毛的形式,他称之为"前鞭毛体"。这一发现揭示了利什曼原虫复杂的生活史:它能够在两种截然不同的形态之间转换,适应完全不同的生存环境。
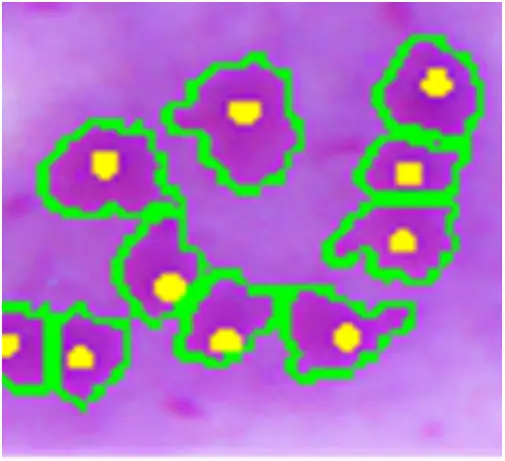
利什曼原虫的无鞭毛体是椭圆形的寄生虫,长约二到四微米,具有一个偏心的细胞核和副核动基体。它们可以在巨噬细胞的细胞质内或细胞外被发现,常常呈现出"蜂群"样的排列。这是诊断利什曼病的关键形态学特征。
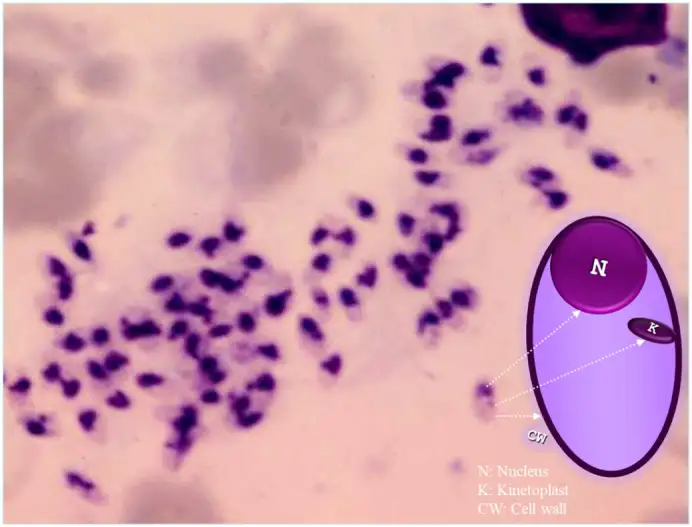
一九二四年,英国科学家斯诺和印度科学家克里希南最终确认了传播媒介——白蛉。这些微小的、毛茸茸的昆虫只有两到三毫米长,足以穿过普通的蚊帐。当雌性白蛉叮咬感染者时,它们吸入含有无鞭毛体的血液。在白蛉的肠道内,无鞭毛体转化为前鞭毛体并进行大量繁殖。当白蛉再次叮咬新的宿主时,前鞭毛体被注入皮肤,开始新一轮的感染。
温度与酸性的死亡信号
当利什曼原虫被巨噬细胞吞噬后,它必须完成一个惊人的转变:从细长的、有鞭毛的前鞭毛体转变为圆形的、无鞭毛的无鞭毛体。这个转变的触发因素是温度和酸度的双重变化。在白蛉体内,寄生虫生活在约二十五摄氏度的环境中;而在哺乳动物体内,温度骤升至三十七摄氏度或更高。与此同时,吞噬体内部的酸度急剧增加,pH值降至五点五左右。
实验室研究表明,将前鞭毛体暴露于高温和酸性环境中,可以在试管中诱导其转变为无鞭毛体,这个过程被称为"体外无鞭毛体化"。不同种类的利什曼原虫对温度的适应性不同:引起内脏利什曼病的杜氏利什曼原虫和婴儿利什曼原虫适应三十七摄氏度的体温,而引起皮肤利什曼病的墨西哥利什曼原虫和巴西利什曼原虫则适应三十二到三十四摄氏度的皮肤温度。这种温度偏好的差异决定了寄生虫在人体内的归宿:是停留在皮肤引起局部溃疡,还是侵入内脏器官造成系统性感染。
在转变过程中,寄生虫经历剧烈的代谢重组。与翻译和核糖体生物合成相关的基因表达大幅下调,这反映了无鞭毛体较低的增殖速率。与此同时,与应激反应、脂肪酸代谢和氧化应激反应相关的蛋白质合成增加。一种名为A2的蛋白质家族在无鞭毛体中高度表达,它们由多个十氨基酸重复序列组成,与寄生虫在哺乳动物宿主体内的存活能力密切相关。研究表明,A2蛋白的主要功能是保护寄生虫免受应激损伤。
热休克蛋白在这一转变过程中扮演着核心角色。当利什曼原虫从白蛉进入哺乳动物时,温度上升超过十摄氏度,这构成了一个强烈的热应激信号。热休克蛋白九十和热休克蛋白七十作为分子伴侣,负责帮助其他蛋白质在应激条件下保持正确的折叠。研究发现,用热休克蛋白九十的抑制剂处理前鞭毛体,可以诱导其向无鞭毛体样形态转变,这表明热休克蛋白九十不仅是应激反应的一部分,更是调控寄生虫发育阶段的关键分子开关。
最危险的居所
巨噬细胞是人体免疫系统的重要成员,专门负责吞噬和消化入侵的病原体。当巨噬细胞吞噬细菌或真菌时,它会激活一系列强有力的杀菌机制:吞噬体与溶酶体融合,产生大量活性氧和氮中间体,释放各种蛋白水解酶。对于绝大多数微生物来说,进入巨噬细胞的吞噬溶酶体意味着必死无疑。然而,利什曼原虫不仅选择主动进入巨噬细胞,而且将吞噬溶酶体作为自己的居所,这是寄生虫界最惊人的生存策略之一。
利什曼原虫入侵巨噬细胞的过程是一个精心设计的欺骗游戏。前鞭毛体表面覆盖着一层厚厚的脂磷酸糖,这是一种由重复的二糖单元组成的复杂糖脂分子。脂磷酸糖不仅是寄生虫附着于巨噬细胞表面的粘附分子,更是一种强大的免疫调节剂。当寄生虫被吞噬后,脂磷酸糖会干扰吞噬体的正常成熟过程,抑制吞噬体与溶酶体的融合,减少活性氧的产生。
另一种关键的毒力因子是GP63蛋白酶,这是一种位于寄生虫表面的锌金属蛋白酶。GP63能够切割多种宿主蛋白质,包括补体成分、信号转导蛋白和转录因子。在寄生虫入侵时,GP63帮助将补体C3b裂解为iC3b,后者通过巨噬细胞表面的补体受体介导寄生虫的吞噬。这一过程至关重要,因为通过补体受体进入巨噬细胞的寄生虫不会触发强烈的呼吸爆发,从而避免了活性氧的大量产生。
一旦进入吞噬溶酶体,无鞭毛体必须应对多重威胁。首先是酸性环境,吞噬溶酶体的pH值约为四点五至五点零,足以杀死大多数微生物。利什曼原虫通过表达一种质子泵来调节其内部pH值,同时其表面的脂磷酸糖能够中和部分酸性。其次是各种蛋白水解酶,寄生虫通过分泌自身的蛋白酶抑制剂来对抗溶酶体酶的攻击。第三是氧化应激,巨噬细胞会产生一氧化氮和活性氧来杀死入侵者,而利什曼原虫则通过表达抗氧化酶如过氧化物酶和超氧化物歧化酶来保护自己。
利什曼原虫还会主动干扰宿主细胞的信号转导通路。研究发现,感染利什曼原虫的巨噬细胞会下调主要组织相容性复合体II类分子的表达,这削弱了巨噬细胞向T细胞呈递抗原的能力。同时,寄生虫会诱导巨噬细胞产生白细胞介素-10,这是一种强效的抗炎细胞因子,能够抑制巨噬细胞的杀菌活性。通过这些手段,利什曼原虫不仅在自己的死亡陷阱中存活下来,而且将其转化为一个安全的避风港。
三张面孔的诅咒
利什曼病的三种主要临床类型反映了寄生虫与宿主之间复杂的相互作用。皮肤利什曼病是最常见的形式,占所有病例的百分之七十五以上。感染通常发生在白蛉叮咬的部位,最初表现为一个小丘疹,随后逐渐扩大形成溃疡。溃疡边缘隆起,中央覆盖坏死组织,呈现出典型的"火山口"外观。
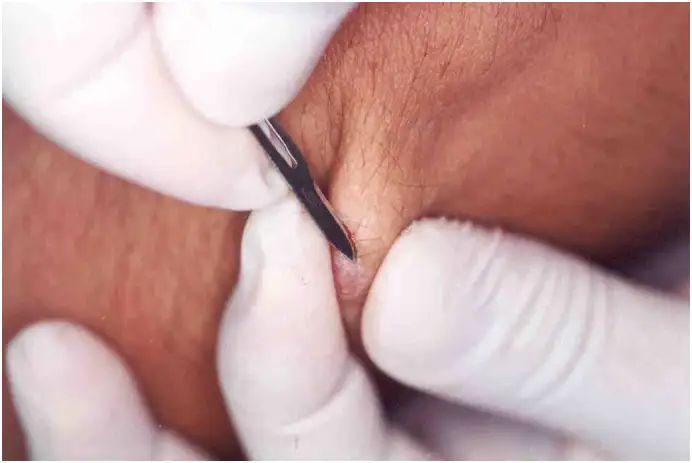
大多数皮肤利什曼病病例由热带利什曼原虫、大型利什曼原虫或婴儿利什曼原虫引起,主要分布在西亚、中亚、北非和地中海沿岸地区。在南美洲,巴西利什曼原虫复合体是主要病因。皮肤利什曼病的病灶虽然通常不致命,但会造成严重的社会心理影响。在许多流行地区,面部疤痕被视为耻辱的标志,影响患者的婚姻前景和社会地位。
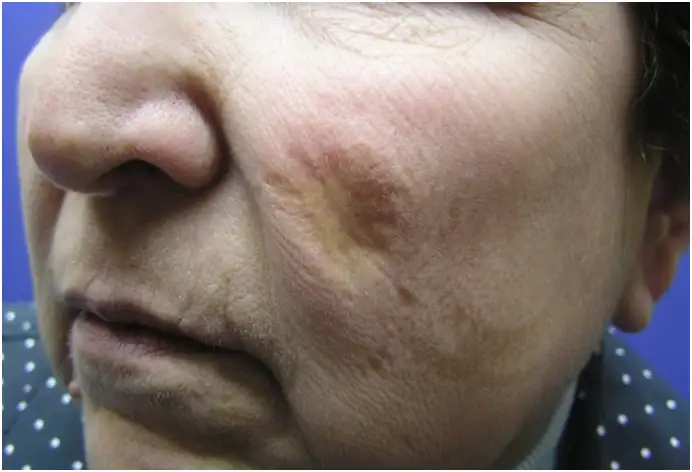
研究显示,面部皮肤利什曼病患者中抑郁和焦虑的发生率显著高于一般人群。对于女性患者而言,影响尤为严重,因为她们可能面临被社会排斥和无法结婚的风险。在阿富汗和叙利亚等保守社会,皮肤利什曼病被赋予了深刻的社会污名,被称为"可怕的面孔病"。利什曼病疤痕可能导致个人的隔离和排斥,对心理、社会和经济福祉造成重大改变。
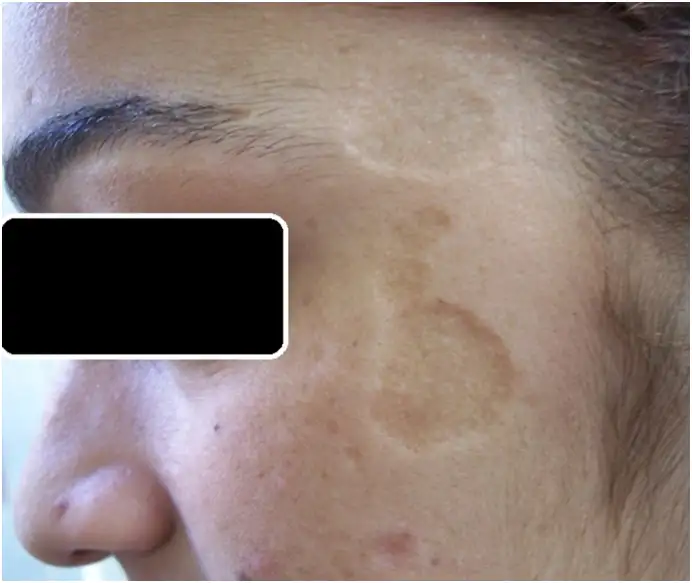
黏膜皮肤利什曼病主要由巴西利什曼原虫复合体的物种引起,分布在南美洲,尤其是巴西、秘鲁和玻利维亚。这种形式的疾病开始时与皮肤利什曼病相似,但寄生虫会通过血液或淋巴系统迁移到上呼吸道的黏膜组织。初始皮肤病灶可能愈合多年后,黏膜病变才出现。患者会出现鼻塞、鼻出血和面部疼痛,随着疾病进展,鼻中隔和腭部可能被破坏,导致鼻塌陷或穿孔。在严重病例中,嘴唇、咽喉和喉部也会受累,可能危及生命。
内脏利什曼病,又称黑热病,是三种类型中最致命的形式。它主要由杜氏利什曼原虫(南亚和东非)和婴儿利什曼原虫(地中海地区、中东和中亚)引起。寄生虫通过感染的巨噬细胞播散到脾脏、肝脏、骨髓和淋巴结,引起进行性脾脏肿大、肝脏肿大、贫血、白细胞减少和血小板减少。患者的脾脏可以肿大到占据大部分腹腔,触诊时质地坚硬。皮肤可能呈现深灰色或黑色,这是该病在印度被称为"黑热病"的原因之一。
未经治疗的内脏利什曼病几乎是致命的。患者通常在症状出现后两年内死于继发感染、出血或严重贫血。然而,即使接受治疗,死亡率仍可达百分之十,这主要与诊断延迟、营养不良和合并感染有关。在东非和南亚,内脏利什曼病是重要的公共卫生问题,特别是在贫困农村地区。印度比哈尔邦、孟加拉国和尼泊尔南部是世界上内脏利什曼病负担最重的地区,这三国占全球报告病例的百分之八十以上。
叙利亚的黑色遗产
二〇一一年,叙利亚危机爆发。在随后的内战中,数百万人流离失所,医疗系统崩溃,基础设施遭到严重破坏。这些条件为利什曼病的爆发创造了完美的土壤。根据世界卫生组织的数据,叙利亚的利什曼病病例从二〇一〇年的两万三千例激增至二〇一三年的四万一千例以上,而且这一数字很可能被低估。
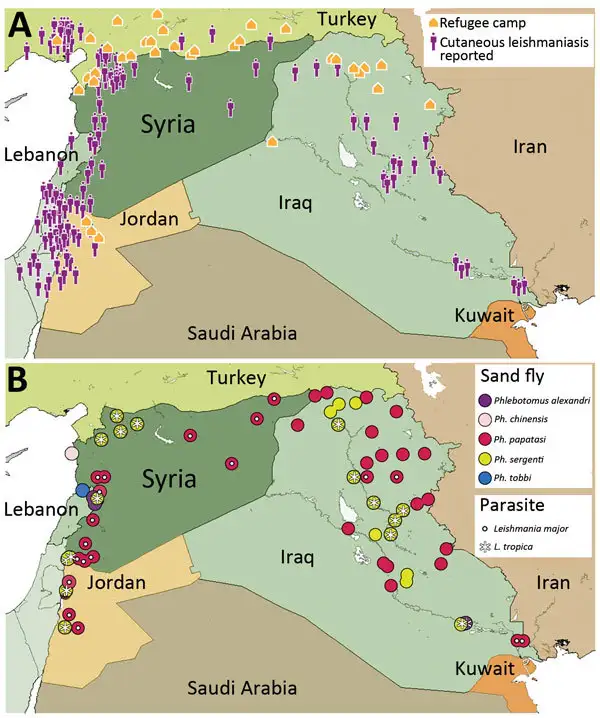
叙利亚原本就是皮肤利什曼病的流行区。在阿勒颇及周边地区,这种疾病被称为"阿勒颇疖"或"东方疮",有着数百年的流行历史。在正常情况下,公共卫生系统能够有效控制疾病的传播,但战争改变了一切。大规模的人口流离失所使人们暴露于白蛉叮咬的风险中。难民营通常缺乏有效的防护措施,蚊帐稀缺,环境卫生条件恶劣。白蛉的繁殖地——垃圾堆积处、废墟和动物栖息地——在战争区域大量增加。
研究人员对叙利亚的利什曼病爆发进行了深入分析。他们发现,病例的增加不仅发生在叙利亚境内,也影响到邻国。黎巴嫩、土耳其、约旦和伊拉克都报告了来自叙利亚难民或在这些国家工作后返回的叙利亚人的利什曼病病例。在黎巴嫩,皮肤利什曼病病例从二〇一〇年的六例增加到二〇一三年的一千零三十三例,这一剧增几乎完全归因于叙利亚难民。
分子流行病学研究揭示了叙利亚利什曼病爆发的病原体构成。大型利什曼原虫是主要的致病种,占总病例的大多数,但也有相当比例的病例由婴儿利什曼原虫引起。两种寄生虫在临床表现和药物敏感性上存在差异,这对治疗策略的选择有重要影响。婴儿利什曼原虫感染可能导致黏膜受累,需要更积极的治疗,而大型利什曼原虫感染通常局限于皮肤,对局部治疗的反应较好。
叙利亚的利什曼病爆发还揭示了战争对传染病监测和控制系统的破坏性影响。在冲突前,叙利亚有着相对完善的利什曼病监测网络,病例报告和治疗系统运转良好。战争期间,医疗设施被摧毁或废弃,医务人员逃离,药品供应链中断,疾病监测系统几乎完全瘫痪。许多患者无法获得诊断和治疗,只能任由疾病发展。对于皮肤利什曼病来说,这意味着毁容性疤痕的形成;对于内脏利什曼病来说,这意味着近乎确定的死亡。
针尖上的千年战争
治疗利什曼病的历史是一部人类与寄生虫之间不断升级的军备竞赛。五价锑剂,特别是葡萄糖酸锑钠,是治疗利什曼病的传统一线药物,已经使用了近一个世纪。锑剂的作用机制尚不完全清楚,但它似乎通过干扰寄生虫的能量代谢和抗氧化防御系统来杀死利什曼原虫。对于内脏利什曼病,标准疗程是每天静脉注射二十毫克/千克体重,持续二十八天;对于皮肤利什曼病,可以采用病变内注射或系统性治疗。
然而,锑剂治疗存在严重的问题。首先,副作用常见且可能严重,包括心脏毒性、胰腺炎、肝肾损害和肌肉关节疼痛。在某些情况下,患者因为无法耐受副作用而中断治疗。其次,在印度比哈尔邦,对锑剂的耐药性已成为一个严重的公共卫生问题。研究表明,该地区百分之六十以上的内脏利什曼病患者对锑剂治疗无反应,这迫使医疗工作者转向替代治疗方案。
两性霉素B是一种广谱抗真菌药物,后来发现对利什曼原虫也有效。它通过与寄生虫细胞膜中的麦角固醇结合,形成孔隙,导致细胞内容物泄漏和死亡。脂质体两性霉素B是治疗内脏利什曼病的首选药物,尤其适用于锑剂耐药病例。它比传统两性霉素B更安全,可以在短时间内给予大剂量治疗。然而,脂质体两性霉素B价格昂贵,在资源有限的流行地区往往难以获得。
米尔替福辛是一种口服的抗癌药物,后来被重新定位为抗利什曼病药物。它是第一种口服治疗内脏利什曼病的有效药物,对于印度次大陆的内脏利什曼病显示出良好的疗效。然而,米尔替福辛有致畸性,禁用于孕妇,且在东非的疗效不如印度。此外,关于米尔替福辛耐药性的担忧也日益增加,实验室研究表明利什曼原虫可以相对容易地发展出对这种药物的耐药性。
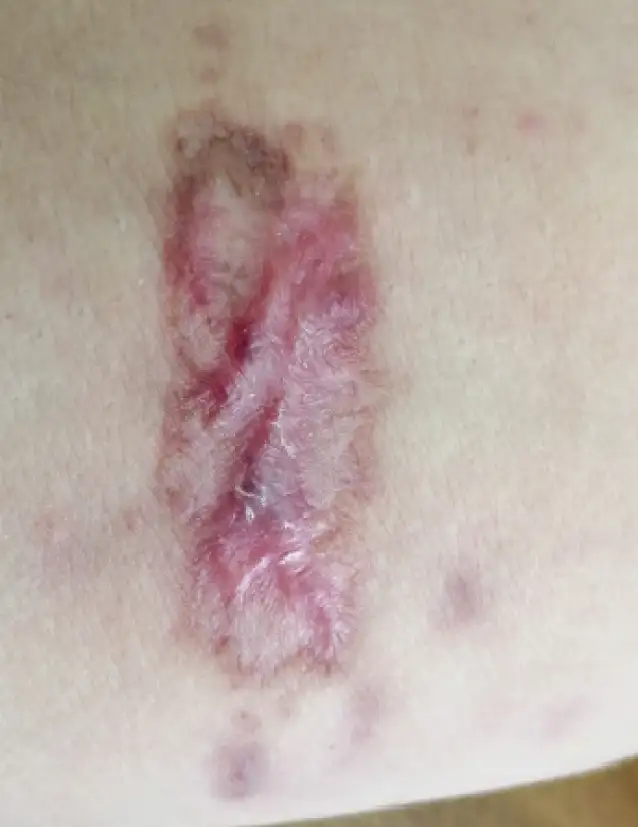
对于皮肤利什曼病,治疗方案取决于病变的数量、大小、部位和致病物种。局部治疗包括病变内锑剂注射、冷冻疗法、热疗和局部药物如巴龙霉素软膏。对于面部、关节附近或多发性病变,通常需要系统性治疗。值得注意的是,由巴西利什曼原虫复合体引起的皮肤利什曼病需要系统性治疗,因为有发展为黏膜疾病的风险。
耐药性的阴影
随着抗利什曼病药物的广泛使用,耐药性问题日益突出。在印度比哈尔邦,对五价锑剂的耐药性已经达到危机水平。研究表明,耐药机制涉及寄生虫对药物摄取的减少、药物外排的增加以及药物靶点的修饰。一种名为AQP1的水通道蛋白负责锑剂的摄入,该蛋白的表达下调与耐药性相关。另一方面,一种ATP结合盒转运蛋白MRPA的过表达导致药物从寄生虫细胞内外排。
对米尔替福辛的耐药性也在实验室中被诱导出来。耐药机制包括药物外排转运蛋白的上调、药物靶点——磷酸脂酶C和神经酰胺激酶——的突变以及细胞膜脂质成分的改变。虽然在临床环境中米尔替福辛耐药性尚未成为主要问题,但这些实验室发现敲响了警钟,提示不合理的药物使用可能迅速导致耐药性的出现。
两性霉素B的耐药性在临床上尚未成为重要问题,但已有实验室研究证明利什曼原虫可以发展出对两性霉素B的耐药性。耐药机制涉及麦角固醇生物合成途径的改变,特别是甾醇C24-甲基转移酶和Δ8-Δ7甾醇异构酶的突变,导致细胞膜中麦角固醇被其他甾醇替代,减少了两性霉素B的结合位点。
面对耐药性的威胁,研究人员正在积极寻找新的治疗策略。靶向寄生虫必需的蛋白激酶是一个有前景的方向。由于利什曼原虫的蛋白激酶与人类同源物存在结构和功能的差异,有可能开发出具有选择性的抑制剂。另一个有前景的靶点是寄生虫的能量代谢,特别是其独特的糖酵解途径和脂肪酸氧化。此外,针对寄生虫入侵和细胞内存活必需的毒力因子如GP63和脂磷酸糖的干预也可能提供新的治疗途径。
免疫系统的背叛
利什曼病的临床结局在很大程度上取决于宿主的免疫反应。在大多数皮肤利什曼病患者中,寄生虫被有效控制,病灶最终自愈。自愈过程依赖于强有力的T辅助细胞1型免疫反应,特征是产生干扰素-γ和肿瘤坏死因子-α。这些细胞因子激活巨噬细胞的杀菌活性,通过产生一氧化氮和其他活性氮中间体来杀死寄生虫。
然而,在某些个体中,免疫反应偏向T辅助细胞2型,特征是产生白细胞介素-4、白细胞介素-10和白细胞介素-13。这些细胞因子抑制巨噬细胞的杀菌活性,导致寄生虫的持续存在和疾病的慢性化。在内脏利什曼病患者中,这种免疫偏差尤为明显。研究表明,内脏利什曼病患者外周血中的干扰素-γ水平极低,而白细胞介素-10水平显著升高。这种免疫抑制状态不仅使寄生虫得以大量繁殖,还使患者容易发生继发感染。
利什曼原虫如何操纵宿主免疫反应使其向有利于自己的方向发展?研究表明,寄生虫通过多种机制实现这一目标。首先,无鞭毛体表面和分泌的分子如脂磷酸糖和GP63可以直接干扰巨噬细胞的信号转导。GP63能够切割宿主细胞的转录因子和信号分子,干扰核因子-κB和丝裂原活化蛋白激酶等关键信号通路的激活。其次,寄生虫通过诱导调节性T细胞的扩增和活化,增加白细胞介素-10的产生。第三,寄生虫可以干扰树突状细胞的成熟和功能,削弱向T细胞呈递抗原的能力。
值得注意的是,利什曼原虫感染后的免疫记忆存在显著差异。成功自愈的皮肤利什曼病患者通常获得持久的免疫力,很少再次感染。相反,治疗后康复的内脏利什曼病患者并不一定能获得稳固的免疫力,再次感染的情况时有发生。这种差异可能与不同形式疾病中免疫反应的性质和强度有关。
在流行地区,无症状感染是常见现象。研究表明,在利什曼病流行区,暴露于利什曼原虫的人群中只有一部分会发展为临床疾病,大多数感染者保持无症状。这些无症状携带者的免疫系统能够有效控制寄生虫的增殖,但他们可能成为传染源,维持疾病在社区中的传播。这一发现对于理解利什曼病的流行病学和制定控制策略具有重要意义。
白蛉的秘密生活
利什曼原虫与白蛉之间的关系不仅仅是简单的寄生。研究发现,寄生虫能够操纵白蛉的生理和行为,以增加传播的机会。感染的白蛉在吸血时更频繁地中断叮咬,增加了传播寄生虫到多个宿主的机会。此外,寄生虫通过分泌各种分子改变白蛉肠道的物理屏障,促进自己向前迁移。
控制白蛉是预防和控制利什曼病的重要策略。在室内栖息的白蛉物种可以通过杀虫剂残留喷洒来控制,这一策略在印度次大陆的内脏利什曼病消除计划中被广泛采用。个人防护措施包括使用蚊帐、驱虫剂和穿着覆盖皮肤的衣物。然而,在野外栖息的白蛉物种更难控制,这限制了传统媒介控制在某些地区的效果。
从实验室到田野
疫苗的开发是利什曼病研究的终极目标之一。鉴于自愈的皮肤利什曼病患者能够获得持久的免疫力,理论上应该可以开发出有效的疫苗。然而,尽管进行了数十年的研究,至今仍没有获准用于人类的利什曼病疫苗。
早期的研究集中在"利什曼化"——故意让易感人群感染皮肤利什曼病,以诱导保护性免疫。这种方法在伊朗和以色列等国家曾被广泛使用,接种部位通常选择隐蔽的身体部位以避免面部疤痕。虽然利什曼化能够提供持久的保护,但它也可能导致严重的皮肤病变,在某些个体中甚至可能发展为播散性疾病。因此,这种方法在现代已被放弃。
第一代疫苗候选物包括杀死的前鞭毛体全虫疫苗,通常与卡介苗或其他佐剂联合使用。虽然这些疫苗在某些临床试验中显示出一定的保护效果,但结果不一致,未能推进到许可阶段。第二代疫苗候选物包括重组蛋白疫苗和DNA疫苗,针对寄生虫的关键抗原如GP63、KMP-11和Leish-111f等。这些疫苗在动物模型中显示出良好的保护效果,但在人体试验中的结果尚不理想。
近年来,研究人员开始探索利用白蛉唾液蛋白作为疫苗组分。白蛉在叮咬时会注入含有各种生物活性分子的唾液,这些分子具有抗凝血、血管扩张和免疫调节功能。研究发现,预先暴露于白蛉唾液可以增强对利什曼原虫感染的抵抗力,这为开发针对媒介唾液的新型疫苗策略开辟了道路。
被遗忘的疾病
利什曼病是世界卫生组织认定的二十种被忽视热带病之一。被忽视热带病是一组主要影响世界上最贫困人口的疾病,它们虽然不像艾滋病、结核病和疟疾那样造成大量死亡,但其总体负担相当可观。被忽视热带病的共同特点是主要影响贫困社区、缺乏有效控制工具、研究和开发投入不足。
利什曼病的"被忽视"状态体现在多个方面。首先,它主要影响发展中国家的贫困人口,这些人群缺乏政治声音和经济资源来推动研究和控制工作。其次,与艾滋病和疟疾相比,利什曼病的研究资金投入严重不足。第三,尽管利什曼病造成显著的发病率和死亡率,但其全球负担仍被低估,因为许多病例未被发现或报告。
世界卫生组织于二〇〇七年建立了被忽视热带病部门,将利什曼病纳入全球公共卫生议程。此后,利什曼病的控制工作取得了一定进展,包括药物捐赠计划、诊断工具的改进和消除计划的实施。在印度次大陆,各国政府承诺消除内脏利什曼病这一公共卫生问题,虽然这一目标尚未完全实现,但病例数量已显著下降。
然而,利什曼病控制仍面临严峻挑战。气候变化可能改变白蛉和利什曼原虫的地理分布,使新的地区面临风险。人口流动、城市化、战争和社会动荡增加了疾病传播的风险。诊断工具在许多流行地区仍然缺乏,治疗药物昂贵或有严重副作用。最重要的是,消除利什曼病需要跨部门合作,包括改善住房条件、加强卫生系统、消除贫困和促进社会经济发展。
永恒的博弈
从伊本·西纳在波斯宫廷中观察的神秘溃疡,到现代叙利亚战争中的大规模爆发,利什曼病与人类的纠葛已跨越千年。这种寄生虫以其惊人的适应能力,在白蛉和哺乳动物两种截然不同的宿主之间穿梭,在人体免疫系统的核心建立起自己的王国。它能够忍受吞噬溶酶体的致命环境,操纵宿主的免疫反应,抵抗药物的治疗,展现出令人惊叹的生存智慧。
然而,人类并非被动地接受利什曼病的侵袭。从利什曼和多诺万在显微镜下首次发现寄生虫,到现代科学家揭示其复杂的分子生物学,人类对利什曼原虫的理解不断深入。新的诊断工具、治疗药物和疫苗候选物正在研发中,流行病学监测和控制策略不断完善。在印度次大陆,内脏利什曼病的消除已从梦想变为可触及的目标。
利什曼病的故事是人类与病原体之间永恒博弈的缩影。在这场博弈中,人类运用科学的力量不断推进,而寄生虫则以其惊人的变异和适应能力进行反击。最终,战胜利什曼病需要的不仅是药物和疫苗,更是对贫困、不平等和社会动荡这些根本原因的解决。只有当每一个生活在这片土地上的人都能获得基本的卫生保健、清洁的居住环境和足够的营养,这位沙漠新娘的诅咒之吻才会真正成为历史的记忆。