四千年前的恐惧
公元前1930年的某个黄昏,在美索不达米亚平原的埃什努纳城邦,一名苏美尔书记官在湿润的泥板上刻下了一段楔形文字。这段文字被后世称为《埃什努纳法典》,是人类历史上最早成文的法律之一。在第五十六条和第五十七条中,法典记载了一条奇特的规则:如果一只狗变得疯狂并咬了人,导致那人死亡,狗的主人必须支付赔偿。这是人类历史上关于狂犬病的最早文字记录,距今已有近四千年。
苏美尔人对这种疾病的理解令人惊讶地精准。他们不仅认识到疯狂与咬伤之间的因果关联,还意识到存在着某种致命的东西可以通过唾液传播。出土于尼普尔遗址的阿卡德语咒语文本更加直白:祭司们会在患者身上朗读一段对话,内容是医神马杜克向其父恩基请求救治方法。而恩基的回答充满绝望——如果患者已经开始出现症状,死亡将不可避免。这是人类历史上最早对狂犬病"发病即死"这一残酷现实的文字记载。
古巴比伦人将狂犬病与月亮联系起来,他们相信月食发生时,狗更容易发疯。在女神古拉的雕像中,这位掌管医药的神祇脚边总是蹲着一只狗——这只狗既是守护者,也是危险的来源。这种矛盾的形象完美地捕捉了人类与犬类之间复杂的关系:我们最早的伙伴,同时也是一种恐怖疾病的传播者。
亚里士多德在《动物史》中写道:“疯狗会让被咬的人也发疯。“希波克拉底描述了患者对水的极度恐惧。老普林尼在他的《自然史》中记载了数十种"疗法”,从烧灼伤口到喂食狗毛——“以毒攻毒"这一成语正是由此而来,而英文中"hair of the dog”(狗毛)这一表达至今仍在使用,尽管它的含义已经从治疗狂犬病变成了治疗宿醉。

古巴比伦女神古拉的雕像,脚边蹲着一只狗。这是人类最早将狗与医术联系起来的形象之一,同时也暗示了狗既是保护者也是疾病来源的双重身份。
子弹形状的杀手
在电子显微镜下,狂犬病毒呈现出一种独特的子弹形状。病毒颗粒长约180纳米,直径约75纳米,一端圆润或呈锥形,另一端则是平坦的基底。这种独特的形态使它成为病毒世界中最容易辨认的成员之一。这种子弹形状并非偶然——它反映了狂犬病毒作为弹状病毒科成员的独特构造。
狂犬病毒的基因组是一条单股负链RNA,全长约12000个核苷酸。这条RNA链条上排列着五个基因,依次编码五种蛋白质:核蛋白(N)、磷蛋白(P)、基质蛋白(M)、糖蛋白(G)和大蛋白(L)。这五种蛋白质各司其职,共同完成一场针对神经系统的精密入侵。
糖蛋白是狂犬病毒最关键的武器。它像无数根尖刺一样覆盖在病毒颗粒的表面,形成一种独特的"拉链"状结构。2022年,科学家利用冷冻电镜技术解析出了糖蛋白三聚体在融合前构象的原子级结构,揭示了它如何像一把精密的钥匙一样插入宿主细胞的受体。糖蛋白由融合结构域、血小板同源结构域和中央结构域组成,这三个部分通过复杂的链间连接协同工作,使病毒能够精准地识别并侵入神经细胞。
核蛋白则负责保护那条珍贵的RNA链条。在病毒颗粒内部,核蛋白紧紧包裹着RNA,形成一种螺旋对称的核衣壳结构。这种结构不仅保护病毒基因组免受降解,还为RNA复制提供了平台。磷蛋白充当分子伴侣的角色,连接着核蛋白和大蛋白——后者是一种RNA依赖的RNA聚合酶,负责转录和复制病毒基因组。
基质蛋白位于病毒包膜的内侧,像一个建筑师的蓝图,指导着病毒颗粒的组装和出芽。它与其他结构蛋白相互作用,确保每一个新生的病毒颗粒都拥有完整的子弹形状。当病毒在细胞内完成复制后,基质蛋白会帮助新组装的核衣壳迁移到细胞膜附近,在那里与糖蛋白相遇,最终以出芽的方式释放出新的病毒颗粒。
潜伏在神经纤维中的幽灵
狂犬病毒最令人恐惧的特性是它感染神经细胞的方式。当一只携带病毒的动物咬伤人类时,病毒随着唾液进入伤口。但它不会立即进入血液循环——相反,它选择了一条更加隐蔽也更加致命的路径:沿着周围神经纤维逆行而上,直奔大脑。
病毒进入伤口后,首先会在局部肌肉组织中复制数天甚至数周。这个阶段是患者最后的希望——如果能在病毒进入神经之前接种疫苗和免疫球蛋白,死亡是可以避免的。一旦病毒进入神经末梢,它就开始了一场沿着轴突逆流而上的旅程。
狂犬病毒利用了宿主细胞自己的运输系统来完成这场入侵。神经细胞的轴突中存在着一种称为动力蛋白的分子马达,它负责沿着微管运输各种物质。狂犬病毒巧妙地劫持了这个系统,将自己伪装成需要运输的"货物”,以每天约50到100毫米的速度向中枢神经系统移动。
2014年的一项研究揭示了这一过程的分子机制。狂犬病毒的糖蛋白能够结合神经细胞表面的p75神经营养因子受体——这个受体正常情况下是用来接收神经生长因子的。病毒通过与这个受体结合,激活了一系列细胞内信号通路,使动力蛋白马达系统加速运转。病毒就这样搭上了一趟开往大脑的快车。
病毒穿越神经肌接头进入运动神经纤维,然后沿着脊髓后根神经节进入脊髓,最终抵达脑干。一旦进入中枢神经系统,病毒开始在大脑的各个区域疯狂复制:海马体、大脑皮层、小脑、脑干——没有任何一个区域能够幸免。
狂犬病毒拥有一种可怕的"隐形"能力。在野生型毒株感染中,病毒会主动抑制宿主的先天免疫反应。它的磷蛋白能够干扰干扰素的诱导,阻断下游信号通路的激活。同时,病毒还会保持血脑屏障的完整性,阻止免疫细胞进入中枢神经系统。这意味着患者的免疫系统在病毒最疯狂复制的大脑中几乎是瞎子——它根本不知道那里正在发生什么。
病毒的这种免疫逃逸策略造成了两个悲剧性的后果。第一,患者的大脑被病毒大规模摧毁,而免疫系统却无能为力。第二,当病毒最终从唾液腺释放时,患者已经失去了自我保护的能力,变成了一个传播病毒的工具——这正是狂犬病毒进化的终极目的。
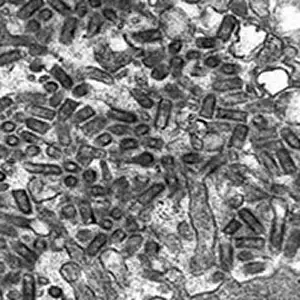
这张电子显微镜照片展示了一只狂犬狐狸唾液腺中的病毒颗粒。唾液腺腔隙中充满了子弹状的病毒颗粒,它们将随着唾液被注射到下一个受害者体内。这是狂犬病毒传播链中最关键的一环。
恐水的死亡之舞
狂犬病的临床症状分为两种类型:狂躁型和麻痹型。狂躁型占病例的约80%,也是人们印象中"疯狗病"的典型表现。患者会出现极度的躁动不安、攻击行为、幻觉和癫痫发作。最典型的症状是恐水症——患者看到水、听到水声,甚至只是想到水,就会引发咽喉部剧烈的痉挛性收缩。
恐水症的机制深藏在脑干的神经回路中。狂犬病毒特别嗜好感染脑干的运动神经元,尤其是控制吞咽和呼吸的神经核团。当患者试图吞咽时,控制咽喉肌肉的神经元会发出混乱的信号,导致剧烈的痉挛性收缩。这种痉挛如此痛苦,以至于患者会对任何可能触发吞咽反射的东西产生极度的恐惧——水首当其冲。
一个经典的临床描述是这样的:患者口渴难耐,端起水杯送到嘴边,但就在水即将触及嘴唇的那一刻,剧烈的痉挛猛烈收缩了他的喉咙。水杯摔落在地,患者痛苦地喘息着,眼中充满恐惧。他知道水能够解渴,但他的大脑已经将水与无法忍受的痛苦绑在了一起。这是人类已知的最残酷的生理矛盾之一:极度口渴的人对水产生了最深的恐惧。
恐风症是另一个典型症状。患者对气流特别敏感,即使是一阵微风掠过面部,也会引发类似的咽喉痉挛。有些患者甚至对强光、噪音或触摸产生同样的反应。这些症状反映了病毒对脑干感觉处理区域的广泛破坏。
麻痹型狂犬病约占病例的20%。患者的症状更加隐蔽:从被咬伤的肢体开始,逐渐发展为上行性瘫痪。这种类型容易被误诊为吉兰-巴雷综合征或其他神经系统疾病。但无论如何,两种类型的结局都是一样的——死亡。
狂犬病的一个奇特之处是它对神经元结构破坏的轻微程度。电子显微镜研究显示,即使是被病毒严重感染的神经元,其细胞结构仍然保持相对完整。病毒似乎不是通过直接摧毁神经元来杀死患者,而是通过干扰神经递质的释放和信号传导来实施致命打击。
2024年的一项研究揭示了一种新的机制:狂犬病毒感染会导致神经元发生焦亡(pyroptosis)——一种程序性细胞死亡形式。病毒感染激活了Gasdermin D蛋白,这种蛋白会在细胞膜上打孔,导致细胞死亡和炎症反应。这个过程可能解释了为什么患者的神经系统会逐渐崩溃。
从症状出现到死亡,通常只有几天到两周的时间。患者会在意识清醒的状态下逐渐失去对身体的控制,最终陷入昏迷和呼吸衰竭。整个过程极其痛苦,而且患者往往全程保持清醒,能够感知到自己正在死去。医学文献中记载了太多这样的病例:患者用最后的力气向医生求救,但医生们只能眼睁睁地看着他们死去。
内基小体:死亡的证据
1903年,意大利病理学家阿德尔基·内基在研究狂犬病患者的脑组织时,发现了一种奇特的结构。在感染神经元的细胞质中,存在着一些圆形或卵圆形的嗜酸性包涵体,大小约2到10微米。这些结构后来被称为"内基小体",成为诊断狂犬病的金标准。
内基小体本质上是病毒的"工厂"。在这里,病毒的核衣壳物质大量聚集,正在进行活跃的复制。电子显微镜下的内基小体呈现出一种迷人的内部结构:中心是致密的病毒核衣壳颗粒,周围环绕着各种细胞器和病毒颗粒。有些内基小体中可以看到正在从细胞膜出芽的病毒颗粒。
内基小体最常出现在海马体的锥体细胞和小脑的浦肯野细胞中。病理学家在尸检时会特别检查这些区域。用塞勒染色法或曼氏染色法处理脑组织切片,内基小体会呈现出鲜艳的红色或品红色,与蓝色的细胞核形成鲜明对比。
然而,内基小体并非在所有狂犬病例中都能找到。研究显示,只有约50%到80%的病例存在典型的内基小体。这意味着诊断狂犬病不能仅仅依靠寻找这些结构。现代诊断方法已经转向更敏感的技术:直接荧光抗体法检测病毒抗原、逆转录聚合酶链反应检测病毒RNA、以及病毒分离培养。
直接荧光抗体法是生前诊断最常用的方法。医生会从患者颈后部取一小块皮肤活检样本,用荧光标记的抗狂犬病毒抗体染色。如果存在病毒感染,在荧光显微镜下会看到特异性的苹果绿色荧光。这种方法的敏感性和特异性都很高,但需要在专门的实验室进行。
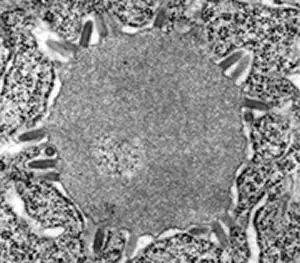
这张电子显微镜照片展示了内基小体形成的早期阶段。病毒核衣壳物质开始在神经元细胞质中聚集,一些病毒颗粒正在从周围的细胞膜出芽。当这个结构长大到一定程度,就可以在光学显微镜下看到典型的内基小体。
巴斯德的赌局
1885年7月6日的巴黎,一个九岁的男孩站在路易·巴斯德的实验室里。约瑟夫·迈斯特来自阿尔萨斯地区,两天前被一只疯狗咬了十四次。他的母亲听说巴黎有一位科学家正在研究狂犬病疫苗,便带着儿子千里迢迢赶来求助。
巴斯德当时正处于他科学生涯的巅峰。他已经成功开发了鸡蛋乱疫苗和炭疽疫苗,证明了微生物致病理论的正确性。但狂犬病疫苗是另一回事——它从未在人类身上试验过。
巴斯德的团队——尤其是他的助手埃米尔·鲁——已经花了五年时间研究狂犬病。他们发现,将感染狂犬病的兔子脊髓在干燥空气中暴露不同天数,可以使病毒的毒力逐渐减弱。暴露十五天的脊髓几乎完全失去了致病能力,但仍能激发保护性免疫。
当约瑟夫·迈斯特到达时,巴斯德面临着一个艰难的决定。理论上,他的疫苗在狗和兔子身上效果很好,但人类呢?没有人知道。埃米尔·鲁坚决反对在人体上试验——他认为风险太大。但另一位医生雅克-约瑟夫·格朗谢说服了巴斯德:这个男孩如果不治疗必死无疑,疫苗是他唯一的希望。
从7月6日晚上8点开始,格朗谢医生在巴斯德的监督下,给约瑟夫注射了第一针疫苗。这是来自一只死于狂犬病的兔子的脊髓,已经干燥了十五天,病毒毒力已经大大减弱。在接下来的十天里,约瑟夫接受了总共十三针疫苗,每一针使用的脊髓干燥时间都比前一针短,意味着病毒毒力更强。
这是一场与时间的赛跑。狂犬病毒的潜伏期从几周到几个月不等,而约瑟夫被咬已经过了两天。疫苗必须在他发病之前建立起足够的免疫力。巴斯德每天焦急地观察着这个男孩,等待着任何发病的迹象。
一个月过去了。约瑟夫·迈斯特没有发病。他活了下来。
消息很快传遍了世界。患者从欧洲各地、甚至从遥远的俄罗斯蜂拥而至,希望得到这种神奇的疫苗。巴斯德不得不在他的实验室附近建立一个专门的疫苗接种中心来应对蜂拥而来的人群。到1886年底,已经有约350人接受了疫苗接种。

约瑟夫·迈斯特在1885年的照片,当时他被路易·巴斯德的狂犬病疫苗拯救,成为历史上第一个接受狂犬病疫苗的人类。
然而,巴斯德的疫苗并非没有争议。首先,他本人并不是医生,法律上无权进行医疗操作——这由格朗谢医生代劳。其次,疫苗中使用的活病毒虽然经过了减毒,但仍然是活的,理论上仍有引起疾病的风险。第三,后来发现并非所有被疯狗咬伤的人都会患上狂犬病——即使不接种疫苗,许多人也不会发病。这意味着一些所谓的"成功案例"可能根本不会发展成狂犬病。
尽管如此,巴斯德的疫苗是医学史上的里程碑。它是第一种在暴露后能够预防疾病的疫苗,开创了暴露后预防的概念。更重要的是,它证明了微生物致病理论可以转化为实际的医学干预——这一理念彻底改变了现代医学。
约瑟夫·迈斯特后来成为了巴斯德研究所的看门人,在那里工作了数十年。1940年,德国纳粹占领巴黎。据说迈斯特选择自杀而不是让纳粹进入巴斯德的陵墓。这个故事的真实性有争议,但它已成为狂犬病疫苗史上一个动人的注脚。
密尔沃基协议:死亡边缘的奇迹
2004年10月,威斯康星州的一个小镇上,一个十五岁的女孩躺在医院的病床上。珍娜·吉斯三周前被一只蝙蝠咬伤,没有接种疫苗。现在,她出现了典型的狂犬病症状:恐水、躁动、发烧。医生们告诉她的父母,她会在几天内死去。
狂犬病发病后的死亡率被认为是100%。在人类历史上,只有极少数人在出现症状后存活下来,而且大多数都留下了严重的神经系统后遗症。但当珍娜的病例被送到罗德尼·威洛比医生面前时,这位儿科传染病专家决定尝试一些不同的东西。
威洛比医生的思路是这样的:狂犬病毒并不是直接杀死神经元,而是干扰神经系统的功能。如果我们能让患者的大脑"休眠"——降低其代谢活动和电活动——或许能让免疫系统有时间清除病毒。与此同时,使用抗病毒药物抑制病毒复制,也许能为患者赢得生存的机会。
这个方案后来被称为"密尔沃基协议"。珍娜被置于药物诱导的昏迷状态,使用氯胺酮和咪达唑仑抑制大脑活动。同时,她接受了利巴韦林和金刚烷胺两种抗病毒药物的治疗。医疗团队密切监测她的脑电图和病毒载量,在适当的时候逐渐减少镇静剂的剂量。
七十六天后,珍娜醒了过来。她能够说话、走路、甚至回到学校。她是历史上第一个在没有接种疫苗的情况下从狂犬病中康复的人。
这个消息震惊了医学界。几十年来被认为不可治愈的疾病,似乎出现了突破。密尔沃基协议被迅速推广到世界各地,人们希望它能够拯救更多的狂犬病患者。
然而,随后的结果令人失望。在接下来的十几年里,密尔沃基协议被用于治疗数十名狂犬病患者,但绝大多数仍然死亡。只有极少数幸存者,而且都留下了严重的神经系统后遗症。2025年发表的一项综述研究得出结论:密尔沃基协议对大多数狂犬病患者无效,不应作为常规治疗方案。
为什么珍娜能够存活?科学家们提出了几种可能的解释。首先,咬伤她的是一只蝙蝠,而蝙蝠携带的狂犬病毒毒力可能比狗携带的病毒低。其次,她被咬伤的位置在手指,距离大脑较远,病毒需要更长的传播时间。第三,她的免疫系统可能对病毒产生了某种独特的反应。
珍娜的案例仍然是一个医学奇迹,但它也提醒我们:狂犬病一旦发病,死亡仍然是压倒性的结局。预防,而不是治疗,才是对抗这种疾病的唯一有效策略。
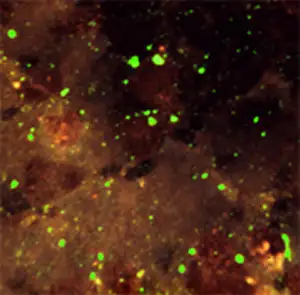
直接免疫荧光法诊断狂犬病。这张图片来自1965年一只狂犬狐狸的脑干印片,使用荧光标记的抗狂犬病抗体染色。这种方法自1958年首次应用以来,至今仍是狂犬病诊断的金标准。
全球战争:零死亡的目标
世界卫生组织估计,每年全球有约59000人死于狂犬病。这个数字可能被严重低估——由于报告系统不完善,实际死亡人数可能是官方统计的三倍。95%以上的死亡发生在非洲和亚洲,尤其是农村贫困地区。
印度承担了全球狂犬病死亡的约35%。这个国家拥有约3000万只流浪狗,每年有约2000万人被狗咬伤。尽管印度是世界上最大的狂犬病疫苗生产国,但大多数疫苗被出口到发达国家,本国人口却难以获得及时的暴露后预防。
非洲的情况更加严峻。在撒哈拉以南非洲,狂犬病死亡的真实规模几乎无法统计。许多患者在被咬后从未寻求医疗帮助,即使寻求了帮助,当地的医疗机构也可能没有疫苗或免疫球蛋白。一位肯尼亚医生描述了这样一种场景:一个八岁的男孩被疯狗咬伤,母亲抱着他走了三十公里山路来到诊所,却发现诊所的冰箱坏了,所有疫苗都失效了。那个男孩在一周后死去。
狂犬病的经济负担是惊人的。全球每年因狂犬病造成的经济损失估计超过86亿美元,包括暴露后预防的费用、牲畜损失和劳动力丧失。对于贫困家庭来说,一次暴露后预防的费用可能相当于几个月的收入。
然而,消除狂犬病的目标是可实现的。2015年,世界卫生组织、世界动物卫生组织、联合国粮农组织和全球狂犬病控制联盟联合发起了"零死亡2030"倡议,目标是在2030年消除犬介导的人类狂犬病死亡。
这个目标的关键策略是大规模犬类疫苗接种。研究显示,当一个地区70%以上的犬只接种了狂犬病疫苗,病毒的传播链就会被打断。墨西哥在2019年成为第一个被世界卫生组织确认消除犬介导狂犬病的国家,证明了这一策略的可行性。
拉丁美洲的经验尤其值得借鉴。在1980年代,该地区每年有数百人死于狂犬病。通过大规模犬类疫苗接种和改善暴露后预防的可及性,死亡人数在几十年内下降了超过95%。这证明,即使在资源有限的环境中,狂犬病也是可以被击败的。
中国的狂犬病挑战
中国是狂犬病流行的重要国家。在1950年代,每年报告的狂犬病死亡人数超过1000人。经过大规模的犬类管理和疫苗接种运动,死亡人数在1990年代下降到每年约200人。然而,随着宠物犬数量的激增和农村地区免疫覆盖率的下降,狂犬病死亡人数在2000年代初期再次上升,2007年达到3300人的峰值。
近年来,中国的狂犬病防控取得了显著进展。2022年,全国报告的狂犬病死亡人数已下降到约100人。但挑战仍然存在:农村地区的犬类疫苗接种率仍然偏低,暴露后预防的费用对许多家庭来说仍然是一个负担,而且关于狂犬病的错误认识在民间仍然广泛流传。
一个常见的误解是"十日观察法"——被狗咬伤后,观察狗十天,如果狗没有发病,人就不会得狂犬病。这种方法在理论上是正确的,因为狗只有在发病前几天才会通过唾液排毒。然而,在实践中,等待十天可能会导致错过最佳的疫苗接种时机。正确的做法是立即开始暴露后预防,同时观察狗的情况——如果十天后狗仍然健康,可以停止后续的疫苗接种。
另一个挑战是蝙蝠传播的狂犬病。在中国,蝙蝠相关的狂犬病病例虽然罕见,但几乎总是致命的,因为蝙蝠咬伤往往不被察觉或被忽视。2002年至2018年间,中国报告了至少七例蝙蝠相关的人类狂犬病病例,所有患者都在发病后死亡。
疫苗的进化
自从巴斯德开发出第一种狂犬病疫苗以来,狂犬病疫苗技术已经经历了多次革新。巴斯德最初使用的是神经组织疫苗——将感染狂犬病的动物脑组织干燥处理后制成。这种疫苗有效但存在严重问题:它含有髓磷脂,可能引发严重的神经并发症,如急性播散性脑脊髓炎。
20世纪中叶,科学家开发了禽胚疫苗,使用感染狂犬病的鸭胚或鸡胚制作。这种疫苗减少了神经并发症的风险,但仍然需要多次注射,而且局部反应常见。
1950年代, Wiktor和Koprowski开发了第一种细胞培养疫苗——人二倍体细胞疫苗。这种疫苗使用人胚肺成纤维细胞培养病毒,然后灭活制成。它是目前安全性最高、免疫原性最强的狂犬病疫苗,但成本也最高,限制了在发展中国家的使用。
后来开发的纯化鸡胚细胞疫苗和非洲绿猴肾细胞疫苗提供了更加经济的选择,同时保持了良好的安全性和有效性。这些疫苗已经成为世界大多数国家的标准选择。
中国开发的vero细胞疫苗使用非洲绿猴肾上皮细胞系,成本较低,产量较高,已经成为中国使用最广泛的狂犬病疫苗。近年来,中国还批准了人二倍体细胞疫苗和地鼠肾细胞疫苗,为不同需求提供了多种选择。
暴露后预防的标准方案包括两部分:疫苗和免疫球蛋白。疫苗刺激机体产生主动免疫,但这需要一周左右的时间才能产生足够的抗体。免疫球蛋白提供即时的被动免疫,在疫苗发挥作用之前中和病毒。
世界卫生组织推荐的简化方案是"2-1-1"方案:第0天在两个部位各注射一剂疫苗,第7天和第21天各注射一剂。另一种方案是在第0、3、7、14天各注射一剂。两种方案都被证明有效。
免疫球蛋白的使用需要特别注意。它应该尽可能多地注射到伤口周围,以中和局部的病毒。如果伤口位置不适合注射(如手指或脚趾),剩余的免疫球蛋白可以注射到远离疫苗注射部位的肌肉中。免疫球蛋白供应短缺是全球性问题,特别是在狂犬病高发的发展中国家。
未解之谜
尽管我们对狂犬病的认识已经大大深化,许多问题仍然没有答案。
为什么狂犬病的潜伏期如此多变?大多数病例在被咬后一到三个月发病,但也有短至几天、长至几年的案例。1977年报告的一例狂犬病患者,声称自己是在六年前被咬伤的。影响潜伏期的因素包括咬伤位置(距离大脑越近,潜伏期越短)、咬伤严重程度、病毒载量、以及宿主的免疫状态。但这些因素无法完全解释潜伏期的巨大差异。
为什么狂犬病一旦发病就无法治愈?这是狂犬病与其他病毒性脑炎最大的不同。单纯疱疹病毒性脑炎可以用阿昔洛韦治疗,西尼罗病毒性脑炎也有康复的案例。但狂犬病发病后几乎100%死亡。一种解释是病毒在症状出现之前已经广泛扩散到中枢神经系统,而且通过保持血脑屏障完整性和抑制免疫反应来逃避免疫监视。另一种解释是病毒造成的神经功能紊乱是不可逆的,即使病毒被清除,神经系统也无法恢复正常。
是否有可能开发出有效的抗病毒药物?目前没有针对狂犬病毒的特效抗病毒药物。利巴韦林在体外显示了一定的活性,但在临床应用中效果不佳。一些新开发的抗病毒药物,如法匹拉韦,在动物模型中显示出希望,但距离临床应用还有很长的路要走。
狂犬病毒的天然宿主是什么?这是一个出人意料难以回答的问题。虽然狗是狂犬病传播给人类的主要媒介,但狗并不是狂犬病毒的天然宿主——病毒在不同物种之间传播时会经历不同的进化压力。蝙蝠被认为是许多狂犬病毒变种的天然储存宿主,但具体哪些蝙蝠物种以及病毒如何在蝙蝠种群中维持传播,仍然不清楚。
结语:人类最古老的敌人
狂犬病是人类历史上最古老的疾病之一。在四千年前美索不达米亚的泥板上,我们的祖先就已经记录下了这种疾病的恐怖。从那时起,人类一直在与这个子弹形状的杀手进行着殊死的搏斗。
我们取得了巨大的进步。巴斯德的疫苗拯救了数百万人的生命。暴露后预防使得被咬伤的人们不再注定死亡。犬类疫苗接种运动在某些地区消除了狂犬病的威胁。我们比历史上任何时候都更接近于击败这个古老的敌人。
然而,狂犬病仍然存在。它潜伏在世界的角落,等待着那些没有保护的人们。每年仍有近六万人死于这种疾病,其中大多数是贫困地区的儿童。对于他们来说,巴斯德一个多世纪前发明的疫苗仍然是遥不可及的奢侈品。
狂犬病是人类医学的一个独特悖论:它是最致命的传染病之一,同时又是最可预防的疾病之一。我们拥有阻止每一例死亡所需的所有工具——疫苗、免疫球蛋白、知识。缺少的是将这些工具送到每一个需要它们的人手中的决心和资源。
四千年前,苏美尔祭司在患者身上朗读咒语,乞求神灵拯救他们。今天,我们有了疫苗。问题不再是"我们能做什么",而是"我们愿不愿意做"。2030年零死亡的目标是否能够实现,取决于这个问题的答案。
参考资料
- World Health Organization. Rabies Fact Sheet. 2024.
- Nel LH, Markotter W. New and emerging lyssaviruses. Current Opinion in Virology. 2024.
- Fooks AR, et al. Current status of rabies and prospects for elimination. Lancet. 2014;384(9951):1389-1399.
- Pasteur Institute. The history of the first rabies vaccination in 1885. 2023.
- Willoughby RE Jr, et al. Survival after treatment of rabies with induction of coma. New England Journal of Medicine. 2005;352(24):2508-2514.
- Jackson AC. Current and future approaches to the therapy of human rabies. Antiviral Research. 2013;99(1):61-67.
- Hampson K, et al. Estimating the global burden of endemic canine rabies. PLOS Neglected Tropical Diseases. 2015;9(4):e0003709.
- WHO. Zero by 30: The Global Strategic Plan. 2018.
- Schnell MJ, et al. The cell biology of rabies virus: using stealth to reach the brain. Nature Reviews Microbiology. 2010;8(1):51-61.
- Callaway E. Engineered rabies virus illuminates neural circuitry. The Scientist. 2024.
- Davis BM, et al. Everything you always wanted to know about rabies virus (but were afraid to ask). Annual Review of Virology. 2015;2:451-471.
- Mistry AM, et al. Rabies virus glycoprotein: Structure, function, and antivirals. Heliyon. 2025.
- CDC. Rabies Post-exposure Prophylaxis Guidance. 2025.
- Lancet. Demise of the Milwaukee Protocol for Rabies. 2025.