一九七七年,日本九州大学医学院的血液科病房里,高月清教授面对着一系列令他困惑不已的病例。这些患者来自九州南部和冲绳地区,他们共同呈现出一种前所未见的T细胞白血病——异常淋巴细胞在血液中疯狂增殖,皮肤布满结节和斑块,血钙水平高得离奇,而且在确诊后往往只能存活几个月。高月清将这种疾病命名为"成人T细胞白血病",但他无法解释为什么这种疾病会在特定地理区域集中爆发。
三年后,大洋彼岸的美国国立癌症研究所,罗伯特·加洛博士的实验室里,一场改变人类病毒学历史的发现正在酝酿。加洛团队从一名黑人男性T细胞淋巴瘤患者的血液中分离出一种前所未知的逆转录病毒。这是人类历史上发现的第一种能够致癌的逆转录病毒——人类T淋巴细胞白血病病毒一号,简称HTLV-1。这一发现不仅填补了人类病毒学的一项空白,更揭开了一段跨越千年的病毒与人类博弈史。
HTLV-1的发现绝非偶然。早在一九七〇年代初期,科学家们就怀疑某些癌症可能由病毒引起。一九七六年,两名美国科学家毕晓普和瓦缪斯因发现逆转录病毒致癌基因而获得诺贝尔奖,他们的研究揭示了病毒如何将自身的致癌基因整合到宿主细胞基因组中。加洛团队正是在这一理论指导下,坚持不懈地寻找人类致癌逆转录病毒。他们从培养的T细胞中观察到一种神秘的颗粒,这种颗粒具有逆转录酶活性,能够将RNA基因组逆转录为DNA并整合到宿主细胞染色体中。
与此同时,日本的研究者们也在独立追踪着同一种病毒。一九八一年,日本京都大学的日沼赖夫团队从一名成人T细胞白血病患者的细胞系中分离出一种逆转录病毒,他们将其命名为ATLV。很快,国际科学界确认加洛和日沼发现的是同一种病毒,统一命名为HTLV-1。这一年,距离人类首次发现逆转录病毒只过去了不到二十年,而HTLV-1成为第一个被证实能够导致人类癌症的逆转录病毒。
HTLV-1的传播方式与它的近亲HIV截然不同。虽然两者都是逆转录病毒,都感染CD4阳性T细胞,但HTLV-1的传播效率远低于HIV。主要传播途径有三种:母婴传播、性传播和血液传播。其中,母婴传播是最主要的途径,通过母乳喂养实现。研究表明,如果HTLV-1阳性母亲进行长期母乳喂养,约百分之十到二十五的婴儿会被感染。这种传播模式解释了为什么HTLV-1感染呈现明显的家族聚集性——在流行地区,往往整个家族几代人都是携带者。
病毒进入人体后,并不会像HIV那样迅速复制并摧毁免疫系统。相反,HTLV-1采取了一种极为狡猾的策略:它将自身的基因组整合到宿主T细胞的DNA中,形成前病毒,然后随着宿主细胞的分裂而被动复制。这种"搭便车"式的繁殖方式使得HTLV-1能够终生潜伏在感染者体内,不引发任何急性症状,也不激起强烈的免疫反应。大多数感染者终其一生都不会出现任何症状,他们不知道自己体内携带着一枚定时炸弹。
然而,在约百分之五的感染者身上,这枚炸弹会爆炸。经过数十年甚至终生潜伏后,HTLV-1可能引发两种致命疾病:成人T细胞白血病/淋巴瘤和HTLV-1相关脊髓病/热带痉挛性瘫痪。前者是一种极具侵袭性的血液系统恶性肿瘤,后者是一种进行性神经系统疾病。为什么同样感染HTLV-1,有人终生无症状,有人却罹患绝症?这个问题至今仍是病毒学领域最引人入胜的谜题之一。
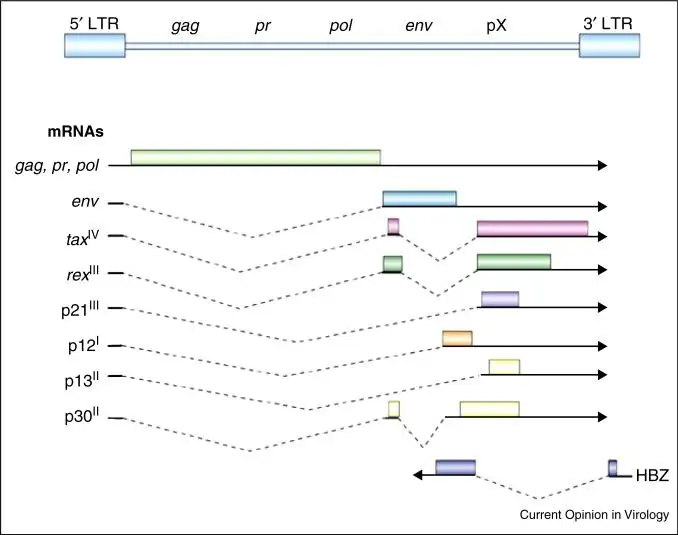
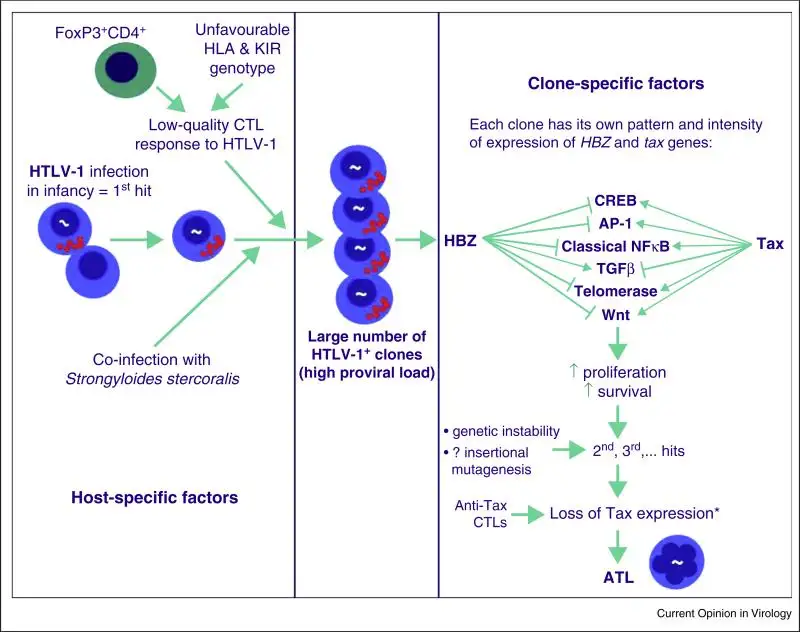
要理解HTLV-1如何致癌,我们需要深入到分子层面。HTLV-1基因组编码两种关键的调节蛋白:Tax和HBZ。Tax蛋白是病毒致癌的主力军。它是一种强效的转录激活因子,能够激活多种细胞信号通路,促进T细胞增殖。更重要的是,Tax能够干扰细胞的DNA修复机制,导致基因组不稳定,为癌症的发生创造条件。然而,Tax也是一把双刃剑——它的高免疫原性使得表达Tax的细胞很容易被宿主的细胞毒性T细胞识别和清除。
HBZ蛋白则扮演着更加隐秘的角色。与Tax不同,HBZ的免疫原性很低,能够逃避免疫系统的监视。研究表明,HBZ在几乎所有ATLL病例中都有表达,而Tax在许多病例中已经沉默或缺失。科学家们认为,HTLV-1感染后的致癌过程可能分为两个阶段:早期,Tax蛋白驱动感染细胞大量增殖,但同时也会激发免疫清除;晚期,Tax表达被沉默,而HBZ继续维持细胞的恶性表型,最终导致白血病的发生。
HTLV-1的另一个独特之处在于它的遗传稳定性。与HIV等逆转录病毒快速变异不同,HTLV-1在不同感染者之间、甚至不同地区之间,基因序列高度保守。这种罕见的稳定性源于HTLV-1独特的复制策略:它主要通过感染细胞的分裂而非病毒颗粒的传播来扩增。每当一个携带前病毒的T细胞分裂,前病毒DNA就被精确复制到两个子代细胞中,几乎不发生突变。这种机制使得科学家能够利用HTLV-1的序列变异来追踪人类迁徙历史,就像利用线粒体DNA一样。
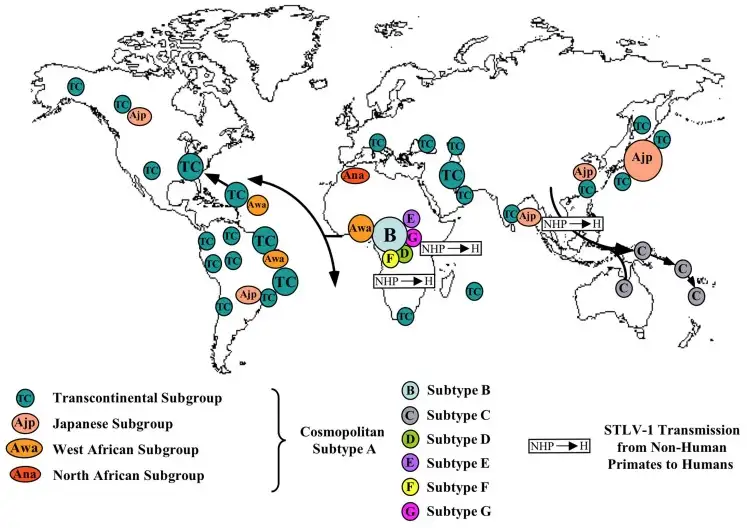
基于HTLV-1的分子流行病学研究揭示了一段跨越数千年的人类迁徙史。科学家发现,HTLV-1存在多个地理亚型:世界性亚型A广泛分布于日本、加勒比海、非洲和美洲;中非亚型B主要流行于中非地区;澳大拉尼西亚亚型C则发现于澳大利亚原住民和美拉尼西亚群岛居民中。最令人惊讶的是,亚型C与其他亚型的序列差异高达百分之三十,这意味着它已经在孤立人群中演化了数千年甚至上万年。
这些发现支持了一个引人入胜的假说:HTLV-1可能起源于非人类灵长类动物。在非洲和亚洲的多种猴类中,科学家发现了一种与HTLV-1高度相似的病毒——猿类T淋巴细胞病毒一号,简称STLV-1。分子钟分析表明,某些HTLV-1亚型可能是在数千年前通过跨物种传播从STLV-1演化而来。在遥远的过去,人类在狩猎、屠宰或饲养猴类的过程中,偶然接触到了感染STLV-1的猴类血液或体液,病毒跨越物种屏障,从此成为人类永恒的伴侣。
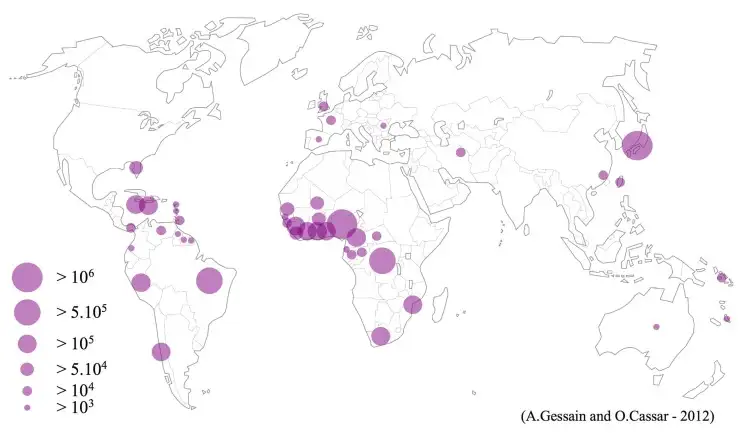
HTLV-1在全球的分布极不均匀。据世界卫生组织估计,全球约有五百万到一千万人感染HTLV-1,但这些人主要集中在几个特定的流行区域。最著名的高流行区是日本西南部的九州岛和冲绳群岛。在这些地区,某些年龄超过五十岁的人群中,HTLV-1感染率可高达百分之二十到四十。为什么这种病毒会在日本西南部如此集中?这可能与古代的人口迁徙模式有关。有学者认为,HTLV-1可能是随古代从东南亚或中国南方迁徙到日本的人群带入的。
另一个重要的高流行区是加勒比海地区。在牙买加、马提尼克、海地等岛屿,HTLV-1感染率可达百分之三到六。这里的病毒来源与悲惨的奴隶贸易历史密切相关。分子流行病学研究表明,加勒比海地区的HTLV-1毒株与西非的毒株高度相似,这强烈暗示病毒是随被贩卖的非洲奴隶带到美洲的。这一发现不仅揭示了病毒传播的历史,也为我们理解人类迁徙史提供了独特视角。
在非洲大陆,HTLV-1流行于撒哈拉以南的广大地区。加蓬、刚果、尼日利亚等国的部分地区感染率较高。有趣的是,非洲不仅是HTLV-1的可能起源地,也是病毒多样性最高的地区——所有已知的HTLV-1亚型几乎都能在非洲找到。这种遗传多样性支持了"非洲起源"假说:HTLV-1在非洲的人类群体中已经演化了数千年,期间分化出多个亚型,然后随人类迁徙传播到世界各地。
南美洲,特别是巴西、秘鲁、法属圭亚那等国的某些地区,也存在HTLV-1流行区。这里的病毒来源同样与奴隶贸易和移民有关。在法属圭亚那的诺瓦马龙人中,HTLV-1感染率高达百分之五以上。诺瓦马龙人是逃亡奴隶的后代,他们世代居住在与世隔绝的丛林中,保留了许多非洲传统,也保留了祖先带来的HTLV-1病毒。
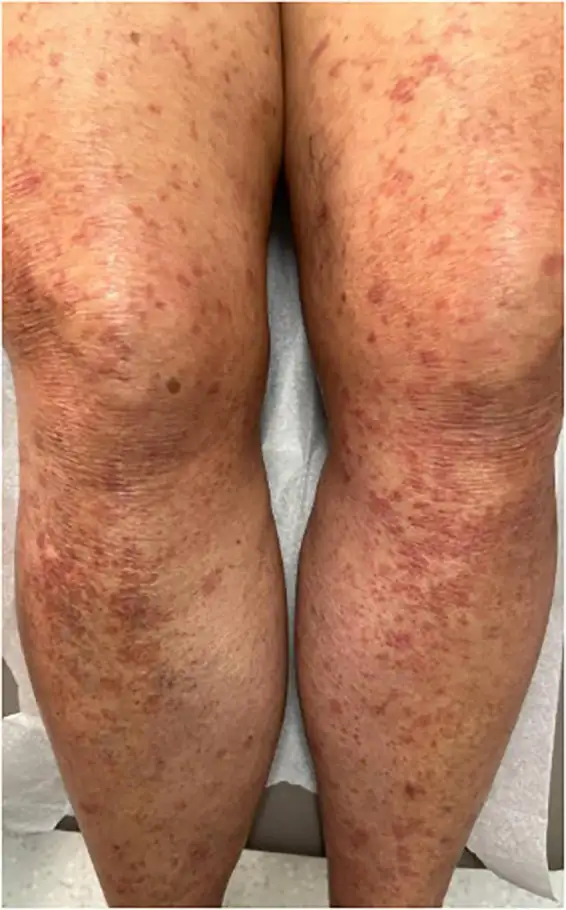
成人T细胞白血病/淋巴瘤,简称ATLL,是HTLV-1感染最可怕的后果。这种疾病最初由高月清团队在一九七七年描述,其临床特征极为独特:患者多为成年人,平均发病年龄约六十岁;血液中出现形态异常的淋巴细胞,这些细胞的细胞核呈花瓣状分叶,被称为"花细胞";患者常伴有皮肤病变、高钙血症和免疫缺陷;预后极差,急性型患者的中位生存期不足一年。
ATLL的诊断往往充满戏剧性。由于皮肤病变是ATLL最常见的临床表现之一,许多患者最初被当作皮肤病治疗。在流行地区,有经验的皮肤科医生看到难以解释的丘疹、结节或斑块时,会立即联想到ATLL,并要求进行HTLV-1抗体检测。然而,在非流行地区,这种疾病常常被误诊为其他类型的皮肤淋巴瘤或炎症性皮肤病,延误治疗时机。
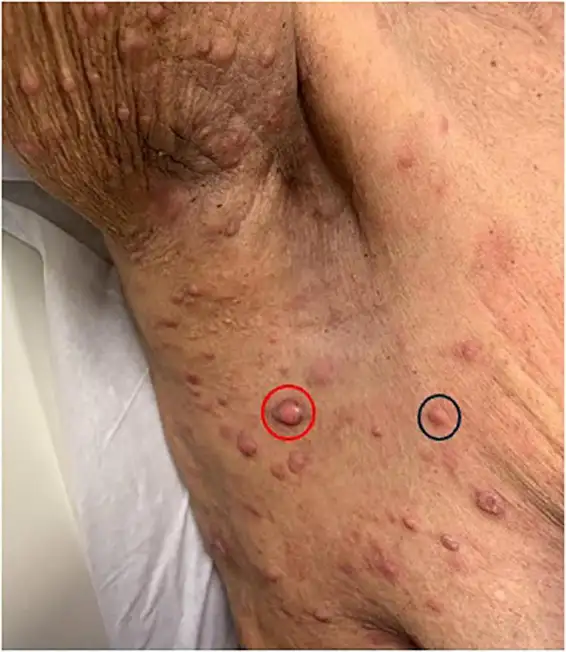
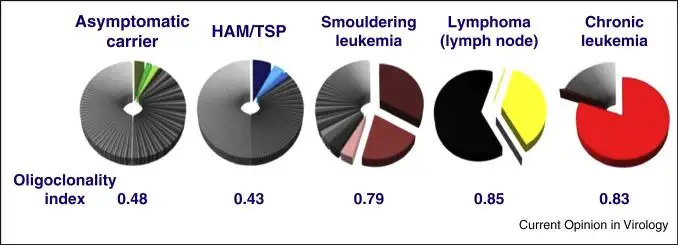
ATLL的临床亚型决定了患者的预后。根据下野正恒于一九九一年提出的分类系统,ATLL分为四型:急性型、淋巴瘤型、慢性型和冒烟型。急性和淋巴瘤型属于侵袭性,预后极差,中位生存期不足一年;慢性和冒烟型看似温和,但中位生存期也分别只有五点四年和两年九年。更令人沮丧的是,约半数的慢性型和冒烟型患者最终会转化为侵袭性急性型。
ATLL的治疗一直是血液肿瘤学的难题。传统的化疗方案对ATLL效果有限,完全缓解率低,复发率高。近年来,抗病毒药物齐多夫定联合干扰素-α的方案在部分患者中显示出疗效,尤其是慢性型和冒烟型患者。对于符合条件的患者,异基因造血干细胞移植是目前唯一可能治愈ATLL的方法,但移植相关死亡率高,许多患者因年龄或身体状况无法承受。新药研发方面,针对CCR4的单克隆抗体莫加珠单抗、组蛋白去乙酰化酶抑制剂等新型药物正在临床试验中。
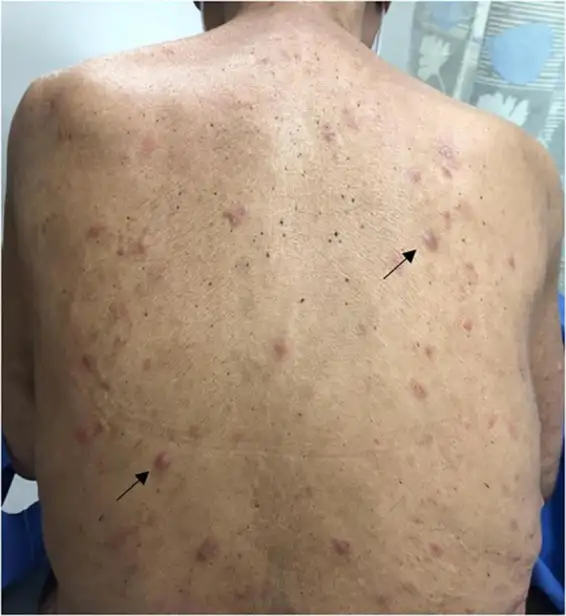
HTLV-1相关的另一种严重疾病是HTLV-1相关脊髓病/热带痉挛性瘫痪,简称HAM/TSP。这是一种慢性进行性神经系统疾病,主要表现为双下肢无力、痉挛和麻木,最终导致患者丧失行走能力。HAM/TSP的发病机制与ATLL不同:在HAM/TSP中,病毒蛋白引发的剧烈免疫反应攻击脊髓,导致神经损伤。有趣的是,HAM/TSP在女性中更常见,而ATLL在男性中略多见,提示激素或免疫因素可能影响疾病表型。
HAM/TSP的发现历程同样充满戏剧性。一九八五年,加勒比海地区的医生注意到,一种被称为"热带痉挛性瘫痪"的神经系统疾病在当地异常高发。同年,日本研究者描述了一种类似的疾病,命名为"HTLV-1相关脊髓病"。很快,科学家证实这是同一种疾病,由HTLV-1感染引起。这一发现不仅揭示了一种新疾病的病因,也拓展了人们对HTLV-1致病谱的认识——这种病毒不仅可以致癌,还可以攻击神经系统。
除了ATLL和HAM/TSP,HTLV-1还与多种其他疾病相关,包括葡萄膜炎、感染性皮炎、多发性肌炎、关节炎等炎症性疾病。这些疾病的发生可能与病毒蛋白引发的免疫紊乱有关。在某些流行地区,HTLV-1相关的葡萄膜炎是导致视力丧失的重要原因之一。
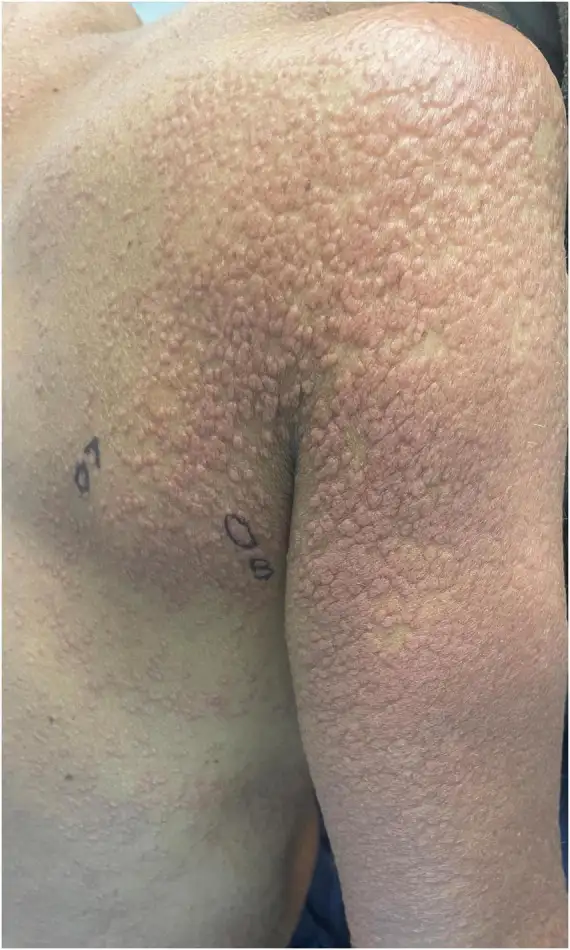
预防和控制HTLV-1感染面临着独特挑战。与HIV不同,HTLV-1感染在大多数国家并不属于法定报告传染病,全球范围内的流行病学监测数据非常有限。许多感染者终生不知自己携带病毒,因为常规体检不包括HTLV-1检测。在流行地区,一些国家已经采取了筛查措施。日本自一九八六年开始对所有献血者进行HTLV-1筛查,显著降低了输血传播风险。对于HTLV-1阳性母亲,建议避免母乳喂养或缩短母乳喂养时间,以减少母婴传播。
然而,HTLV-1的预防和控制仍面临诸多困难。首先,缺乏有效的疫苗。HTLV-1的免疫逃逸机制使得疫苗研发面临巨大挑战。其次,抗病毒治疗对已经整合的前病毒效果有限。虽然齐多夫定等药物可以抑制病毒复制,但无法清除已经整合到宿主基因组中的前病毒。第三,公众对HTLV-1的认知度低,即使在流行地区,许多人也不知道这种病毒的存在和危害。
HTLV-1研究的历史也是人类认识病毒与癌症关系的缩影。在HTLV-1被发现之前,许多人怀疑病毒是否能导致人类癌症。HTLV-1的发现不仅证实了这一可能性,也为后来发现HIV奠定了基础。有趣的是,加洛团队在研究HTLV-1的过程中开发出的T细胞培养技术,后来被证明对于分离HIV至关重要。可以说,HTLV-1的发现间接推动了艾滋病研究的进程。
HTLV-1与HIV的比较研究揭示了逆转录病毒的多样性和复杂性。两种病毒都感染CD4阳性T细胞,但采取了截然不同的生存策略。HIV以高突变率著称,每年每个位点可产生约百分之一的突变,使其能够迅速逃避免疫系统和抗病毒药物。HTLV-1则恰恰相反,其序列高度保守,主要通过细胞分裂而非病毒复制来扩增。这种策略使得HTLV-1能够长期潜伏,但也限制了它的传播效率。
HTLV-1研究的前沿领域之一是病毒如何调控宿主免疫系统。近年来的研究发现,HTLV-1能够诱导感染细胞表达一种叫做CCR4的趋化因子受体。这种受体不仅帮助病毒选择性感染特定亚群的T细胞,还可能参与恶性肿瘤的逃避免疫监视。基于这一发现,靶向CCR4的单克隆抗体莫加珠单抗已被批准用于治疗ATLL,成为靶向治疗的成功案例之一。
另一个前沿领域是表观遗传学在ATLL发病中的作用。研究发现,ATLL细胞中存在广泛的表观遗传学改变,包括DNA甲基化和组蛋白修饰异常。这些改变可能导致抑癌基因沉默和癌基因激活,促进肿瘤发生。基于这些发现,组蛋白去乙酰化酶抑制剂和EZH2抑制剂等表观遗传学药物正在ATLL临床试验中进行测试,初步结果令人鼓舞。
HTLV-1的社会学意义同样值得关注。在日本九州和冲绳地区,HTLV-1感染曾经是一种禁忌话题。携带者担心被歧视,许多人在求职、婚恋中隐瞒自己的感染状态。随着公众教育的普及,这种情况正在改善,但污名化问题仍然存在。在加勒比海和南美地区,HTLV-1流行与奴隶贸易历史的联系,也为这种病毒增添了文化和社会维度。
对于居住在流行地区的人们来说,HTLV-1检测是一个复杂的选择。知道自己是携带者意味着可以采取预防措施避免传播给下一代,但也意味着面临终生焦虑——即使只有百分之五的几率发展为疾病。一些学者主张在流行地区开展大规模筛查,另一些学者则担心筛查可能带来的心理负担和社会歧视。如何在公共卫生利益和个人权利之间取得平衡,仍是一个未解的难题。
HTLV-1的故事还在继续书写。随着分子生物学技术的进步,科学家们对这种病毒的认识不断深入。高通量测序技术揭示了HTLV-1前病毒在宿主基因组中的整合位点偏好性;单细胞技术帮助研究者追踪感染细胞的克隆演化;结构生物学研究阐明了病毒蛋白与宿主因子相互作用的分子细节。这些研究不仅深化了我们对HTLV-1的理解,也为开发新的诊断和治疗方法提供了理论基础。
当我们回顾HTLV-1被发现以来的四十多年历程,不禁感叹人类与病毒博弈的漫长与艰辛。从最初被当作地区性罕见疾病,到认识到这是一种全球性的公共卫生问题;从发现第一种人类致癌逆转录病毒,到开发出靶向治疗药物;从对病毒致癌机制一无所知,到深入到分子层面解析Tax和HBZ蛋白的功能——人类在认识和控制HTLV-1的道路上已经取得了长足进步,但距离最终战胜这种病毒还有很长的路要走。
HTLV-1的千年潜伏史提醒我们:在人类与病毒的博弈中,时间尺度往往超出我们的想象。当HTLV-1的祖先在数千年甚至上万年前首次感染人类时,人类文明尚在襒褓之中;当这种病毒随奴隶贸易横渡大西洋时,人类对病毒的存在一无所知;当高月清在九州观察到第一批ATLL患者时,人类刚刚开始理解逆转录病毒的奥秘。今天,我们终于有能力识别、检测、部分控制这种古老的病毒,但它仍然潜伏在数百万人的体内,等待着时机爆发。
这就是HTLV-1——一种沉默的致癌诅咒,一段跨越千年的潜伏史,一个关于病毒、癌症、人类迁徙和医学进步的故事。在人类与病毒的永恒博弈中,HTLV-1或许不如HIV那样声名狼藉,不如埃博拉那样恐怖骇人,但它以其独特的方式,深刻地影响了人类病毒学的发展,也提醒着我们:最危险的敌人,往往是最沉默的敌人。
参考文献
-
Poiesz BJ, Ruscetti FW, Gazdar AF, Bunn PA, Minna JD, Gallo RC. Detection and isolation of type C retrovirus particles from fresh and cultured lymphocytes of a patient with cutaneous T-cell lymphoma. Proc Natl Acad Sci USA. 1980;77(12):7415-7419.
-
Hinuma Y, Nagata K, Hanaoka M, et al. Adult T-cell leukemia: antigen in an ATL cell line and detection of antibodies to the antigen in human sera. Proc Natl Acad Sci USA. 1981;78(10):6476-6480.
-
Uchiyama T, Yodoi J, Sagawa K, Takatsuki K, Uchino H. Adult T-cell leukemia: clinical and hematologic features of 16 cases. Blood. 1977;50(3):481-492.
-
Yoshida M, Miyoshi I, Hinuma Y. Isolation and characterization of retrovirus from cell lines of human adult T-cell leukemia and its implication in the disease. Proc Natl Acad Sci USA. 1982;79(6):2031-2035.
-
Gessain A, Cassar O. Epidemiological aspects and world distribution of HTLV-1 infection. Front Microbiol. 2012;3:388.
-
Matsuoka M, Jeang KT. Human T-cell leukemia virus type 1 (HTLV-1) and leukemic transformation. Nat Rev Cancer. 2007;7(4):270-280.
-
Satou Y, Yasunaga J, Yoshida M, Matsuoka M. HTLV-I basic leucine zipper factor gene mRNA supports proliferation of adult T-cell leukemia cells. Proc Natl Acad Sci USA. 2006;103(3):720-725.
-
Shimoyama M. Diagnostic criteria and classification of clinical subtypes of adult T-cell leukaemia-lymphoma. Br J Haematol. 1991;79(3):428-437.
-
Iwanaga M, Watanabe T, Yamaguchi K. Adult T-cell leukemia: a review of epidemiological evidence. Front Microbiol. 2012;3:322.
-
Osame M, Usuku K, Izumo S, et al. HTLV-I associated myelopathy, a new clinical entity. Lancet. 1986;1(8488):1031-1032.
-
Gessain A, Barin F, Vernant JC, et al. Antibodies to human T-lymphotropic virus type-I in patients with tropical spastic paraparesis. Lancet. 1985;2(8452):407-410.
-
Takatsuki K. Discovery of adult T-cell leukemia. Retrovirology. 2005;2:16.
-
Gallo RC. History of the discoveries of the first human retroviruses: HTLV-1 and HTLV-2. Oncogene. 2005;24(39):5926-5930.
-
Katsuya H, Ishitsuka K, Utsunomiya A, et al. Treatment and survival among 1594 patients with ATL. Blood. 2015;126(24):2570-2577.
-
Tsukasaki K, Hermine O, Bazarbachi A, et al. Definition, prognostic factors, treatment, and response criteria of adult T-cell leukemia-lymphoma: a proposal from an international consensus meeting. J Clin Oncol. 2009;27(3):453-459.
-
Hanchard B. Adult T-cell leukemia/lymphoma in Jamaica: 1986-1995. J Acquir Immune Defic Syndr Hum Retrovirol. 1996;13(Suppl 1):S20-S25.
-
Sawada Y, Hino R, Hama K, et al. Type of skin eruption is an independent prognostic indicator for adult T-cell leukemia/lymphoma. Blood. 2011;117(15):3961-3967.
-
Bangham CRM, Araujo A, Yamano Y, Taylor GP. HTLV-1-associated myelopathy/tropical spastic paraparesis. Nat Rev Dis Primers. 2015;1:15012.
-
Martin F, Tagaya Y, Gallo R. Time to eradicate HTLV-1: an open letter to WHO. Lancet. 2018;391(10133):1893-1894.
-
Watanabe T. Current status of HTLV-1 infection. Int J Hematol. 2011;94(5):430-434.
-
Mahieux R, Gessain A. HTLV-3/STLV-3 and HTLV-4 viruses: discovery, epidemiology, serology and molecular aspects. Viruses. 2019;11(1):60.
-
Setoyama M, Katahira Y, Kanzaki T. Clinicopathologic analysis of 124 cases of adult T-cell leukemia/lymphoma with cutaneous manifestations. J Dermatol. 1999;26(12):785-790.
-
Marchetti M, Pulitzer M, Myskowski P, et al. Cutaneous manifestations of human T-cell lymphotrophic virus type-1-associated adult T-cell leukemia/lymphoma. J Am Acad Dermatol. 2015;72(2):293-301.
-
Iwanaga M, Watanabe T, Utsunomiya A, et al. Human T-cell leukemia virus type I (HTLV-1) proviral load and disease progression in asymptomatic HTLV-1 carriers. Blood. 2010;116(8):1211-1219.
-
Saito M, Bangham CRM. Immunopathogenesis of HTLV-1 associated diseases. Curr Opin Virol. 2012;2(4):460-465.