沉默的入侵者
1972年,德国埃朗根大学的病理实验室里,年轻的病毒学家哈拉尔德·楚尔·豪森(Harald zur Hausen)正凝视着显微镜下的一片宫颈组织切片。他的目光穿透染色后的细胞层,寻找着一个他坚信存在的敌人。这个敌人如此微小,以至于光学显微镜根本无法捕捉它的身影;这个敌人如此狡猾,以至于数十年来科学家们一直在错误的方向上追寻它的踪迹。
在那之前的二十年里,医学界普遍认为单纯疱疹病毒(HSV)是导致宫颈癌的罪魁祸首。教科书上白纸黑字地写着这一结论,研究资金流向HSV相关项目,无数科学家在这个假设上耗尽了职业生涯。但豪森不一样。他注意到一个令人困惑的现象:在宫颈癌组织中,单纯疱疹病毒的DNA几乎从不出现。如果HSV真是元凶,为什么它在犯罪现场从不留下指纹?
豪森的怀疑让他走向了一个在当时被视为异端的假设:宫颈癌的真正凶手可能是一种被认为只会引起无害疣体的病毒——人乳头瘤病毒(Human Papillomavirus,简称HPV)。这个假设如此大胆,以至于当他第一次在学术会议上提出时,听众席上响起了明显的笑声。
然而,豪森不知道的是,他即将开启一段长达十五年的孤独旅程。这段旅程将改变人类对癌症的理解,拯救数百万人的生命,并最终为他赢得诺贝尔奖。但在此之前,他将经历无数次实验失败、资金申请被拒、同行的嘲笑,以及那漫长而痛苦的等待——等待一个可能永远不会到来的答案。
更令人震惊的是,豪森追踪的这个敌人,已经与人类纠缠了数千年。古埃及的医学纸草书记载了它的痕迹,中世纪的欧洲将它视为上帝的惩罚,而到了二十世纪,它已经悄无声息地成为全球女性第四大癌症杀手。每年,超过三十五万名女性因为这个病毒而失去生命,而其中绝大多数人甚至从未听说过它的名字。
这是一个关于隐形杀手的故事,一个关于两个微小蛋白质如何瓦解人体最强大防御机制的故事,也是一个关于人类如何在绝望中找到希望的故事。
被遗忘的线索
要理解HPV如何成为人类医学史上最成功的隐形杀手,我们需要回到更早的时代。
早在古希腊时期,希波克拉底就已经描述过一种"女性子宫口的恶性肿瘤"。当时的人们对这种疾病的成因一无所知,只能眼睁睁看着患者痛苦地死去。这种疾病似乎特别青睐性生活活跃的女性,这一观察让中世纪的医生们将其归咎于道德败坏,而非任何生物学机制。
1842年,意大利帕多瓦的医生多梅尼科·里戈尼-斯特恩(Domenico Rigoni-Stern)发表了一项开创性的研究。他分析了帕多瓦地区多年的死亡记录,发现一个惊人的模式:宫颈癌几乎只发生在已婚妇女和寡妇身上,修女几乎从不患此病。这一发现暗示了疾病的某种"性传播"特性,但里戈尼-斯特恩并不知道到底是什么在传播。
1884年,意大利医生吉罗拉莫·塞尼奥尼(Girolamo Segnini)观察到一个更令人困惑的现象:患有生殖器疣的女性似乎更容易患上宫颈癌。这些疣体——后来被确认为由HPV引起——与癌症之间似乎存在某种神秘的联系。但当时的科学家们无法理解一种引起疣体的病毒如何能导致癌症。
真正的突破要等到二十世纪初。1907年,意大利科学家朱塞佩·奇菲(Giuseppe Ciuffo)首次证明寻常疣可以通过无细胞滤液传播,这意味着疾病是由病毒而非细菌引起的。这是人类第一次捕捉到HPV存在的间接证据,但奇菲并不知道他发现的是什么病毒。
随着电子显微镜的发明,科学家们终于在1949年首次看到了人乳头瘤病毒的真面目。在放大数万倍的镜头下,这些病毒呈现出完美的球形,直径仅有55纳米,由72个蛋白质亚单位组成一个二十面体的外壳。它们看起来如此简洁优雅,以至于没有人能想象它们内部的基因组携带着足以摧毁人类生命的武器。

人乳头瘤病毒的电子显微镜图像,显示出其标志性的球形二十面体结构。每个病毒颗粒直径约55纳米,由72个蛋白质亚单位组成。这种看似简单的结构内部携带着编码E6和E7致癌蛋白的基因组。
然而,电子显微镜揭示了一个更复杂的问题:科学家们发现存在多种不同类型的HPV。一些类型引起的是手脚上的寻常疣,另一些引起生殖器疣,还有一些似乎不引起任何症状。这些不同类型的HPV之间有什么区别?哪些类型是危险的?这些问题在二十世纪六十年代仍然没有答案。
与此同时,一个更根本的问题困扰着研究者们:HPV真的会导致癌症吗?
在二十世纪七十年代初期,主流科学界对这个问题的回答是明确的否定。当时,单纯疱疹病毒(HSV)被广泛认为是宫颈癌最可能的病因。HSV是一种DNA病毒,在培养皿中很容易生长,研究表明它可以诱导细胞转化,而且在宫颈癌患者体内经常能检测到HSV抗体。一切似乎都指向HSV。
但哈拉尔德·楚尔·豪森看到了别人忽略的细节。
异端者的执着
豪森1936年出生于德国盖尔森基兴,在杜塞尔多夫大学获得医学学位后,于1960年代末期开始研究病毒与癌症的关系。他最初的兴趣集中在另一种病毒上,但很快就被HPV这个谜题所吸引。
令豪森困惑的是HSV假设中的一个致命缺陷:如果HSV是宫颈癌的病因,那么HSV的DNA应该能够持续在宫颈癌组织中被检测到。然而,当时最敏感的检测方法也无法在大多数宫颈癌标本中找到HSV的遗传物质。一个真正的致癌病毒应该将其基因组整合到宿主细胞的DNA中,从而驱动细胞的恶性转化。如果HSV做不到这一点,它如何能导致癌症?
1974年,豪森在佛罗里达州基西米举行的国际乳头瘤病毒会议上首次公开提出了他的假说:HPV,而非HSV,才是宫颈癌的真正病因。他引用了一些初步的实验数据,显示在某些宫颈癌组织中存在HPV的DNA序列。
会议的反应是冷淡的,甚至是嘲讽的。一位资深科学家公开质疑豪森的方法论,暗示他可能只是检测到了污染。另一位评论者指出,HPV是一种极其常见的病毒,大多数成年人在一生中都会感染,如果HPV真的导致癌症,为什么不是每个人都患癌?
豪森知道这是一个好问题。他也知道答案可能隐藏在HPV的多样性之中。
回到德国后,豪森开始了一项艰苦卓绝的研究计划。他的策略是使用当时最先进的分子杂交技术,系统地搜索宫颈癌组织中是否存在HPV的DNA。他的团队收集了数百份宫颈癌标本,逐一进行检测。
过程是痛苦缓慢的。每一次实验都需要数天时间,而大多数样本给出的结果是阴性。资助机构开始质疑这项研究的价值,一些同事建议豪森放弃这个"死胡同"。到1970年代末期,豪森的实验室已经花光了研究经费,他不得不四处借钱购买实验材料。
但豪森有一个直觉:他们一直没有找到HPV,可能是因为他们一直在用错误的探针搜索。
当时已知的HPV类型只有少数几种,科学家们使用针对这些类型的DNA探针来检测癌症组织。但豪森开始怀疑,导致宫颈癌的可能是某种尚未被发现的HPV类型。
1983年,豪森的坚持终于得到了回报。他的团队从一位宫颈癌患者的组织标本中克隆出了一段全新的HPV DNA序列。这种病毒与已知的HPV类型有显著差异,豪森将其命名为HPV-16。
几个月后,他们在另一位患者的标本中发现了另一种新类型,命名为HPV-18。
接下来的发现震惊了整个病毒学界:豪森的团队发现,大约70%的宫颈癌标本中含有HPV-16或HPV-18的DNA。这两种HPV类型的基因组被整合到了癌细胞的染色体中,这是致癌病毒的经典特征。
豪森的假说终于得到了证实。但更令人震惊的发现还在后面。
细胞内部的战争
当豪森的团队深入分析HPV-16和HPV-18的基因组时,他们发现了这些病毒如此危险的秘密武器。
HPV的基因组极其精简,总共只有约8000个碱基对,编码区区8个蛋白质。与拥有超过两万个基因的人类基因组相比,HPV的武器库看起来贫瘠得可怜。然而,这8个蛋白质中的两个——E6和E7——拥有足以瓦解人体最强大防御机制的能力。
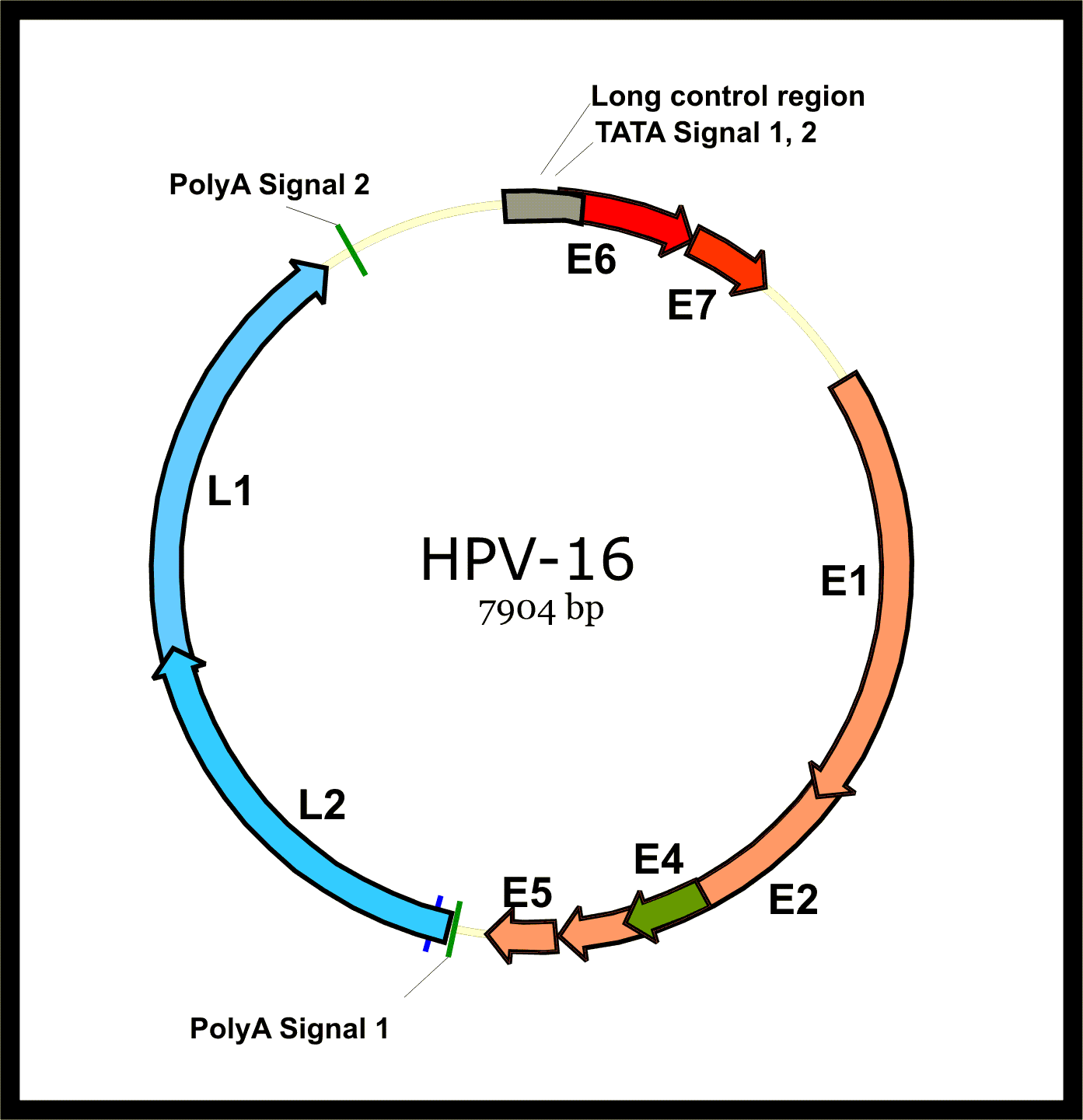
HPV-16病毒基因组结构示意图。环形DNA基因组约8000个碱基对,编码8种蛋白质。早期基因(E1-E7)负责病毒复制和致癌转化,其中E6和E7是主要的致癌蛋白。晚期基因(L1和L2)编码病毒外壳蛋白。
要理解E6和E7是如何工作的,我们需要首先了解人体的肿瘤抑制系统。
在每一个正常细胞的基因组中,存在着一组被称为"肿瘤抑制基因"的守护者。其中最重要的是p53和Rb(视网膜母细胞瘤蛋白)。p53被称为"基因组守护者",它监控着细胞的DNA完整性。当DNA受到损伤时,p53会启动修复程序;如果损伤过于严重,p53会命令细胞自杀——这在生物学上被称为"凋亡"。通过这种方式,p53确保了任何可能发展成癌细胞的异常细胞都被及时清除。
Rb蛋白则控制着细胞分裂的"刹车踏板"。在正常情况下,Rb会阻止细胞在不该分裂的时候进入分裂周期。只有当细胞准备好进行分裂时,Rb才会被暂时失活,允许细胞复制其DNA并分裂。
这两个蛋白质共同构成了人体对抗癌症的第一道防线。任何想要发展成癌症的细胞,都必须首先突破这道防线。
这正是E6和E7的专长。
HPV的E6蛋白质像一个精密的刺客,专门猎杀p53。E6不会直接攻击p53,而是利用人体细胞内的一种蛋白质——E6相关蛋白(E6AP)——作为中介。E6、E6AP和p53三者形成一个复合物,然后E6AP给p53贴上一个"垃圾"标签。这个标签是一串名为"泛素"的小蛋白质分子。当p53被泛素化后,细胞的垃圾处理系统——蛋白酶体——就会识别并降解它。
通过这种精巧的机制,E6将p53从细胞的守护者变成了它的猎物。失去p53的细胞不再能够检测DNA损伤,也不再能够启动凋亡程序。那些本应被清除的异常细胞,现在可以肆无忌惮地积累突变。
E7则负责攻破第二道防线——Rb蛋白。E7与Rb结合后,会强行将Rb从它本应结合的位置上拉下来。失去了Rb的抑制,细胞分裂的"刹车踏板"被踩到底,细胞开始疯狂地复制和分裂。
当E6和E7同时发挥作用时,后果是灾难性的:细胞失去了DNA损伤检测能力,失去了凋亡能力,失去了对分裂的控制。这正是癌症的开始。
但HPV为什么要这样做?毕竟,杀死宿主对病毒本身也没有好处。
答案在于HPV的生命周期。HPV是一种专门感染上皮细胞的病毒。在正常的上皮细胞中,只有位于基底层的细胞才具有分裂能力。当基底细胞分裂时,产生的子细胞会逐渐向上迁移,分化成不同层次的上皮细胞,最终在表层死亡脱落。
HPV的繁殖需要宿主细胞的DNA复制机制,而这种机制只在分裂中的细胞中活跃。因此,HPV需要刺激其感染的细胞保持分裂状态。E6和E7正是为此而进化出来的工具:它们让细胞保持"年轻"和"活跃",为病毒复制提供必要的条件。
在大多数HPV感染中,这个过程是短暂的。当免疫系统识别并清除感染后,病毒被消灭,一切恢复正常。但在某些情况下——特别是当感染的是高危型HPV如HPV-16或HPV-18时——病毒的基因组可能会整合到宿主细胞的染色体中。整合过程往往导致E6和E7基因的表达失控,这些蛋白质开始以更高的水平、更长的时间产生。
这就是癌症的开始。从HPV感染到宫颈癌发展,通常需要15到20年的时间。在这漫长的潜伏期中,细胞不断积累突变,最终变成侵袭性的癌细胞。
豪森的发现不仅解释了HPV如何导致癌症,还揭示了一个更深刻的真理:癌症可以被病毒引起。这为人类征服癌症开辟了一条全新的道路——如果我们可以预防病毒感染,就可以预防癌症。
不可能的疫苗
在豪森发现HPV-16和HPV-18的同年,澳大利亚布里斯班,两位科学家正在思考一个被认为不可能的问题:我们能制造出针对HPV的疫苗吗?
伊恩·弗雷泽(Ian Frazer)是一位苏格兰出生的免疫学家,1985年来到澳大利亚昆士兰大学建立自己的实验室。他的研究重点是HPV感染如何影响男性的免疫系统。在他的研究中,他注意到一个令人沮丧的事实:HPV似乎能够有效地躲避免疫系统的侦测。
1989年,弗雷泽在剑桥大学度假时遇到了中国病毒学家周健。周健当时正在剑桥研究HPV的分子生物学,他对这种病毒的蛋白质结构有着深刻的理解。两人很快建立了友谊,并开始讨论合作的可能性。
弗雷泽说服周健搬到澳大利亚,加入他的研究团队。1990年,两人开始了一场大胆的冒险:试图开发出世界上第一种预防癌症的疫苗。
他们面临的挑战是前所未有的。
传统的疫苗开发依赖于在实验室中培养病毒。科学家们会让病毒在细胞培养物中繁殖,然后灭活或减毒这些病毒,制成疫苗。当人体接种疫苗后,免疫系统会"记住"病毒的样子,在真正遇到病毒时能够迅速发起攻击。
但HPV是一种特殊的病毒。它只能在活的人体上皮细胞中繁殖,无法在实验室培养皿中生长。更糟糕的是,HPV的基因组一旦整合到宿主细胞中,就有导致癌症的风险。即使科学家们能够培养HPV,使用活的或灭活的HPV作为疫苗也太危险了。
另一个选择是使用重组DNA技术,在实验室中生产HPV的蛋白质外壳。这种方法已经在乙肝疫苗的开发中取得成功。但HPV的外壳由两种蛋白质组成——L1和L2——而早期的尝试表明,单独表达这些蛋白质只能产生无结构的蛋白质聚集体,无法组装成病毒的样子。
这里的"样子"至关重要。免疫系统并不针对单个蛋白质分子产生强烈反应,它需要看到病原体的整体形态才能被有效激活。如果疫苗不能模拟HPV的真实外观,它就无法诱导足够的免疫反应。
弗雷泽和周健陷入了一个看似无解的困境。直到1991年初,一个突破性的想法改变了历史。
周健提出,也许问题不在于蛋白质本身,而在于表达系统。他和他的妻子、同为研究者的孙小依开始尝试使用一种特殊的细胞系来表达HPV的L1和L2蛋白质。他们选择了能够正确进行蛋白质折叠和修饰的真核细胞,而不是通常使用的细菌表达系统。
1991年3月的一个下午,孙小依在电子显微镜下观察到了她一生中最美丽的画面:在培养皿中,无数微小的球形颗粒正在闪烁。这些颗粒看起来与真正的HPV完全一样,拥有完美的二十面体结构,有72个亚单位整齐排列。但它们没有基因组——它们是空的。
这些"病毒样颗粒"(Virus-Like Particles,简称VLPs)正是弗雷泽和周健一直在寻找的答案。它们拥有HPV的外观,因此能够有效激活免疫系统;但它们没有致癌的遗传物质,因此绝对安全。
1991年6月,弗雷泽和周健提交了临时专利申请。他们知道,这只是漫长旅程的开始。从实验室发现到可用的疫苗,还需要经历漫长的临床试验、监管审批和大规模生产。他们没有预料到的是,其中一个主要发明者将永远无法看到这项发明改变世界的那一天。
永恒的贡献
1999年3月9日,周健因肝炎并发症在杭州去世,年仅42岁。
周健1957年出生于杭州,在温州医学院完成医学教育后,先后在浙江医科大学和河南医科大学获得硕士和博士学位。1988年,他来到英国剑桥大学从事博士后研究,在那里遇到了伊恩·弗雷泽。
周健的贡献是HPV疫苗成功的关键。他不仅提出了VLP技术的核心概念,还亲自设计了实验方案,指导他的妻子孙小依完成了关键的蛋白质表达和纯化工作。他对HPV蛋白质结构的深刻理解,使得VLP能够在正确的条件下自组装成病毒形态。
周健的去世让整个HPV疫苗研发团队陷入悲痛。但弗雷泽和他们的同事们决定继续推进这项工作,完成周健未竟的事业。
2006年,经过15年的开发和临床试验,第一支HPV疫苗——Gardasil——终于获得美国FDA批准上市。Gardasil是一种四价疫苗,针对HPV-6、HPV-11、HPV-16和HPV-18四种类型。其中HPV-16和HPV-18是导致宫颈癌的主要元凶,而HPV-6和HPV-11则导致生殖器疣。

Gardasil是全球第一款获批的HPV疫苗,由默克公司研发。这种疫苗使用病毒样颗粒(VLP)技术,能够预防四种HPV类型的感染,包括导致约70%宫颈癌的HPV-16和HPV-18。
临床试验的结果令人振奋:在未感染HPV的女性中,Gardasil对HPV-16和HPV-18相关病变的保护效力接近100%。这是人类历史上第一支能够预防癌症的疫苗。
2007年,另一种HPV疫苗——Cervarix——也获得批准。Cervarix是二价疫苗,专门针对HPV-16和HPV-18。两种疫苗都使用VLP技术,但采用了不同的佐剂和生产系统。
2008年,哈拉尔德·楚尔·豪森因"发现人乳头瘤病毒导致宫颈癌"而获得诺贝尔生理学或医学奖。在斯德哥尔摩的颁奖典礼上,他回顾了自己长达三十年的研究历程,感谢了所有支持他的人。
但豪森也知道,他的发现只是一个更大故事的开端。HPV疫苗的问世,标志着人类与这种隐形杀手之间的战斗进入了全新的阶段。
隐藏的真相
当科学家们在实验室中追逐HPV的秘密时,一个更加复杂的故事正在医院和诊所中悄然展开。
1999年,美国医生Maura Gillison在研究头颈部癌症时注意到了一个奇怪的趋势:在过去的几十年里,与吸烟和饮酒相关的头颈部癌症发病率在稳步下降,这得益于公共卫生运动减少了吸烟率。但与此同时,一种特殊类型的口咽癌——发生在扁桃体和舌根的鳞状细胞癌——的发病率却在上升,尤其是在中年男性中。
Gillison决定检测这些肿瘤组织是否含有HPV的DNA。结果令她震惊:大约60%的口咽癌样本呈HPV阳性,而且几乎都是HPV-16型。
这个发现颠覆了医学界对口咽癌的认识。传统上,口咽癌被认为是由吸烟和饮酒引起的,患者通常是老年男性,预后较差。但HPV阳性的口咽癌患者却呈现出完全不同的特征:他们更年轻,往往没有吸烟或饮酒史,社会经济地位较高,而且——最令人惊讶的是——他们对治疗的反应更好,生存率更高。
进一步的研究揭示了一个令人不安的真相:HPV阳性的口咽癌主要通过口交传播。当口腔黏膜接触到感染HPV的生殖器时,病毒可以通过微小的伤口进入口腔上皮细胞,开始同样的致癌过程。
流行病学数据显示,HPV阳性口咽癌的发病率在过去三十年里增长了超过200%。在美国,每年有超过18,000例HPV相关的口咽癌新病例,其中绝大多数是男性。一些专家预测,在不久的将来,HPV阳性口咽癌的发病率可能超过宫颈癌。
这个发现引发了关于HPV疫苗的新讨论。虽然HPV疫苗最初被批准用于预防宫颈癌,但越来越多的证据表明,它也可以预防HPV相关的口咽癌。2018年,美国FDA批准Gardasil 9用于预防HPV相关的口咽癌。
然而,HPV阳性口咽癌的兴起也暴露了HPV疫苗推广中的一个关键问题:最初的疫苗接种计划主要针对女孩,目的是预防宫颈癌。如果要让疫苗发挥最大作用,预防HPV在人群中的传播,男孩也应该被纳入接种计划。
2011年,美国疾病控制与预防中心(CDC)建议将HPV疫苗纳入男孩的常规免疫计划。随后,越来越多的国家开始实施性别中立的HPV疫苗接种政策。
永生的细胞
在HPV的故事中,有一个特殊的角色不能被遗忘。她的名字叫亨丽埃塔·拉克斯(Henrietta Lacks),她的细胞以一种意想不到的方式改变了医学史。
1951年1月29日,31岁的非裔美国女性亨丽埃塔·拉克斯来到巴尔的摩的约翰·霍普金斯医院。她告诉医生,她感觉到子宫里有一个"肿块"。妇科医生霍华德·琼斯检查后发现,她的宫颈上有一个紫色的、光滑的肿块,一碰就出血。活检结果确认了最坏的诊断:宫颈癌。
当时,约翰·霍普金斯医院的组织培养实验室负责人乔治·盖伊(George Gey)正在寻找一种能够在实验室中无限增殖的人类细胞。这种细胞将为医学研究提供无尽的资源,使科学家能够在培养皿中研究疾病和药物。但Gey的所有尝试都失败了——从患者身上取下的细胞通常在几天内就会死亡。
当拉克斯的肿瘤组织被送到Gey的实验室时,他的技术员玛丽·库比切克(Mary Kubicek)按照惯例将组织切成小块,放在培养瓶中。她并没有抱太大希望——之前的几百个样本都失败了。
但这一次,奇迹发生了。
拉克斯的癌细胞以惊人的速度繁殖。每隔20到24小时,它们的数量就会翻倍。Gey兴奋地将这些细胞命名为"HeLa"——取自亨丽埃塔·拉克斯姓名的前两个字母。
HeLa细胞成为人类历史上第一个"永生化"的人类细胞系。它们被分发到世界各地的实验室,用于各种医学研究。1954年,乔纳斯·索尔克使用HeLa细胞测试了他的脊髓灰质炎疫苗,帮助终结了这种可怕的疾病。此后,HeLa细胞被用于研究癌症、艾滋病、基因图谱、辐射效应等几乎每一个医学领域。

HeLa细胞的显微镜图像,显示细胞分裂的不同阶段(中期和末期)。这些来自亨丽埃塔·拉克斯宫颈癌的细胞因其HPV感染导致的E6和E7蛋白表达而获得了永生化能力,成为医学研究中最重要的人类细胞系。
然而,亨丽埃塔·拉克斯本人对这些一无所知。1951年10月4日,她在约翰·霍普金斯医院去世,年仅31岁。癌细胞已经扩散到她全身的每一个器官。
更令人不安的是,拉克斯的家人在接下来的二十多年里都不知道HeLa细胞的存在。直到1975年,在一次偶然的谈话中,拉克斯的家人才得知她的细胞正在世界各地的研究实验室中繁殖。更糟糕的是,研究人员多次联系拉克斯家族成员,要求提供血液样本用于研究,但从未解释原因。
HeLa细胞的故事揭示了医学研究中的伦理问题——知情同意、隐私保护、利益分享——这些问题至今仍在引发讨论。但这个故事也以一种深刻的方式与HPV的故事相连:HeLa细胞的永生化正是HPV E6和E7蛋白质作用的结果。正是这两种蛋白质对p53和Rb的抑制,使得亨丽埃塔·拉克斯的癌细胞获得了无限增殖的能力。
2013年,经过与拉克斯家族的协商,美国国立卫生研究院同意让两位家族代表参与决定谁可以访问HeLa细胞的基因组数据。2021年,亨丽埃塔·拉克斯的遗产起诉了赛默飞世尔科技公司,指控该公司未经许可商业化利用HeLa细胞。2023年,双方达成了和解。
2020年,亨丽埃塔·拉克斯被追授入选美国国家女性名人堂。她的墓碑上刻着这样的铭文:“她的不朽细胞将永远帮助人类。”
筛查的革新
在HPV疫苗问世之前,人类对抗宫颈癌的主要武器是筛查。这场革命的领导者是一位希腊裔美国科学家,他的名字被刻在每一位女性健康检查单上。
乔治斯·帕帕尼科劳(Georgios Papanikolaou)1883年出生于希腊基米岛,在雅典大学获得医学学位后,于1913年移民美国。在康奈尔大学医学院,他开始研究女性生殖系统的细胞学变化。
帕帕尼科劳的妻子安德洛玛赫(人称玛丽)成为他最重要的研究伙伴。为了研究女性月经周期中的细胞变化,玛丽每天提供自己的阴道分泌物样本,并亲自处理和染色这些样本。这种奉献持续了21年。
1920年,帕帕尼科劳在检查一位女性患者的宫颈细胞样本时,发现了异常的癌细胞。他后来回忆说:“第一次在宫颈涂片中观察到癌细胞,是我科研生涯中经历的最大激动之一。”
1928年,帕帕尼科劳在一次医学会议上介绍了这种简单、廉价的宫颈癌筛查方法:医生只需要用刮片从宫颈收集一些细胞,涂抹在玻璃片上,染色后在显微镜下观察。但当时医学界对这个方法反应冷淡,许多人认为这太简单了,不可能有效。
帕帕尼科劳没有放弃。1941年,他与妇科医生赫伯特·特劳特合作发表了一篇里程碑式的论文,基于对3000多例病例的研究,证明了"巴氏涂片"检测宫颈癌的有效性。1943年,他们出版了专著《阴道涂片诊断子宫癌》,奠定了现代细胞病理学的基础。
巴氏涂片(Pap smear)很快成为全球最广泛使用的癌症筛查方法之一。通过定期筛查,医生可以在癌症发展的早期阶段发现异常细胞,及时治疗,从而大大降低宫颈癌的死亡率。在美国,自巴氏涂片普及以来,宫颈癌的死亡率下降了超过70%。
异常巴氏涂片的显微镜图像,显示宫颈上皮细胞发生异常变化。正常的宫颈细胞排列整齐、大小均匀,而异常细胞则表现出核增大、核浆比例失调、染色质增粗等癌前病变特征。
帕帕尼科劳一生获得了无数荣誉,包括1950年的阿尔伯特·拉斯克临床医学研究奖——这被认为是美国的"诺贝尔奖"。但他始终未能获得真正的诺贝尔奖,尽管他先后被提名五次。一些历史学家认为,这可能是因为诺贝尔奖委员会对诊断工具类研究的偏见。
帕帕尼科劳于1962年因心脏病在迈阿密去世。他的妻子玛丽继续他在迈阿密大学建立的研究所的工作,直到1982年去世。
今天,巴氏涂片仍然是宫颈癌筛查的主要手段,但一种新的方法正在逐渐取代它:HPV DNA检测。这种检测方法直接寻找高危型HPV的遗传物质,比巴氏涂片更敏感,能够更早发现感染。研究表明,HPV DNA检测可以发现那些巴氏涂片可能漏掉的癌前病变。
世界卫生组织建议,女性从30岁开始进行HPV DNA检测,每5到10年进行一次。对于HIV感染者,筛查应该从25岁开始,每3到5年进行一次。
全球挑战
尽管HPV疫苗和筛查手段的出现为消除宫颈癌提供了技术可能,但现实情况仍然令人忧心。
根据世界卫生组织的数据,2022年全球有约66万例宫颈癌新发病例和35万例死亡。这意味着每两分钟就有一名女性死于宫颈癌。更令人不安的是,这些死亡中的94%发生在低收入和中等收入国家。
这种巨大的地理差异反映了全球卫生资源分配的不平等。在高收入国家,广泛的筛查项目和疫苗接种计划已经大幅降低了宫颈癌的发病率和死亡率。但在低收入国家,许多女性甚至没有机会接受一次巴氏涂片检查,更不用说昂贵的HPV疫苗。
以撒哈拉以南非洲为例,这里是全球宫颈癌负担最重的地区。在马拉维、莫桑比克和赞比亚等国,宫颈癌是女性癌症死亡的首要原因。这些国家面临的挑战是多方面的:医疗基础设施薄弱,缺乏训练有素的医护人员,筛查设备短缺,疫苗价格高昂,文化障碍阻止女性寻求医疗服务。
即使在高收入国家内部,健康不平等同样存在。在美国,非裔女性和拉丁裔女性的宫颈癌发病率和死亡率明显高于白人女性。这些差异与社会经济地位、医疗保险覆盖、医疗服务的可及性密切相关。
2020年,世界卫生组织启动了加速消除宫颈癌的全球战略。这是人类历史上第一次承诺消除一种癌症。该战略设定了三个关键目标——被称为"90-70-90"目标——到2030年实现:
90%的女孩在15岁前完成HPV疫苗接种; 70%的女性在35岁和45岁时接受高效筛查检测; 90%的癌前病变和癌症患者得到适当治疗。
模型研究预测,如果这些目标得以实现,到2120年,可以预防7400万例宫颈癌新发病例和6200万例死亡。
但要实现这些目标,需要前所未有的全球合作和资源动员。HPV疫苗的价格仍然是一个主要障碍,尽管一些发展中国家已经通过全球疫苗免疫联盟(GAVI)获得了价格优惠。筛查和治疗基础设施的建设需要大量投资。社区教育和文化敏感性的工作同样不可或缺。
新的希望
近年来,HPV疫苗领域出现了一系列令人鼓舞的进展。
2014年,美国FDA批准了Gardasil 9,这是一种九价疫苗,针对九种HPV类型。除了HPV-6、11、16和18之外,它还覆盖了HPV-31、33、45、52和58,这些类型加起来导致了大约20%的宫颈癌。研究表明,Gardasil 9可以预防约90%的宫颈癌和80-85%的HPV相关口咽癌。
更令人振奋的是,越来越多的证据表明,单剂HPV疫苗可能足以提供长期保护。传统的接种方案需要两到三剂,这增加了成本和物流复杂性。如果单剂方案被证实有效,将大大简化疫苗接种的实施,特别是在资源有限的环境中。
2022年,世界卫生组织免疫战略专家组建议,9到14岁的女孩可以接种一到两剂HPV疫苗,而15到26岁的女性可以接种一到三剂。这一建议为各国提供了更大的灵活性来设计适合本国国情的疫苗接种计划。
在筛查方面,自取样技术的进步为提高筛查覆盖率开辟了新途径。女性可以在家中使用简单的工具收集自己的阴道分泌物样本,然后邮寄到实验室进行HPV DNA检测。研究表明,自取样的准确性可以与医生取样相媲美。这种方法特别适合那些难以获得医疗服务的女性,包括生活在偏远地区的女性和对妇科检查感到不适的女性。
在治疗方面,研究人员正在开发针对已建立的HPV感染的治疗性疫苗。与预防性疫苗不同,治疗性疫苗旨在激活免疫系统清除已经存在的感染和癌前病变。虽然这些疫苗仍处于临床试验阶段,但一些早期结果令人期待。
永恒的战斗
从哈拉尔德·楚尔·豪森1974年首次提出HPV致癌假说,到2006年第一支HPV疫苗问世,人类用了32年时间。从亨丽埃塔·拉克斯1951年去世,到她的家族获得对HeLa细胞基因组数据的一定控制权,花了62年。从乔治斯·帕帕尼科劳1928年介绍巴氏涂片,到这种方法成为全球宫颈癌筛查的标准,经历了近二十年。
这些时间线提醒我们,医学进步往往是缓慢而艰难的。它们需要科学家的执着、患者的配合、资金的支持、政策的推动。每一个突破的背后,都有无数次失败、质疑和挫折。
但它们也告诉我们,进步是可能的。
曾经被认为是不治之症的宫颈癌,现在可以被预防、被早期发现、被治愈。曾经被认为是"不可能"的癌症疫苗,现在已经保护了数亿人。曾经被认为是"宿命"的疾病,现在被揭示为一种可预防的病毒感染。
HPV的故事仍在继续。每年仍有数十万女性因为缺乏筛查和疫苗而死于宫颈癌。HPV阳性口咽癌的发病率仍在上升。健康不平等仍然是一个全球挑战。
但我们已经拥有了战胜这个隐形杀手的武器。问题不再是"我们能不能",而是"我们愿不愿意"。这需要政治意愿、全球合作、资源分配,以及对每一个生命的尊重——无论她生活在世界的哪个角落,无论她有多大的经济能力。
在布里斯班的昆士兰大学,一座雕像纪念着周健。在巴尔的摩的约翰·霍普金斯医院,一块牌匾纪念着亨丽埃塔·拉克斯。在世界各地的实验室里,科学家们继续研究着HPV的奥秘。在诊所和社区健康中心,医生和护士继续进行着筛查和疫苗接种。
这是一场没有硝烟的战争,但它的胜利意味着数百万生命的挽救。这正是医学最崇高的使命。
参考资料
-
zur Hausen H. Papillomaviruses and cancer: from basic studies to clinical application. Nature Reviews Cancer. 2002;2(5):342-350.
-
Frazer IH. HPV vaccines and the prevention of cervical cancer. UpToDate. 2023.
-
World Health Organization. Cervical Cancer. WHO Fact Sheet. 2024.
-
Lowy DR, Schiller JT. Prophylactic human papillomavirus vaccines. Journal of Clinical Investigation. 2006;116(5):1167-1173.
-
Schiller JT, Lowy DR. Understanding and learning from the success of prophylactic human papillomavirus vaccines. Nature Reviews Microbiology. 2022;20(2):87-98.
-
Gillison ML, et al. Evidence for a causal association between human papillomavirus and a subset of head and neck cancers. Journal of the National Cancer Institute. 2000;92(9):709-720.
-
Skloot R. The Immortal Life of Henrietta Lacks. Crown Publishing; 2010.
-
Tan SY, Tatsumura Y. George Papanicolaou (1883-1962): Discoverer of the Pap smear. Singapore Medical Journal. 2015;56(10):586-587.
-
Zhou J, et al. Expression of vaccinia recombinant HPV 16 L1 and L2 ORF proteins in epithelial cells. Journal of Virology. 1991;185:251-257.
-
International Agency for Research on Cancer. Human Papillomaviruses. IARC Monographs on the Evaluation of Carcinogenic Risks to Humans. 2007;90.
-
Centers for Disease Control and Prevention. HPV-Associated Oropharyngeal Cancer Rates by Race and Ethnicity. 2023.
-
Bruni L, et al. Human Papillomavirus and Related Diseases Report. HPV Information Centre. 2023.
-
Simms KT, et al. Impact of scaled up human papillomavirus vaccination and cervical screening and the potential for global elimination of cervical cancer. Lancet Oncology. 2019;20(3):394-407.
-
Drolet M, et al. Population-level impact and herd effects following human papillomavirus vaccination programmes: a systematic review and meta-analysis. Lancet. 2015;384(9960):1597-1608.
-
Doorbar J. Molecular biology of HPV infection and cervical cancer. Clinical Science. 2006;110(5):525-541.
-
Stanley M. Pathology and epidemiology of HPV infection in females. Gynecologic Oncology. 2010;117(2):S5-S10.
-
zur Hausen H. The search for infectious causes of human cancers: Where and how. Virology. 2009;392(1):1-10.
-
Koutsky LA, et al. A controlled trial of a human papillomavirus type 16 vaccine. New England Journal of Medicine. 2002;347(21):1645-1651.
-
Joura EA, et al. A 9-valent HPV vaccine against infection and intraepithelial neoplasia in women. New England Journal of Medicine. 2015;372(8):711-723.
-
WHO Strategic Advisory Group of Experts on Immunization. One-dose human papillomavirus vaccine schedule. 2022.